
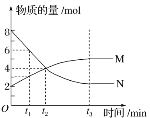
【题目】在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图所示,下列表述正确的是( )
A. 化学方程式:2M![]() N
N
B. t2时,正逆反应速率相等,达到平衡
C. t3时,正反应速率大于逆反应速率
D. t1时,N的浓度是M浓度的2倍
【答案】D
【解析】
A.由图像可知N为反应物,M为生成物,然后找出在相同时间段内变化的M、N的物质的量之比(与是否达平衡无关)以确定M、N在化学方程式中的化学计量数之比,即该反应的化学方程式是:2N![]() M;A项错误;
M;A项错误;
B.t2时刻M、N的物质的量相等,但此时M、N的物质的量仍在发生变化,反应未达到平衡状态,因此正反应速率不等于逆反应速度,反应未到达平衡状态,B项错误;
C.t3时刻及t3时刻之后,M、N的物质的量不再改变,证明已达平衡状态,此时正、逆反应速率相等。C项错误;
D.t1时刻,N的物质的量为6mol,M的物质的量为3mol,在相同的体积下,N的浓度为M浓度的2倍,D项正确;
本题答案选D。


 特高级教师点拨系列答案
特高级教师点拨系列答案科目:高中化学 来源: 题型:
【题目】化学与生产、生活密切相关,下列说法正确的是( )
A.石油的分馏和煤的液化都是物理变化
B.聚乙烯塑料的老化是因为发生了加成反应
C.被称为“黑金”的新型纳米材料石墨烯属于有机化合物
D.利用化学工艺调整织物孔隙直径,可以制作出防水透气面料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,反应4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g) ΔH=-a kJ·mol-1 在5 L密闭容器中进行,10 s时,水蒸气的物质的量增加了0.60 mol。则下列说法不正确的是( )
4NO(g)+6H2O(g) ΔH=-a kJ·mol-1 在5 L密闭容器中进行,10 s时,水蒸气的物质的量增加了0.60 mol。则下列说法不正确的是( )
A. 10 s内,NH3的平均反应速率为0.008 mol·L-1·s-1
B. 该反应达到平衡时6v正(O2)=5v逆(H2O)
C. 10 s内,反应放出的热量为0.1a kJ
D. 10 s时,H2O的反应速率为0.012 mol·L-1·s-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】白磷会对人体造成严重的烧伤,白磷(P4)分子结构如下。下列说法不正确的是( )

A. 已知P4(白磷,s)+3O2(g)===2P2O3(s) ΔH=-Q kJ·mol-1,则白磷的燃烧热为Q kJ·mol-1
B. 白磷着火点低,在空气中可自燃
C. 白磷、红磷互为同素异形体
D. 31 g白磷中,含P—P键1.5 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有八种短周期主族元素x、y、z、d、e、f、 g、h,其中x、y、d、f随着原子序数的递增,其原子半径的相对大小、最高正价或最低负价的变化如图1所示。z、e、g、h的最高价氧化物对应水化物溶液(浓度均为0.01 mol/L)的pH与原子序数的关系如图2所示。
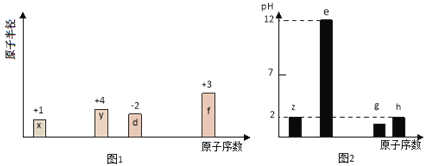
根据上述信息进行判断,并回答下列问题:
(1)g在元素周期表中的位置是____________________。
(2)比较d、e、f的简单离子半径大小为______<______<______(用离子符号表示);y、h 的最高价氧化物对应水化物酸性较强的是__________(用化学式表示)。
(3)下列可作为比较e和f金属性强弱的依据是________。
A.测等浓度相应氯化物水溶液的pH
B.测两种元素单质的硬度和熔、沸点
C.比较单质做还原剂时失去的电子数目的多少
D.比较两种元素在化合物中化合价的高低
E.比较单质与同浓度盐酸反应的剧烈程度
(4)据报道,最近意大利科学家获得了极具研究价值的z4,其分子结构与白磷分子(P4)的正四面体结构相似。已知断裂1 mol z-z键吸收167 kJ热量,生成1 mol Z≡Z键放出942 kJ热量,请写出z4气体在一定条件下生成z2气体反应的热化学方程式___________________。
(5)由上述元素中的y、z、e组成的某剧毒化合物eyz不慎泄露时,消防人员通常采用喷洒过氧化氢溶液的方式处理,以减少污染。反应生成一种酸式盐和一种气体,二者溶于水均呈碱性,该反应的化学方程式为___________________________________________。已知eyz含有z2分子中类似的化学键,写出化合物eyz的电子式____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)根据如图所示情况,判断下列说法中正确的是________。

A.其热化学方程式为:CO(g)+H2O(g)=CO2(g)+H2(g) ΔH=41 kJ·mol-1
B.该反应为吸热反应
C.该反应为放热反应
D.若当H2O为液态时反应热为ΔH2,则ΔH2>ΔH
(2)25℃、101 kPa下,已知1g氢气完全燃烧生成液态水时放出142.9 kJ的热量,表示氢气燃烧热的热化学方程式是_________。
(3)已知反应:N2(g) + O2 (g) = 2NO(g) △H1
2H2(g) + O2(g) = 2H2O(g) △H2
N2(g) + 3H2(g) = 2NH3(g) △H3
利用上述三个反应,计算4NH3(g) + 5O2(g) = 4NO(g) + 6H2O(g) △H4 的反应焓变为________________(用含△H1、△H2、△H3的式子表示)。
(4)在25 ℃、101 kPa下,一定质量的无水乙醇完全燃烧时放出热量Q kJ,其燃烧生成的CO2用过量饱和石灰水吸收可得100 g CaCO3沉淀,则乙醇燃烧的热化学方程式为__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下的定容容器中,当下列哪些物理量不再发生变化时,表明反应A(s)+2B(g)![]() C(g)+D(g)已达到平衡状态( )
C(g)+D(g)已达到平衡状态( )
①混合气体的压强 ②混合气体的密度 ③ B的物质的量浓度 ④混合气体的总物质的量 ⑤混合气体的平均相对分子质量 ⑥v(C)与v(D)的比值 ⑦混合气体的总质量 ⑧C、D的分子数之比为1∶1
A. ②③④⑤ B. ①③⑤⑦ C. ②③⑤⑦ D. ②③⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式中,正确的是( )
A.氯气与水反应:Cl2+H2O=2H++Cl-+ClO-
B.氧化亚铁与稀盐酸混合:FeO+2H+=Fe3++H2O
C.氯化铝与过量氨水反应:Al3++3NH3·H2O=Al(OH)3↓+3NH4+
D.氢氧化钡溶液与稀硫酸H2SO4反应:Ba2++SO42-=BaSO4↓
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将30mL0.5mol/ L NaOH溶液加水稀释到 0.03 mol/L ,则选用的容量瓶规格为
A.100 mLB.250 mLC.500 mLD.1000 mL
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com