
【题目】2016年IUPAC命名117号元素为Ts(中文名“![]() ”,tián),Ts的原子核外最外层电子数是7。下列说法不正确的是
”,tián),Ts的原子核外最外层电子数是7。下列说法不正确的是
A.Ts是第七周期第ⅦA族元素
B.Ts的同位素原子具有相同的电子数
C.Ts在同族元素中非金属性最弱
D.中子数为176的Ts核素符号是![]()
 全优冲刺100分系列答案
全优冲刺100分系列答案 英才点津系列答案
英才点津系列答案 红果子三级测试卷系列答案
红果子三级测试卷系列答案科目:高中化学 来源: 题型:
【题目】在一定温度下,在体积为2L的恒容密闭容器中,某一反应中X、Y、Z三种气体的物质的量随时间变化的曲线如图所示,下列
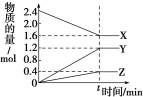
表述中正确的是
A.反应的化学方程式为2X = 3Y + Z
B.t时,正、逆反应都不再继续进行,反应达到化学平衡
C.若t=4,则0~t的X的化学反应速率为0.1 molL-1min-1
D.温度、体积不变,t时刻充入1 mol He使压强增大,正、逆反应速率都增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数的值。下列说法正确的是
A. 1.4gC2H4、C3H6 的混合气体中,所含碳原子总数为 0. lNA
B. 1.0 mol CH4 与 Cl2 在光照下反应生成的 CH3Cl 分子数为 1.0NA
C. 标准状况下,22. 4LC2H6 中所含极性共价键的数目为 7NA
D. 50mL l2mol·L 的浓盐酸与足量 MnO2 反应,转移电子总数为 0. 3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“铝热反应”的化学方程式为2Al+Fe2O3![]() Al2O3+2Fe。某同学对“铝热反应”的现象有这样的描述:“反应放出大量的热,并发出耀眼的光芒”、“纸漏斗的下部被烧穿,有熔融物落入沙中”。查阅《化学手册》知,Al、Al2O3、Fe、Fe2O3熔点、沸点数据如下:
Al2O3+2Fe。某同学对“铝热反应”的现象有这样的描述:“反应放出大量的热,并发出耀眼的光芒”、“纸漏斗的下部被烧穿,有熔融物落入沙中”。查阅《化学手册》知,Al、Al2O3、Fe、Fe2O3熔点、沸点数据如下:
物质 | Al | Al2O3 | Fe | Fe2O3 |
熔点/℃ | 660 | 2 054 | 1 535 | 1 462 |
沸点/℃ | 2 467 | 2 980 | 2 750 | —— |
(1)该同学推测,铝热反应所得到的熔融物应是铁铝合金。这种推测有一定的道理,理由是________________________________________________________________________。
(2)根据已有知识找出一种验证产物中有Fe的最简单方法:_____________________。
(3)设计一个简单的实验方案,证明上述所得的块状熔融物中含有金属铝。该实验所用试剂是________,当观察到________时,说明熔融物中含有金属铝。
(4)实验室溶解该熔融物,最好选用下列试剂中的____(填字母),理由是__________。
A.浓硫酸 B.稀硫酸
C.稀硝酸 D.氢氧化钠溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Na2S2O5是常用的防腐剂和漂白剂。可利用烟道气中的SO2生产Na2S2O5,其流程如下:
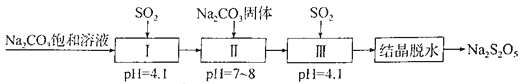
下列说法正确的是
A. 上述制备过程所涉及的物质中只有一种酸性氧化物
B. Na2S2O5作防腐剂和SO2作漂白剂时,均表现还原性
C. 上述流程中的Na2CO3饱和溶液和Na2CO3固体不可互换
D. 实验室模拟“结晶脱水”时用到的仪器只有蒸发皿、玻璃棒、烧杯、漏斗
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知几种短周期元素的原子半径、常见的最高价和最低价如下表,下列说法中不正确的是( )
元素编号 | |||||||
① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | |
原子半径 | 0.073 | 0.075 | 0.152 | 0.110 | 0.099 | 0.186 | 0.143 |
最高正化合价 | 无 |
|
|
|
|
|
|
最低负化合价 |
|
| 无 |
|
| 无 | 无 |
A.⑦的简单离子不是同周期元素离子半径最小的
B.①元素的氢化物有两种
C.②的气态氢化物浓溶液可用于检验氯气管道的泄漏
D.阴离子的还原性④大于⑤,最高价氧化物的水化物的碱性③小于⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NOx是空气的主要污染物之一。回答下列问题:
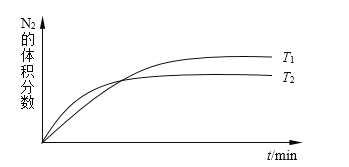
(1)汽车尾气中的NO来自于反应:N2(g)+ O2(g)![]() 2NO(g)。如图表示在不同温度时,一定量NO分解过程中N2的体积分数随时间的变化。则N2(g)+ O2(g)
2NO(g)。如图表示在不同温度时,一定量NO分解过程中N2的体积分数随时间的变化。则N2(g)+ O2(g)![]() 2NO(g)为________(填“吸热”或“放热”)反应。2000℃时,向容积为2L的密闭容器中充入10mol N2和5mol O2,发生上述反应,10min达到平衡,产生2mol NO,则10min内的平均反应速率υ(O2)=____mol·L-1·min-1。
2NO(g)为________(填“吸热”或“放热”)反应。2000℃时,向容积为2L的密闭容器中充入10mol N2和5mol O2,发生上述反应,10min达到平衡,产生2mol NO,则10min内的平均反应速率υ(O2)=____mol·L-1·min-1。
(2)在汽车的排气管上加装催化转化装置可减少NOx的排放。研究表明,NOx的脱除率除与还原剂、催化剂相关外,还取决于催化剂表面氧缺位的密集程度。以La0.8A0.2BCoO3+X(A、B均为过渡元素)为催化剂,用H2还原NO的机理如下:
第一阶段:B4+(不稳定)+H2→低价态的金属离子(还原前后催化剂中金属原子的个数不变)
第二阶段:NO(g)+□→NO(a) ΔH1、K1
2NO(a)→2N(a)+O2(g) ΔH2、K2
2N(a)→N2(g)+2□ ΔH3、K3
2NO(a)→N2(g)+2O(a) ΔH4、K4
2O(a)→O2(g)+2□ ΔH5、K5
注:□表示催化剂表面的氧缺位,g表示气态,a表示吸附态
第一阶段用氢气还原B4+得到低价态的金属离子越多,第二阶段反应的速率越快,原因是_____。第二阶段中各反应焓变间的关系:2ΔH1+ΔH2+ΔH3=________;该温度下,NO脱除反应2NO(g)![]() N2(g)+O2(g)的平衡常数K=_______(用K1、K2、K3的表达式表示)。
N2(g)+O2(g)的平衡常数K=_______(用K1、K2、K3的表达式表示)。
(3)工业废气中的NO和NO2可用NaOH溶液吸收。向20mL0.1mo1·L-1NaOH溶液中通入含NO和NO2的废气,溶液pH随气体体积V的变化如图1所示(过程中温度保持不变),B点对应的溶液中c(HNO2)=c(NO2-),则A点对应溶液中c(NO2-)/c(HNO2)=________。
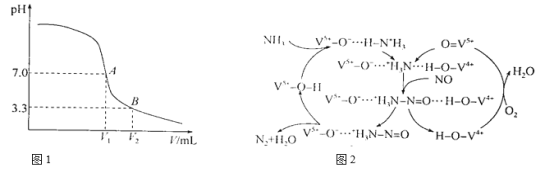
(4)氨催化还原法也可以消除NO,原理如图2所示,NO最终转化为H2O和________(填电子式);当消耗1 molNH3和0.5 molO2时,理论上可消除____________L(标准状况)NO。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】纳米TiO2是一种重要的光催化剂。以钛酸酯Ti(OR)4为原料制备纳米TiO2的步骤如下:
①组装装置如下图所示,保持温度约为65℃,先将30mL钛酸四丁酯[Ti(OC4H9)4]加入盛有无水乙醇的三颈烧瓶,再加入3mL乙酰丙酮,充分搅拌;
②将含水20%的乙醇溶液缓慢滴入三颈烧瓶中,得到二氧化钛溶胶;
③将二氧化钛溶胶干燥得到二氧化钛凝胶,灼烧凝胶得到纳米TiO2。
已知,钛酸四丁酯能溶于除酮类物质以外的大部分有机溶剂,遇水剧烈水解;Ti(OH)4不稳定,易脱水生成TiO2,回答下列问题:
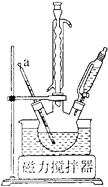
(1)仪器a的名称是_______,冷凝管的作用是________。
(2)加入的乙酰丙酮可以减慢水解反应的速率,其原理可能是________(填标号)。
a.增加反应的焓变 b.增大反应的活化能
c.减小反应的焓变 d.降低反应的活化能
制备过程中,减慢水解反应速率的措施还有________。
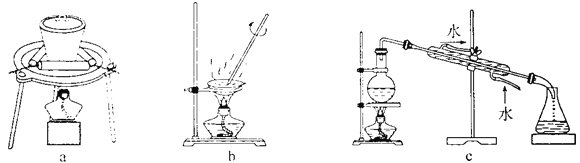
(3)步骤②中制备二氧化钛溶胶的化学方程式为________。下图所示实验装置中,可用于灼烧二氧化钛凝胶的是________(填标号)。
(4)测定样品中TiO2纯度的方法是:精确称取0.2000 g样品放入锥形瓶中,加入硫酸和硫酸铵的混合溶液,加强热使其溶解。冷却后,加入一定量稀盐酸得到含TiO2+的溶液。加入金属铝,将TiO2+全部转化为Ti3+。待过量的金属铝完全溶解并冷却后,加入指示剂,用0.1000 mol·L-lNH4Fe(SO4)2溶液滴定至终点。重复操作2次,消耗0.1000 mol·L-1 NH4Fe(SO4)2溶液的平均值为20.00 mL(已知:Ti3+ +Fe3++H2O=TiO2+ +Fe2+ +2H+)。
①加入金属铝的作用除了还原TiO2+外,另一个作用是________________。
②滴定时所用的指示剂为____________(填标号)
a.酚酞溶液 b. KSCN溶液 c. KMnO4溶液 d.淀粉溶液
③样品中TiO2的质量分数为________%。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镍钼矿(含有MoS2、NiS2、NiS、FeS2、SiO2和C等)为我国特有的一种多金属复杂硫化矿资源,常用来进行钾、镍等战略有色金属的提取。其冶炼工艺主要有氧化焙烧法和选择性还原熔炼法两种。过程如下图所示:
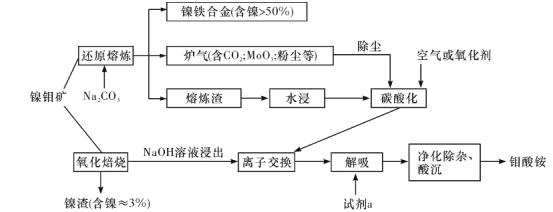
(1)选择性还原熔炼法比氧化焙烧法的优点有_________。
(2)还原熔炼时,FeS2发生的反应为3FeS2+6Na2CO3+11C+8O2![]() 3Fe+6Na2S+17CO2,写出NiS发生反应的化学方程式:______。
3Fe+6Na2S+17CO2,写出NiS发生反应的化学方程式:______。
(3)水浸液中主要含有Na2S、Na2MoO4、Na2CO3、Na2SiO3等,向其中通入适量CO2和空气,然后过滤,所得滤渣的主要成分为____。
(4)已知钼酸钠溶液中c(MoO42-)=0.40mol/L,c(CO32-)=0.10 mol/L。由钼酸钠溶液制备钼酸钠晶体时,需加入Ba(OH)2固体以除去CO32-。当BaMoO4开始沉淀时,CO32-的去除率是______。[已知Ksp( BaCO3)=1×10-9,Ksp(BaMoO4)=4×10-8]
(5)用阴离子交换树脂吸附、提取溶液中的钼,该树脂经解吸、除杂后,用盐酸或硝酸将其酸化至pH=1.5~2.5,可得到钼酸铵产品。试剂a可以是__________。
(6)钼酸钠和月桂酰肌氨酸的混合液常作为碳素钢的缓蚀剂。常温下,碳素钢在三种不同介质中的腐蚀速率实验结果如下图所示:
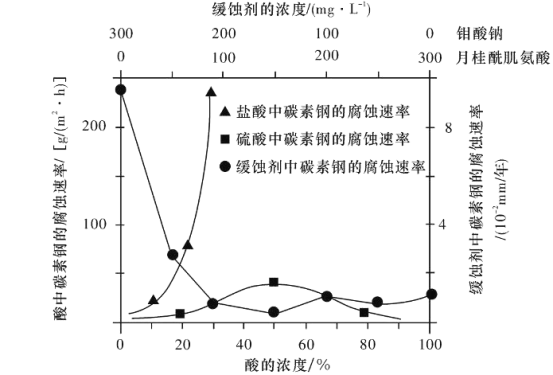
①要使碳素钢的缓蚀效果最优,钼酸钠和月桂酰肌氨酸的浓度比应为________。
②当硫酸的浓度大于90%时,腐蚀速率几乎为零,原因是_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com