
ŌŚŅ»ĆܱÕČŻĘ÷ÖŠÓŠČēĻĀ·“Ó¦£ŗaX£Øg£©£«bY£Øg£© nW£Øg£©£»¦¤H £¬Ä³»ÆѧŠĖȤŠ”×éµÄĶ¬Ń§øł¾Ż“Ė·“Ó¦ŌŚ²»Ķ¬Ģõ¼žĻĀµÄŹµŃ鏿¾Ż£¬×÷³öĮĖČēĻĀĒśĻßĶ¼£ŗ
nW£Øg£©£»¦¤H £¬Ä³»ÆѧŠĖȤŠ”×éµÄĶ¬Ń§øł¾Ż“Ė·“Ó¦ŌŚ²»Ķ¬Ģõ¼žĻĀµÄŹµŃ鏿¾Ż£¬×÷³öĮĖČēĻĀĒśĻßĶ¼£ŗ

ĘäÖŠ£¬¦Ų(W)±ķŹ¾WŌŚ·“Ó¦»ģŗĻĪļÖŠµÄĢå»ż·ÖŹż£¬t±ķŹ¾·“Ó¦Ź±¼ä”£µ±ĘäĖüĢõ¼ž²»±äŹ±£¬ĻĀĮŠ·ÖĪöÕżČ·µÄŹĒ
A£®Ķ¼¢ńæÉÄÜŹĒ²»Ķ¬Ń¹Ēæ¶Ō·“Ó¦µÄÓ°Ļģ£¬ĒŅp2£¾p1£¬a£«b>n
B£®Ķ¼¢ņæÉÄÜŹĒ²»Ķ¬Ń¹Ēæ¶Ō·“Ó¦µÄÓ°Ļģ£¬ĒŅp1£¾p2£¬n£¼a£«b
C£®Ķ¼¢ņæÉÄÜŹĒŌŚĶ¬ĪĀĶ¬Ń¹ĻĀ“߻ƼĮ¶Ō·“Ó¦µÄÓ°Ļģ£¬ĒŅ1Ź¹ÓĆµÄ“ß»Æ¼ĮŠ§¹ūŗĆ
D£®Ķ¼¢óæÉÄÜŹĒ²»Ķ¬ĪĀ¶Č¶Ō·“Ó¦µÄÓ°Ļģ£¬ĒŅT1£¾T2£¬¦¤H£¼0
 ¼ĘĖćøߏÖĻµĮŠ“š°ø
¼ĘĖćøߏÖĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğø£½ØĻĆĆÅŅ»ÖŠøßŅ»ÉĻĘŚÖŠæ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠŹĀŹµÓė½ŗĢåŠŌÖŹĪŽ¹ŲµÄŹĒ
A£®Ļņ¶¹½¬ÖŠ¼ÓČėĮņĖįøĘ×ö¶¹øÆ
B£®½«Ö²ĪļÓĶµ¹ČėĖ®ÖŠÓĆĮ¦½Į°čŠĪ³ÉÓĶĖ®»ģŗĻĪļ
C£®ĄūÓƶ”“ļ¶ūŠ§Ó¦æÉŅŌĒų±šČÜŅŗÓė½ŗĢå
D£®¹Ū擵ēÓ°Ź±£¬“Ó·ÅÓ³»śµ½ŅųĻӊĆ÷ĻŌµÄ¹āĀ·
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğÉĀĪ÷Ź”ø߶žÉĻ10ŌĀŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
C(s)£« O2(g)===CO(g) ¦¤H£½ØD126.4 kJ/mol£¬ÕāøöČČ»Æѧ·½³ĢŹ½±ķŹ¾
O2(g)===CO(g) ¦¤H£½ØD126.4 kJ/mol£¬ÕāøöČČ»Æѧ·½³ĢŹ½±ķŹ¾
A£®1 gĢ¼Č¼ÉÕÉś³ÉŅ»Ńõ»ÆĢ¼Ź±·Å³ö126.4 kJµÄČČĮæ
B£®12 gĢ¼Č¼ÉÕÉś³ÉŅ»Ńõ»ÆĢ¼Ź±ĪüŹÕ126.4 kJµÄČČĮæ
C£®1 mol¹ĢĢåĢ¼ŌŚŃõĘųÖŠČ¼ÉÕÉś³ÉŅ»Ńõ»ÆĢ¼ĘųĢåŹ±·Å³ö126.4 kJµÄČČĮæ
D£®Ģ¼µÄČ¼ÉÕČČĪŖ126.4 kJ/mol
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğ¼ŖĮÖŹ”ø߶žÉĻѧʌʌ֊£ØĄķ£©»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠŹĀŹµÖŠ£¬²»ÄÜÓĆĄÕĻÄĢŲĮŠŌĄķ½āŹĶµÄŹĒ
A£®¶ŌŹģŹÆ»ŅµÄŠü×ĒŅŗ¼ÓČČ£¬Šü×ĒŅŗÖŠ¹ĢĢåÖŹĮæŌö¼Ó
B£®ŹµŃéŹŅÖŠ³£ÓĆÅű„ŗĶŹ³ŃĪĖ®µÄ·½Ź½ŹÕ¼ÆĀČĘų
C£®“ņæŖĘūĖ®Ę棬ӊĘųÅŻ“ÓČÜŅŗÖŠĆ°³ö
D£®ĻņĻ”ŃĪĖįÖŠ¼ÓČėÉŁĮæÕōĮóĖ®£¬ŃĪĖįÖŠĒāĄė×ÓÅØ¶Č½µµĶ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğ¼ŖĮÖŹ”ø߶žÉĻѧʌʌ֊£ØĄķ£©»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
Ģå»żĻąĶ¬µÄ¼×”¢ŅŅĮ½øöČŻĘ÷ÖŠ£¬·Ö±š¶¼³äÓŠµČĪļÖŹµÄĮæµÄSO2ŗĶO2£¬ŌŚĻąĶ¬ĪĀ¶ČĻĀ·¢Éś·“Ó¦£ŗ2SO2£«O2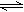 2SO3£¬²¢“ļµ½Ę½ŗā£¬ŌŚÕā¹ż³ĢÖŠ£¬¼×ČŻĘ÷±£³ÖĢå»ż²»±ä£¬ŅŅČŻĘ÷±£³ÖŃ¹Ēæ²»±ä£¬Čō¼×ČŻĘ÷ÖŠSO2µÄ×Ŗ»ÆĀŹĪŖp%£¬ŌņŅŅČŻĘ÷ÖŠSO2µÄ×Ŗ»ÆĀŹ
2SO3£¬²¢“ļµ½Ę½ŗā£¬ŌŚÕā¹ż³ĢÖŠ£¬¼×ČŻĘ÷±£³ÖĢå»ż²»±ä£¬ŅŅČŻĘ÷±£³ÖŃ¹Ēæ²»±ä£¬Čō¼×ČŻĘ÷ÖŠSO2µÄ×Ŗ»ÆĀŹĪŖp%£¬ŌņŅŅČŻĘ÷ÖŠSO2µÄ×Ŗ»ÆĀŹ
A£®µČÓŚp% B£®“óÓŚp% C£®Š”ÓŚ p% D£®ĪŽ·ØÅŠ¶Ļ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğ¼ŖĮÖŹ”ø߶žÉĻѧʌʌ֊£ØĄķ£©»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ÕÓĘųŹĒŅ»ÖÖÄÜŌ“,ĖüµÄÖ÷ŅŖ³É·ÖŹĒCH4.0.5molCH4ĶźČ«Č¼ÉÕÉś³ÉCO2ŗĶĖ®Ź±·Å³ö445KJČČĮæ.ĻĀĮŠÓŠ¹ŲČČ»Æѧ·½³ĢŹ½ÕżČ·µÄŹĒ
A£®2CH4(g)+4O2(g)=2CO2(g)+4H2O(l)£»¦¤H=+890KJ/mol
B£®CH4(g)+ 2O2(g)= CO2(g)+2H2O(l)£»¦¤H=+890KJ/mol
C£®CH4(g)+ 2O2(g)= CO2(g)+2H2O(l)£»¦¤H=-890KJ/mol
D£®1/2 CH4(g)+O2(g)=1/2 CO2(g)+H2O(l)£»¦¤H=-890KJ/mol
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğ¼ŖĮÖŹ”ø߶žÉĻѧʌʌ֊£ØĪÄ£©»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠĪļÖŹŌŚĖ®“¦Ąķ¹ż³ĢÖŠæĻ¶Ø²»»įÓƵ½µÄŹĒ
A£®KAl(SO4)2 •12H2O B£®Cl2
C£®Ca(OH)2 D£®KNO3
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğ¼ŖĮÖŹ”ø߶žÉĻѧʌʌ֊£ØĪÄ£©»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠø÷×éĪļÖŹÖŠ£¬µŚŅ»ÖÖŹĒĖį£¬µŚ¶žÖÖŹĒ»ģŗĻĪļ£¬µŚČżÖÖŹĒ¼īµÄŹĒ
A£®æÕĘų”¢ĮņĖįĶ”¢ĮņĖį B£®Ė®”¢æÕĘų”¢“æ¼ī
C£®Ńõ»ÆĢś”¢µØ·Æ”¢ŹģŹÆ»Ņ D£®ĻõĖį”¢Ź³ŃĪĖ®”¢ÉÕ¼ī
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016½ģÕć½Ź”øßČżÉĻѧʌŌĀæ¼£ØČż£©»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
NH4NO3ŌŚĶس£Ģõ¼žĻĀ¼ÓČČµÄ·Ö½ā·½Ź½ÓŠ¶ąÖÖ£¬Ņ»°ć²»³öĻĀĮŠ·¶Ī§£¬øł¾ŻŅŃѧÖŖŹ¶ÅŠ¶Ļ£¬ĻĀĮŠ·“Ó¦£Ø·“Ó¦Ī“ÅäĘ½£©²»æÉÄܵďĒ£Ø £©
A£®NH4NO3”śN2+O2+H2O B£®NH4NO3”śNH3+HNO3
C£®NH4NO3”śO2+HNO3+H2O D£®NH4NO3”śN2+HNO3 +H2O
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com