
【题目】丙三酸是一种有机酸,用![]() 表示。
表示。![]() 时,向
时,向![]() 的
的![]() 溶液中逐滴加入NaOH溶液,滴加过程中各种含A微粒物质的物质的量分数
溶液中逐滴加入NaOH溶液,滴加过程中各种含A微粒物质的物质的量分数![]() 随溶液pH的变化曲线如图所示。下列相关说法正确的是
随溶液pH的变化曲线如图所示。下列相关说法正确的是
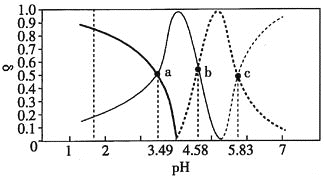
A.a点溶液中:![]()
B.![]() 时,
时,![]() 的第二步电离平衡常数的数量级为
的第二步电离平衡常数的数量级为![]()
C.b点溶液中:![]()
D.当该溶液中![]() 时,溶液中水电离出的
时,溶液中水电离出的![]()
 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:高中化学 来源: 题型:
【题目】不能正确表示下列变化的离子方程式是
A.用醋酸除去水垢:2H++CaCO3=Ca2++CO2↑+H2O
B.用氢氧化钠溶液除去镁粉中的杂质铝:2Al+2OH-+2H2O =2AlO![]() +3H2↑
+3H2↑
C.室温下,测得小苏打溶液pH>7,证明碳酸是弱酸:HCO![]() +H2O
+H2O![]() H2CO3+OH-
H2CO3+OH-
D.将0.10 mol·L-1 NH4Fe(SO4)2溶液与0.40 mol·L-1 NaOH溶液等体积混合: ![]() +Fe3++4OH-=Fe(OH)3↓+NH3·H2O
+Fe3++4OH-=Fe(OH)3↓+NH3·H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将足量的CO2不断通入KOH、Ba(OH)2、KAlO2的混合溶液中,生成沉淀的物质的量与所通入CO2的体积关系如图所示。下列关于整个反应过程中的叙述错误的是
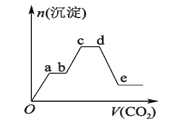
A. Oa段反应的化学方程式是Ba(OH)2+CO2 =BaCO3↓+H2O
B. bc段与cd段所消耗CO2的体积相同
C. bc段反应的离子方程式是2AlO2-+3H2O+CO2 = 2Al(OH)3↓+CO32-
D. de段沉淀减少是由于BaCO3固体的消失
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学用语对事实的表述不正确的是
A. 硬脂酸与乙醇的酯化反应:C17H35COOH+C2H518OH![]() C17H35COOC2H5+H218O
C17H35COOC2H5+H218O
B. 常温时,0.1 mol·L-1氨水的pH=11.1:NH3·H2O![]()
![]() +OH
+OH
C. 由Na和C1形成离子键的过程:![]()
D. 电解精炼铜的阴极反应:Cu2+ +2e![]() Cu
Cu
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计如图装置(气密性已检查)制备Fe(OH)2白色沉淀。

请回答:
(1) 仪器1的名称________。装置5的作用________。
(2) 实验开始时,关闭K2,打开K1,反应一段时间后,再打开K2,关闭K1,发现3中溶液不能进入4中。请为装置作一处改进,使溶液能进入4中________。
(3) 装置改进后,将3中反应后溶液压入4中,在4中析出了灰绿色沉淀。从实验操作过程分析没有产生白色沉淀的原因________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、Q、R是五种短周期元素,原子序数依次增大,X原子是所有原子中半径最小的,Y元素最高正价与最低负价之和为0;Q与X同主族;Z、R分别是地壳中含量最高的非金属元素和金属元素,请回答:
(1)R离子电子排布式为:_____________________。
(2)X与Q形成的化合物属于__________化合物(填“离子”或“共价”)
(3)由以上两种元素组成的化合物中,常温下呈液态的化合物A,原子比例为2:1,其结构式为__________,其熔点,沸点较高时因为分子间存在__________;呈淡黄色固体的化合物B,其电子式:__________。
(4)如果由三种元素组成化合物中,C为两性不溶物,D为强碱,则C与D反应的化学方程式为_____________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制备三氯乙醛(CCl3CHO)的反应原理为C2H5OH+4Cl2![]() CCl3CHO+5HCl,可能发生的副反应是C2H5OH+HCl
CCl3CHO+5HCl,可能发生的副反应是C2H5OH+HCl![]() C2H5Cl+H2O。某探究小组模拟制备三氯乙醛的实验装置如图所示(夹持、加热装置均略去)。
C2H5Cl+H2O。某探究小组模拟制备三氯乙醛的实验装置如图所示(夹持、加热装置均略去)。
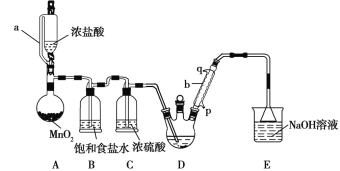
回答下列问题:
(1)用仪器a代替普通分液漏斗的目的是_______________。
(2)装置A中MnO2可以用KMnO4代替,反应可以在常温下进行,试写出反应的离子方程式__。
(3)仪器b中冷凝水从___(填“p”或“q”,下同)口进,___口出。
(4)若撤去装置B,对实验的影响是______________。
(5)实验时发现D中导管口处气泡速率过快,合理的解决方法是___________。
(6)已知:CCl3CHO+OH-![]() CHCl3+HCOO-;HCOO-+I2
CHCl3+HCOO-;HCOO-+I2![]() H++2I-+CO2↑;I2+2S2O32-
H++2I-+CO2↑;I2+2S2O32-![]() 2I-+S4O62-。称取0.40 g产品,配成待测溶液,加入20.00 mL 0.100 mol·L-1碘标准溶液,再加入适量Na2CO3溶液,反应完全后,加盐酸调节溶液的pH,并立即用0.020 mol·L-1的Na2S2O3溶液滴定至终点。重复上述操作3次,平均消耗Na2S2O3溶液20.00 mL。滴定时所用指示剂是___________,达到滴定终点时的现象是_________________,测得该产品的纯度为_____(保留一位小数)。
2I-+S4O62-。称取0.40 g产品,配成待测溶液,加入20.00 mL 0.100 mol·L-1碘标准溶液,再加入适量Na2CO3溶液,反应完全后,加盐酸调节溶液的pH,并立即用0.020 mol·L-1的Na2S2O3溶液滴定至终点。重复上述操作3次,平均消耗Na2S2O3溶液20.00 mL。滴定时所用指示剂是___________,达到滴定终点时的现象是_________________,测得该产品的纯度为_____(保留一位小数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,分别取浓度不同、体积均为20.00mL的3种HCl溶液,分别滴入浓度为1.000mol·L-1,0.1000mol·L-1和0.01000mol·L-1的NaOH溶液,测得3个反应体系的pH随V(NaOH)的变化的曲线如图,在V(NaOH)=20.00mL前后出现突跃。下列说法不正确的是

A. 3种HCl溶液的c(HCl):最大的是最小的100倍
B. 曲线a、b、c对应的c(NaOH):a>b>c
C. 当V(NaOH)=20.00mL时,3个体系中均满足:c(Na+)=c(Cl-)
D. 当V(NaOH)相同时,pH突跃最大的体系中的c(H+)最大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向20 mL0.010 mol·L-1的HA溶液中逐滴加入0.010 mol·L-1的NaOH溶液,溶液中c(OH-)与所加NaOH溶液的体积(V)的关系如图所示。下列说法不正确的是( )
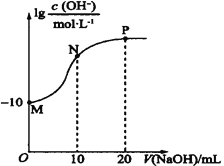
A.常温下,Ka(HA)≈1.0×10-6
B.N点溶液中存在:c(Na+)+c(H+)=c(A-)+c(OH-)
C.P点后的溶液中均存在:c(Na+)>c(A-)>c(OH-)>c(H+)
D.水的电离程度:M<N<P
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com