
| ��� | ||||
| װ�� |  |
 |
 |
 |
| ||
| ||


 ��У������Ԫͬ��ѵ��������ϵ�д�
��У������Ԫͬ��ѵ��������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ����ͼ��ʾ�������ת����ϵ�У�A��һ�ֹ��嵥�ʣ�E��һ�ְ�ɫ������ˮ�����ʣ��ݴ���գ�
����ͼ��ʾ�������ת����ϵ�У�A��һ�ֹ��嵥�ʣ�E��һ�ְ�ɫ������ˮ�����ʣ��ݴ���գ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����Ũ�ȵ������ǿ����ǿ����Һ��Ϻ���Һ��pH=7 |
| B����10 mL pH=a��������100 mL pH=b��Ba��OH��2��Һ��Ϻ�ǡ���кͣ���a+b=13 |
| C��pH=10��Ba��OH��2��Һ��pH=13��NaOH��Һ�������Ϻ���Һ��pH=10.7����֪lg 2=0.3�� |
| D��pH=2��������pH=12�İ�ˮ�������Ϻ�������Һ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
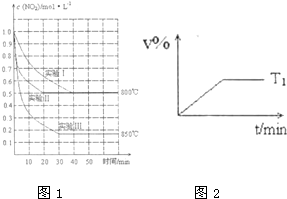 ���Ϊ2L���ܱ������з�Ӧ2NO2��g��?2NO��g��+O2��g�������ֲ�ͬ�����½��У�����ʵ��I��II����800�桢ʵ��III��850�棻NO��O2����ʼŨ�ȶ�Ϊ0��NO2 ��Ũ����ʱ��ı仯��ͼ��ʾ����ش��������⣺
���Ϊ2L���ܱ������з�Ӧ2NO2��g��?2NO��g��+O2��g�������ֲ�ͬ�����½��У�����ʵ��I��II����800�桢ʵ��III��850�棻NO��O2����ʼŨ�ȶ�Ϊ0��NO2 ��Ũ����ʱ��ı仯��ͼ��ʾ����ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�������£�pH��ͬ��CH3COOH��Һ��HCN��Һ�ֱ��ˮϡ����ͬ�ı���ʱ��ǰ��pH�仯��С |
| B�������£���Ũ�ȵ�CH3COOH��HCN��ҺpH�����ߴ� |
| C��HCN��Һ��NaOH���������Ϻ�һ���������¹�ϵc��H+��-c��OH-���Tc��CN-��-c��Na+�� |
| D��0.1mol?L-1CH3COOH��HCN��Һ����ˮ�������c��H+����ǰ���Ǻ��ߵ�10m-n�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A��
| ||||
B��Ag+��H+
| ||||
| C��NH4+��Br-��Na+��SO42- | ||||
D��H+��CI-��Fe2+
|
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ����ϩΪԭ�Ϻϳɻ�����C��������ͼ��ʾ��
����ϩΪԭ�Ϻϳɻ�����C��������ͼ��ʾ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������42.0 L N2����״���� |
| B����0.250 mol KN03������ |
| C��ת�Ƶ��ӵ����ʵ���Ϊ1.25 mol |
| D����������Nԭ�ӵ����ʵ���Ϊ3.75 mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��Fe3+��H+��ClO-��SO32- |
| B��K+��Al3+��Cl-��CO32- |
| C��Na+��Ca2+��HCO3-��OH- |
| D��Al3+��NH4+��Cl-��SO42- |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com