
���Ļ������ж�������+6��Cr��ǿ�����ԣ��䶾����+3��Cr���Ե�100������ˣ�����Ժ����ķ�ˮ���д�����Ŀǰ�о��Ͳ��õĴ���������Ҫ�У�
����һ����ԭ����
���������Խ�������FeSO4��NaHSO3�Ƚ�+6��Cr��ԭ��+3��Cr�������������£�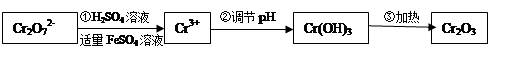
��ش��������⣺
��1���������̢ٷ�����Ӧ�����ӷ���ʽ�� ��
��2�����ڢ� ʹFeSO4�ʵ������������������ɲ������д��ԡ���������������壨Fe3O4��FeO��Fe2O3���ĸ�������� ��y
��y O��(ע��X�����Ƿ���)�����Ϊ��������ƿ���������Ŀ���� ��ʹ�������������ϼ��ķ����� �����账����1 mol Cr2O72���ķ�ˮ������Ҫ����10mol FeSO4��7H2O�������
O��(ע��X�����Ƿ���)�����Ϊ��������ƿ���������Ŀ���� ��ʹ�������������ϼ��ķ����� �����账����1 mol Cr2O72���ķ�ˮ������Ҫ����10mol FeSO4��7H2O������� ��y
��y O����ѧʽ�� ��
O����ѧʽ�� ��
�����о����֣�����������ԭ���������Գ�ȥCr6+�����ܳ�ȥ��ˮ�е�����Mn2+�����о���м������pHֵ�Է�ˮ�и�����ȥ���ʵ�Ӱ�죬
��3��ȡ100mL��ˮ��250 mL����ƿ�У�����pHֵ���涨ֵ���ֱ���벻ͬ���ķ���м���õ���м�����Ը�����ȥ���ʵ�Ӱ������ͼ1��ʾ������pHһ��ʱ����ˮ����м����Ϊ ʱ�̡���ȥ�������
��4��ȡ100mL��ˮ��250 mL����ƿ�У�����涨�������ۣ����ɲ�ͬ��pHֵ���õ�pHֵ�Ը�����ȥ���ʵ�Ӱ������ͼ2��ʾ��������м����һ��ʱ����ˮpH= ʱ�̡���ȥ�������

����������ⷨ������+6��Cr�ķ�ˮ��������ڣ������������������������Ȼ��ƽ��е�⣺���������ɵ�Fe2+��Cr2O72-������Ӧ�����ɵ�Fe3+��Cr3ʮ����������OHһ�������Fe��OH��3��Cr��OH��3������ȥ��
��5��д����������Ӧ�ĵ缫����ʽ ��
��6�������Ϸ�����1��104 L������+6�ۣ�78 mg / L�ķ�ˮ�����ʱ�����������ĵ���������Ϊ________kg��
��16�֣���1��Cr2O72-��14H+��6Fe2+=6Fe3+��2Cr3ʮ��7H2O��2�֣���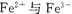
��2��ʹ��Һ�еı���ǡ�������ֹFe2+�����������������Ը��֣���2�֣�
�ô���������2�֣� Cr0.5Fe1.5O3��FeO��2�֣�
��3��15% ��2�֣���4�� 4 ��2�֣���5��2H2O��2e����H2����2OH���� ��2�֣� ��6�� 2��52 ��2�֣�
���������������1��Cr2O72���н�ǿ�����ԣ�FeSO4��Fe2+��һ���Ļ�ԭ�ԣ������Խ����з���������ԭ��Ӧ����ʵ�����̿�֪���ڢٲ���Ӧ��Cr2O72�������������½�Fe2+����ΪFe3+����������ԭΪCr3+�������غ�Ԫ���غ㼰����������֪����Ӧ��ˮ���ɣ���Ӧ���ӷ���ʽΪCr2O72��+14H++6Fe2+=2Cr3++6Fe3++7H2O��
��2�������к������������������������Fe2+����������������ʹ��Һ��Fe2����Fe3���ı�����ǡ����������������д��ԣ�����ʹ�������������ϼ��ķ������ô������������ݷ�Ӧ�����ӷ���ʽ��֪��1mol Cr2O72��������6mol�������ӣ�ͬʱ����2mol Cr3ʮ����ʣ���������ӵ����ʵ�����4mol�����Ը���ԭ���غ�ͻ��ϼ۴�����Ϊ0��֪��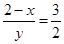 ��3x��6��3x��2y��8�����x��0.5��y��1�����Ը���������Ļ�ѧʽ��Cr0.5Fe1.5O3��FeO��
��3x��6��3x��2y��8�����x��0.5��y��1�����Ը���������Ļ�ѧʽ��Cr0.5Fe1.5O3��FeO��
��3������ͼ1֪����������������ʱ�����ӵ�ȥ������������С������ˮ����м����Ϊ15%ʱ�̡���ȥ������á�
��4������ͼ2֪������Һ��pHֵ������ʱ�������ӵ�ȥ�����ȼ�С��������ȥ������������С����pH=4ʱ�̡���ȥ������á�
��5�������������õ����ӣ���������ˮ������������ӵõ����ӣ�����������Ӧ�ĵ缫����ʽ2H2O��2e����H2����2OH����
��6��1��104 L������+6�ۣ�78 mg / L�ķ�ˮ�и�Ԫ�ص�������78 mg / L��10000��780000mg��780g�����ʵ�����780g��52g/mol��15mol���ڷ�Ӧ�еõ�15mo��3��45mol���ӣ���˸��ݵ��ӵĵ�ʧ�غ��֪���μӷ�Ӧ������������45mol����������������������������45mol��56g/mol��2520g��2.52kg��
���㣺�������ӷ���ʽ��������ԭ��Ӧ���缫��Ӧʽ���й��ж��Լ��йؼ���
�����������Թ�ҵ��ˮ����Ϊ���壬����������ԭ��Ӧ�����ӷ�Ӧ���缫��Ӧʽ����д�Լ��йؼ���ȣ��Ѷ��еȣ��ؼ�����ʵ����������������ԭ��Ӧ�жϷ��������ӷ�Ӧ���Ƕ�ѧ���ۺ������Ŀ��飮��һ�����������������⣬����������ѧ���������������ͷ�ɢ˼ά������Ҳ����������ѧ���Ļ���������ʶ������ѧ����ѧ��������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
 ��֪Cr��OH��3�ڼ��Խ�ǿ����Һ�н�����[Cr��OH��4]-�����Ļ������ж�������+6�۸���ǿ�����ԣ��䶾����+3�۸����Ե�100������ˣ�����Ժ����ķ�ˮ���д������ɲ����������ַ�����
��֪Cr��OH��3�ڼ��Խ�ǿ����Һ�н�����[Cr��OH��4]-�����Ļ������ж�������+6�۸���ǿ�����ԣ��䶾����+3�۸����Ե�100������ˣ�����Ժ����ķ�ˮ���д������ɲ����������ַ�����
| ����� | Fe2+ | Fe3+ | Cr3+ |
| ��ȫ����Ϊ��Ӧ���������pH | 9.0 | 3.2 | 5.6 |
| O | 2- 7 |
| O | 2- 7 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

| ����� | Fe2+ | Fe3+ | Cr3+ |
| ��ȫ����Ϊ��Ӧ���������pH | 9.0 | 3.2 | 5.6 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��12�֣���֪Cr(OH)3�ڼ��Խ�ǿ����Һ�н�����[Cr(OH)4] �D�����Ļ������ж�������+6�۸���ǿ�����ԣ��䶾����+3�۸����Ե�100������ˣ�����Ժ����ķ�ˮ���д������ɲ����������ַ�����
[����һ]��ԭ�� �����Խ�������FeSO4�Ƚ�+6�۸���ԭ��+3�۸���
�����������£�

�й�������ȫ������pH���±���
| ����� | Fe2+ | Fe3+ | Cr3+ |
| ��ȫ����Ϊ��Ӧ���������pH | 9.0[ | 3.2 | 5.6 |
��1��д��Cr2O72�D��FeSO4��Һ�����������·�Ӧ�����ӷ���ʽ �� ��
��2����ԭ+6�۸�����ѡ�����µ� �� �Լ�������ţ���
A������ B����м C����ʯ�� D������������
��3���ں�����ˮ�м���FeSO4���ٵ���pH��ʹFe3+��Cr3+��������������������ڲ������п����ڵ�����ҺpH���Լ�Ϊ�� �� ������ţ���
A��Na2O2 B��Ba(OH)2 C��Ca(OH)2 D��NaOH
��ʱ������Һ��pH��Χ�� �� ������ţ���ѡ�
A��3��4 B��6��8 C��10��11 D��12��14
[������]��ⷨ ����+6�۸��ķ�ˮ��������ڣ������������������������Ȼ��ƽ��е�⡣���������ɵ�Fe2+��Cr2O72һ������Ӧ�����ɵ�Fe3+��Cr3+����������OHһ�������Fe(OH)3��Cr(OH)3������ȥ��
��4��д�������ĵ缫��Ӧʽ �� ��
��5����ⷨ�м����Ȼ��Ƶ������ǣ� �� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012�콭��ʡ�����߿�ѹ�ữѧ�Ծ� ���������� ���ͣ������
��12�֣���֪Cr(OH)3�ڼ��Խ�ǿ����Һ�н�����[Cr(OH)4]�D�����Ļ������ж�������+6�۸���ǿ�����ԣ��䶾����+3�۸����Ե�100������ˣ�����Ժ����ķ�ˮ���д������ɲ����������ַ�����
I����ԭ�� �����Խ�������FeSO4�Ƚ�+6�۸���ԭ��+3�۸��������������£�
�й�������ȫ������pH���±���
| ����� | Fe2+ | Fe3+ | Cr3+ |
| ��ȫ����Ϊ��Ӧ���������pH | 9.0 | 3.2 | 5.6 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2011-2012ѧ�꽭��ʡ�����߿�ѹ�ữѧ�Ծ��������棩 ���ͣ������
��12�֣���֪Cr(OH)3�ڼ��Խ�ǿ����Һ�н�����[Cr(OH)4]�D�����Ļ������ж�������+6�۸���ǿ�����ԣ��䶾����+3�۸����Ե�100������ˣ�����Ժ����ķ�ˮ���д������ɲ����������ַ�����
I����ԭ�� �����Խ�������FeSO4�Ƚ�+6�۸���ԭ��+3�۸��������������£�

�й�������ȫ������pH���±���
|
����� |
Fe2+ |
Fe3+ |
Cr3+ |
|
��ȫ����Ϊ��Ӧ���������pH |
9.0 |
3.2 |
5.6 |
��1��д��Cr2O72�D��FeSO4��Һ�����������·�Ӧ�����ӷ���ʽ__________________��
��2����ԭ+6�۸�����ѡ�����µ�________________�Լ�������ţ���
A������ B����м C����ʯ�� D������������
��3���ں�����ˮ�м���FeSO4���ٵ���pH��ʹFe3+��Cr3+�����������������
���ڲ������п����ڵ�����ҺpH���Լ�Ϊ��_____________������ţ���
A��Na2O2 B��Ba(OH)2 C��Ca(OH)2 D��NaOH
��ʱ������Һ��pH��Χ��____________������ţ���ѡ�
A��3��4 B��6��8 C��10��11 D��12��14
II����ⷨ ����+6�۸��ķ�ˮ��������ڣ������������������������Ȼ��ƽ��е�⡣���������ɵ�Fe2+��Cr2O72һ������Ӧ�����ɵ�Fe3+��Cr3+����������OHһ�������Fe(OH)3��Cr(OH)3������ȥ��
��4��д�������ĵ缫��Ӧʽ______________________________________��
��5����ⷨ�м����Ȼ��Ƶ������ǣ�_______________________________________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com