
将一定量的Na2O2和NaHCO3混合后,在密闭容器中加热充分反应,排出气体,冷却后有固体物质剩余,下列选项不正确的是 ( )。
| Na2O2/mol | NaHCO3/mol | 剩余的固体物质 | |
| A | 1 | 2 | Na2CO3 |
| B | 1.5 | 2 | Na2O2 Na2CO3 |
| C | 2 | 1 | Na2O2 NaOH Na2CO3 |
| D | 2 | 2 | NaOH Na2CO3 |
解析 有关的反应方程式依次为2NaHCO3 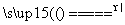 Na2CO3+CO2↑+H2O、2CO2+2Na2O2===2Na2CO3+O2、2Na2O2+2H2O===4NaOH+O2↑。当Na2O2与NaHCO3的物质的量之比为1∶2时,二者反应的总方程式为2Na2O2+4NaHCO3
Na2CO3+CO2↑+H2O、2CO2+2Na2O2===2Na2CO3+O2、2Na2O2+2H2O===4NaOH+O2↑。当Na2O2与NaHCO3的物质的量之比为1∶2时,二者反应的总方程式为2Na2O2+4NaHCO3 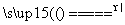 4Na2CO3+O2↑+2H2O;当Na2O2与NaHCO3的物质的量之比为1∶1时,2Na2O2+2NaHCO3
4Na2CO3+O2↑+2H2O;当Na2O2与NaHCO3的物质的量之比为1∶1时,2Na2O2+2NaHCO3 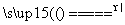 2Na2CO3+O2↑+2NaOH,即1∶2<n(Na2O2)∶n(NaHCO3)≤1∶1,反应后剩余固体的成分为Na2CO3和NaOH,n(Na2O2)∶n(NaCO3)>1∶1时,反应后剩余固体为Na2O2、NaOH、Na2CO3,由此可以判断A、C、D对,B错。
2Na2CO3+O2↑+2NaOH,即1∶2<n(Na2O2)∶n(NaHCO3)≤1∶1,反应后剩余固体的成分为Na2CO3和NaOH,n(Na2O2)∶n(NaCO3)>1∶1时,反应后剩余固体为Na2O2、NaOH、Na2CO3,由此可以判断A、C、D对,B错。
答案 B


科目:高中化学 来源: 题型:
某校化学实验兴趣小组为了探究在实验室制备Cl2的过程中有水蒸气和HCl挥发出来,同时证明氯气的某些性质,甲同学设计了如图所示的实验装置(支撑用的铁架台省略),完成下列问题。
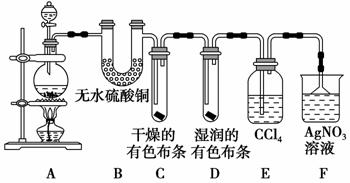
(1)装置B、E的作用分别为_________________________________,
________________________________。
(2)装置C、D的作用分别为________________________________________,
________________________________。
(3)装置F中AgNO3溶液的作用是________,倒置漏斗的作用是________。
(4)乙同学认为甲同学的实验有缺陷,不能确保最终通入AgNO3溶液中的气体只有一种。为了确保实验结论的可靠性,证明最终通入AgNO3溶液的气体只有一种,乙同学提出在某两个装置之间加一个装置。你认为该装置加在________与________之间(填装置各部分字母),装置中应放入________,作用是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于铁的叙述正确的是 ( )。
①铁能被磁铁吸引,但纯铁易被腐蚀 ②在人体内的血红蛋白中含有铁元素 ③铁位于元素周期表中第四周期第ⅧB族 ④铁能在氧气中剧烈燃烧,但不能在水蒸气中燃烧 ⑤铁与强氧化剂硝酸反应的产物仅是Fe(NO3)3 ⑥不能通过化合反应制得FeCl2和Fe(OH)3
A.①③ B.②④
C.②⑤ D.④⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
向一定量的NaOH溶液中逐滴加入AlCl3溶液,生成沉淀Al(OH)3的量随AlCl3加入量的变化关系如图所示。则下列离子组在对应的溶液中一定能大量共存的是 ( )。
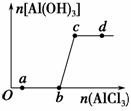
A.a点对应的溶液中:Na+、Fe3+、SO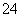 、HCO
、HCO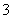
B.b点对应的溶液中:Na+、S2-、SO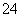 、Cl-
、Cl-
C.c点对应的溶液中:Ag+、Ca2+、NO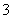 、F-
、F-
D.d点对应的溶液中:K+、NH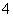 、I-、CO
、I-、CO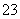
查看答案和解析>>
科目:高中化学 来源: 题型:
铝是现今人类生产生活中使用广泛性仅次于铁的重要金属。工业上常以“钒土矿”为原料来冶炼金属铝。已知:钒土的主要成分是Al2O3(其中含有Fe2O3、SiO2等杂质)。为了检测某“钒土矿”样中Al2O3的含量,进行了如下实验过程:
①取矿样10.0 g加入过量稀盐酸溶解(假定其他未知成分的杂质都不溶于盐酸,也不和盐酸反应),过滤弃去不溶残渣。
②将滤液稀释并在250 mL容量瓶中定容后,取25.0 mL逐滴滴加2.0 mol·L-1的NaOH溶液,得到如图所示的变化关系。请根据有关数据回答下列问题:

(1)写出滴加NaOH溶液24~30 mL时发生反应的离子方程式:______________________________。
(2)最后所得不溶于NaOH溶液的沉淀的化学式为________,其物质的量为______________。
(3)该“钒土矿”样中Al2O3的质量分数为________。
(4)工业上制取金属铝的化学反应原理可表示为
2Al2O3(熔融) 4Al+3O2↑
4Al+3O2↑
用10.0 t “钒土矿”样提纯所得的Al2O3(提纯过程的损耗忽略不计)进行电解,理论上最多可制得金属铝________ t,假定Al2O3在熔融状态完全电离为Al3+和O2-,则电解过程的阳极反应式为_____________________ ___________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
一化学研究性学习小组对某Na2CO3和NaHCO3混合溶液的组成进行探究。取20.0 mL该混合溶液不断加入1.00 mol·L-1的稀盐酸,加入盐酸的体积和产生的现象见下表。
| 反应阶段 | Ⅰ | Ⅱ | Ⅲ |
| 盐酸体积x/mL | 0<x≤10.0 | 10.0<x≤40.0 | x>40.0 |
| 现象 | 无气体 | 产生气体 | 无气体 |
则混合溶液中c(HCO )为 ( )。
)为 ( )。
A.1.00 mol·L-1 B.0.50 mol·L-1
C.1.50 mol·L-1 D.2.00 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
已知离子方程式:As2S3+H2O+NO ―→AsO
―→AsO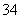 +SO
+SO +NO↑+________(未配平),下列说法错误的是 ( )。
+NO↑+________(未配平),下列说法错误的是 ( )。
A.配平后水的化学计量数为4
B.反应后溶液呈酸性
C.配平后氧化剂与还原剂的物质的量之比为3∶28
D.氧化产物为AsO 和SO
和SO
查看答案和解析>>
科目:高中化学 来源: 题型:
有一无色溶液,可能含有K+.Al3+.Mg2+.NH4+.Cl-.SO42-.HCO3-.MnO4-中的几种。为确定其成分,做如下实验:①取部分溶液,加入适量Na2O2固体,产生无色无味的气体和白色沉淀,再加入足量的NaOH溶液后白色沉淀部分溶解;②另取部分溶液,加入HNO3酸化的Ba(NO3)2溶液,有白色沉淀产生。下列推断正确的是
A.肯定有Al3+.Mg2+.NH4+.Cl- B.可能有K+.Cl-.MnO4-
C.肯定有Al3+.Mg2+.SO42- D.肯定有K+.HCO3-.MnO4-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com