
【题目】X、Y、Z、W是原子序数依次增大的前四周期元素,X、Z的周期序数=族序数,由这四种元素组成的单质或化合物存在如图所示的转化关系,其中甲、戊是两常见的金属单质,丁是非金属单质,其余为氧化物且丙为具有磁性的黑色晶体。下列说法正确的是

A.丙属于碱性氧化物
B.W元素在周期表中的位置是第四周期VIIIB族
C.W的原子序数是Z的两倍,金属性弱于Z
D.常温下等物质的量的甲和戊加入过量浓硝酸中,消耗的HNO3物质的量相等
【答案】C
【解析】
X、Y、Z、W是原子序数依次增大的前四周期元素,X、Z的周期序数═族序数,应分别为H、Al元素,由这四种元素组成的单质或化合物存在如图所示的转化关系,其中甲、戊是两常见的金属单质,丁是非金属单质,其余为氧化物且丙为具有磁性的黑色晶体,则丙为Fe3O4,由转化关系可知甲为Fe、乙为H2O,丁为H2,戊为Al、己为Al2O3,则对应X、Y、Z、W分别为H、O、Al、Fe元素。
A. 丙为Fe3O4,不是两性氧化物,故A错误;
B. W为Fe,原子序数为26,位于第四周期Ⅷ族,故B错误;
C. 由金属活动顺序可知Fe的金属性比Al弱,故C正确;
D. 常温下等物质的量的甲和戊加入过量浓硝酸中,均产生钝化现象,故D错误;
故选C。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】下列说法中正确的是![]()
A.同时含有分子和离子的电解质溶液,一定是弱电解质溶液
B.pH为1的盐酸中,其![]() 是pH为3的盐酸中的100倍
是pH为3的盐酸中的100倍
C.室温时,![]() 的硫酸和
的硫酸和![]() 的NaOH溶液等体积混合,混合溶液的
的NaOH溶液等体积混合,混合溶液的![]()
D.![]() 溶液和
溶液和![]() 盐酸中,其水电离出的
盐酸中,其水电离出的![]() 相等
相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaOH溶液滴定邻苯二甲酸氢钾(邻苯二甲酸氢钾H2A的Ka1=1.1×103 ,Ka2=3.9×106)溶液,混合溶液的相对导电能力变化曲线如图所示,其中b点为反应终点。下列叙述错误的是
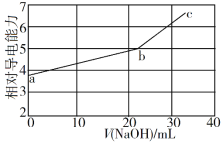
A. 混合溶液的导电能力与离子浓度和种类有关
B. Na+与A2的导电能力之和大于HA的
C. b点的混合溶液pH=7
D. c点的混合溶液中,c(Na+)>c(K+)>c(OH)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,关于下列溶液的说法错误的是
A.某物质的溶液中由水电离出的c(H+)=1×10-10mol/L,则该溶液的pH可能为4或10
B.已知0.1 mol/L NaClO溶液的pH为9.7,0.1 mol/LNaF溶液的pH为7.5,则等体积两溶液中离子总数大小关系为:N(NaClO)>N(NaF)
C.将0.2 mol/L的某一元酸HA溶液和0.1 mol/LNaOH溶液等体积混合后溶液pH大于7,则所得溶液中:2c(OH-)=2c(H+)+c(HA)-c(A-)
D.向饱和氯水中加入NaOH溶液至PH=7,则所得溶液中:c(Na+) >c(Cl-) >c(ClO-) >c(OH-)= c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25 ℃时,某一元酸(HB)的盐NaB的水溶液呈碱性,下列叙述正确的是( )
A.HB的电离方程式为HB===H++B-
B.NaB溶液中:c(Na+)>c(B-)>c(H+)>c(OH-)
C.NaB溶液中:c(Na+)+c(H+)=c(HB)+c(B-)
D.0.1 mol/L NaB溶液中水电离的OH-浓度大于10-7 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D为原子序数依次增大的短周期主族元素,a、d分别是A、D元素对应的单质,m、n、p、q是由这些元素中的部分元素组成的化合物,气体p常作果实催熟剂,m、n为两种常见的液体。上述物质发生的转化关系如下图所示(反应条件已略去)。下列说法错误的是
![]()
A.原子半径由大到小的顺序为:D>B>C>A
B.简单氢化物的沸点:B<C
C.d与m反应的现象为浮在液面上四处游动
D.C与D形成的化合物中一定含有离子键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,将一元酸HA的溶液和KOH溶液等体积混合(忽略体积变化),实验数据如下表:
实验编号 | 起始浓度/(mol·L-1) | 反应后溶液的pH | |
c(HA) | c(KOH) | ||
① | 0.1 | 0.1 | 9 |
② | x | 0.2 | 7 |
下列判断不正确的是
A.实验①反应后的溶液中:c(K+)>c(A-)>c(OH-)>c(H+)
B.实验①反应后的溶液中:c(OH-)=c(K+)-c(A-)=![]() mol/L
mol/L
C.实验②反应后的溶液中:c(A-)+c(HA)>0.1mol·L-1
D.实验②反应后的溶液中:c(K+)=c(A-)>c(OH-) =c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有硫酸与硝酸的混合液,取出其中10mL,加入足量的BaCl2溶液,将生成的沉淀过滤洗涤,干燥称得质量为4.66g。另取这种溶液10mL与2mol·L-1的NaOH溶液25mL恰好中和。则:
(1)混合液中c(H2SO4)=__mol·L-1,c(HNO3)=__mol·L-1
(2)另取10mL的混合液(混合液中的硝酸视为稀硝酸)与0.96g铜粉共热时,产生气体的体积为__L(标准状况)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,向一密闭容器中充入一定量的NH3,反应2NH3(g)![]() N2(g)+3H2(g)达到平衡时N2的体积分数与温度、压强的关系如图所示。下列说法正确的是
N2(g)+3H2(g)达到平衡时N2的体积分数与温度、压强的关系如图所示。下列说法正确的是
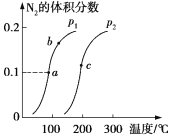
A. 压强:p1>p2
B. b、c两点对应的平衡常数:Kc>Kb
C. a点:2v(NH3)正=3v(H2)逆
D. a点:NH3的转化率为1/3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com