
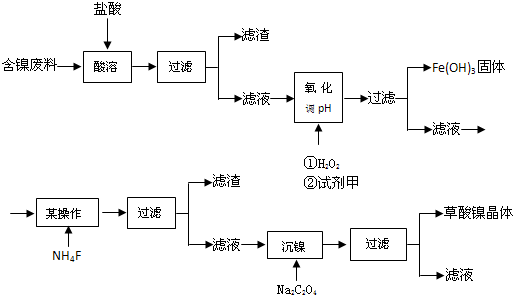
分析 含镍废料用盐酸溶解,Cu、C不与盐酸反应,过滤得到滤渣中含有Cu、C,滤液中含有NiCl2、FeCl2、MgCl2、CaCl2及过量的HCl,加入H2O2将Fe2+氧化为Fe3+,加入镍的混合物调节pH使Fe3+转化为Fe(OH)3沉淀,过滤除去,滤液中含有NiCl2、MgCl2、CaCl2,向滤液中加入NH4F,过滤,再向滤液中加入Na2C2O4,过滤得到草酸镍晶体,故加入NH4F应是除去溶液中Ca2+、Mg2+.
(1)过氧化氢受热易分解,所以温度不能过高;Fe、Ca、Mg均与盐酸直接反应,过氧化氢的加入造成酸溶过滤后的滤液中增加一种金属离子,则该金属离子只能是铜离子;
(2)根据Ksp[(Fe(OH))3]计算反应中c(OH-),再根据水的离子积计算c(H+),调节溶液pH=-lgc(H+);
(3)加入NH4F后的操作是过滤,说明该过程有沉淀产生,所以加入NH4F的目的是除去Ca2+、Mg2+;
(4)根据题目可知无毒气体是二氧化碳,同时有水生成,由氧元素守恒可知,应有氧气参加反应,配平书写方程式;
(5)根据氧化还原反应理论,Cl2氧化Ni(OH)2生成三氧化二镍,自身被还原为氯离子,还有水生成,配平书写化学方程式,根据电子转移守恒计算反应中需要氯气物质的量,再根据氯气利用率计算电解生成氯气物质的量,根据电子转移守恒计算电路中通过电子;
(6)NiO(OH)中Ni的化合价是+3价,Ni(OH)2中Ni是+2价,化合价降低,发生还原反应,所以放电时负极应发生氧化反应,LaNi5H6为负极反应物质,LaNi5H6中各元素化合价均可看作是零,所以化合价升高的只能是H元素,碱性条件下得到LaNi5与H2O.
解答 解:含镍废料用盐酸溶解,Cu、C不与盐酸反应,过滤得到滤渣中含有Cu、C,滤液中含有NiCl2、FeCl2、MgCl2、CaCl2及过量的HCl,加入H2O2将Fe2+氧化为Fe3+,加入镍的混合物调节pH使Fe3+转化为Fe(OH)3沉淀,过滤除去,滤液中含有NiCl2、MgCl2、CaCl2,向滤液中加入NH4F,过滤,再向滤液中加入Na2C2O4,过滤得到草酸镍晶体,故加入NH4F应是除去溶液中Ca2+、Mg2+.
(1)过氧化氢受热易分解,所以温度不能过高的目的是减少过氧化氢的分解;Fe、Ca、Mg均与盐酸直接反应,过氧化氢的加入造成酸溶过滤后的滤液中增加一种金属离子,则该金属离子只能是铜离子,所以反应的离子方程式为:Cu+H2O2+2H+=Cu2++2H2O,
反应答案为:减少过氧化氢的分解;Cu+H2O2+2H+=Cu2++2H2O;
(2)Ksp[(Fe(OH))3]=4.0×10-38=c(Fe3+)×[c(OH-)]3,则[c(OH-)]3=8×10-33mol/L,则c(OH-)=2×10-11mol/L,所以c(H+)=5×10-4,故pH=-lg5×10-4=3.3,
故答案为:3.3;
(3)加入NH4F后的操作是过滤,说明该过程有沉淀产生,所以加入NH4F的目的是除去Ca2+、Mg2+,故答案为:除去Ca2+、Mg2+;
(4)根据题目可知无毒气体是二氧化碳,同时有水生成,由氧元素守恒可知,应有氧气参加反应,所以化学方程式为4(NiC2O4•2H2O)+3O2 $\frac{\underline{\;△\;}}{\;}$2Ni2O3+8CO2+8H2O,
故答案为:4(NiC2O4•2H2O)+3O2 $\frac{\underline{\;△\;}}{\;}$2Ni2O3+8CO2+8H2O;
(5)根据氧化还原反应理论,Cl2氧化Ni(OH)2生成三氧化二镍,自身被还原为氯离子,还有水生成,化学方程式为:Cl2+2Ni(OH)2+2OH-=Ni2O3+2Cl-+3H2O;amol二价镍全部转化为三价镍时,根据电子转移守恒需要氯气$\frac{amol×1}{2}$=0.5amol,氯气的利用率是80%,则电解过程中的氯气是$\frac{0.5amol}{80%}$=0.625a mol,每生成1mol氯气转移2mol电子,所以外电路中通过电子的物质的量是0.625a mol×2=1.25amol,
故答案为:Cl2+2Ni(OH)2+2OH-=Ni2O3+2Cl-+3H2O;1.25amol;
(6)NiO(OH)中Ni的化合价是+3价,Ni(OH)2中Ni是+2价,化合价降低,发生还原反应,所以放电时负极应发生氧化反应,LaNi5H6为负极反应物质,LaNi5H6中各元素化合价均可看作是零,所以化合价升高的只能是H元素,碱性条件下得到LaNi5与H2O,电极反应式为:LaNi5H6+6OH--6e-=LaNi5+6 H2O,
故答案为:LaNi5H6+6OH--6e-=LaNi5+6 H2O.
点评 本题考查制备方案,涉及化学工艺流程、对操作与试剂的分析评价、化学方程式书写、原电池与电解原理等,是对学生综合能力的考查,需要学生具备扎实的基础与迁移运用能力,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 4mol | B. | 8mol | C. | 16mol | D. | 24mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯气与水反应:Cl2+H2O═2H++Cl-+ClO- | |
| B. | 氢氧化镁与稀硫酸反应H++OH=H2O | |
| C. | 过量的SO2通入NaOH溶液中:SO2+2OH-═SO32-+H2O | |
| D. | 大理石溶于醋酸中:CaCO3+2CH3COOH=Ca2++2CH3COO-+CO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③⑤ | B. | ①②③⑤ | C. | ①②④⑤ | D. | 全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有②③④ | B. | 只有②④ | C. | 只有①③④ | D. | 全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | VA | ⅥA | ⅤⅡA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ |
 ,元素②原子核内含有6个中子的原子可表示为137N.
,元素②原子核内含有6个中子的原子可表示为137N. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 阳离子 | Na+、Ba2+、NH4+ |
| 阴离子 | CH3COO-、Cl-、OH-、SO42- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com