
| A£® | p£ØBr2£©”Ü4.66”Į103Pa | B£® | 2.33”Į103Pa£¼p£ØBr2£©”Ü4.66”Į103Pa | ||
| C£® | £¼p£ØBr2£©£¾2.33”Į103Pa | D£® | 2.33”Į103Pa”Üp£ØBr2£©”Ü4.66”Į103Pa |
·ÖĪö »żŌö“óŅ»±¶Ź±£¬P£ØBr2£©½µĪŖŌĄ“µÄŅ»°ė£¬¼õŃ¹Ź¹Ę½ŗāĻņĘųĢåĢå»żŹżŌö“óµÄ·½ĻņŅĘ¶Æ£¬Ń¹ĒæÓÖŌö“ó£¬Čō·“Ó¦Īļ×ćĮæ£¬Ę½ŗā»Öø“µ½ŌÓŠµÄŃ¹Ē森
½ā“š ½ā£ŗĢå»żŌö“óŅ»±¶Ź±£¬P£ØBr2£©½µĪŖŌĄ“µÄŅ»°ė£¬¼“2.33”Į103Pa£¬¼õŃ¹Ź¹Ę½ŗāĻņĘųĢåĢå»żŹżŌö“óµÄ·½ĻņŅĘ¶Æ£¬Ņņ¶ų»į“óÓŚ2.33”Į103Pa£»Čō·“Ó¦Īļ×ćĮ棬æÉĘ½ŗā»Öø“µ½ŌÓŠµÄP£ØBr2£©£¬
¹ŹŃ”B£®
µćĘĄ ±¾Ģāæ¼²éĮĖ»ÆŃ§Ę½ŗāµÄ½ØĮ¢ŗĶÓ°Ļģ»ÆŃ§Ę½ŗāµÄŅņĖŲ·ÖĪöÅŠ¶Ļ£¬ÕĘĪÕ»ł“”ŹĒ½āĢā¹Ų¼ü£¬ĢāÄæÄѶČÖŠµČ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 £»YW2·Ö×ÓŠĪדĪŖÖ±ĻߊĪ£®
£»YW2·Ö×ÓŠĪדĪŖÖ±ĻߊĪ£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
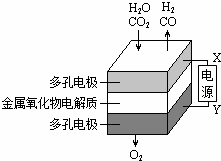 ŌŚ¹ĢĢ¬½šŹōŃõ»ÆĪļµē½ā³ŲÖŠ£¬øßĪĀ¹²µē½āH2O”«CO2»ģŗĻĘųĢåÖʱøH2ŗĶCOŹĒŅ»ÖÖŠĀµÄÄÜŌ“ĄūÓĆ·½Ź½£¬»ł±¾ŌĄķČēĶ¼ĖłŹ¾£®ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ£Ø””””£©
ŌŚ¹ĢĢ¬½šŹōŃõ»ÆĪļµē½ā³ŲÖŠ£¬øßĪĀ¹²µē½āH2O”«CO2»ģŗĻĘųĢåÖʱøH2ŗĶCOŹĒŅ»ÖÖŠĀµÄÄÜŌ“ĄūÓĆ·½Ź½£¬»ł±¾ŌĄķČēĶ¼ĖłŹ¾£®ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ£Ø””””£©| A£® | XŹĒµēŌ“µÄøŗ¼« | |
| B£® | Ņõ¼«µÄ·“Ó¦Ź½ŹĒ£ŗH2O+2e”„=H2+O2”„ | |
| C£® | ×Ü·“Ó¦æɱķŹ¾ĪŖ£ŗH2O+CO2=H2+CO+O2 | |
| D£® | Ņõ”¢ŃōĮ½¼«Éś³ÉµÄĘųĢåµÄĪļÖŹµÄĮæÖ®±ČŹĒ2£ŗ1 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | NaHSO4=Na++H++SO42- | B£® | Ba£ØOH£©2=Ba2++2OH- | ||
| C£® | CaCO3=Ca2++CO32- | D£® | KHCO3=K++H++CO32- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
 ČēĶ¼±ķŹ¾·“Ó¦X£Øg£©?4Y£Øg£©+Z£Øg£©”÷H£¼0£¬ŌŚÄ³ĪĀ¶ČŹ±XµÄÅضČĖꏱ¼ä±ä»ÆµÄĒśĻߣ¬ĻĀĮŠÓŠ¹ŲøĆ·“Ó¦µÄĆčŹöÕżČ·µÄŹĒ£Ø””””£©
ČēĶ¼±ķŹ¾·“Ó¦X£Øg£©?4Y£Øg£©+Z£Øg£©”÷H£¼0£¬ŌŚÄ³ĪĀ¶ČŹ±XµÄÅضČĖꏱ¼ä±ä»ÆµÄĒśĻߣ¬ĻĀĮŠÓŠ¹ŲøĆ·“Ó¦µÄĆčŹöÕżČ·µÄŹĒ£Ø””””£©| A£® | XµÄĘ½ŗā×Ŗ»ÆĀŹĪŖ85% | |
| B£® | µŚ6 min ŗ󣬷“Ó¦¾ĶÖÕÖ¹ĮĖ | |
| C£® | ČōÉżøßĪĀ¶Č£¬XµÄĘ½ŗā×Ŗ»ÆĀŹ½«“óÓŚ85% | |
| D£® | Čō½µµĶĪĀ¶Č£¬vÕż¼õŠ”£¬vÄęŌö“ó |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | MµÄµ„ÖŹæÉÓĆÓŚ“ÓīŃ”¢ļÆµČ½šŹōµÄĀČ»ÆĪļČÜŅŗÖŠÖĆ»»³öīŃ”¢ļÆµČµ„ÖŹ | |
| B£® | ÓÉX”¢Y”¢ZČżÖÖŌŖĖŲŠĪ³ÉµÄijÖÖ»ÆŗĻĪļµÄĖ®ČÜŅŗ£¬æÉÄܳŹ¼īŠŌ»ņĖįŠŌ | |
| C£® | ÓÉX”¢MÓėZŠĪ³ÉµÄ»ÆŗĻĪļX2Z2ŗĶM2Z2ÖŠĖłŗ¬µÄ»Æѧ¼üĄąŠĶĻąĶ¬ | |
| D£® | ŗ¬ÓŠWŃōĄė×ÓµÄijÖÖŃĪ£¬æÉÓĆ×÷¾»Ė®¼Į |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com