
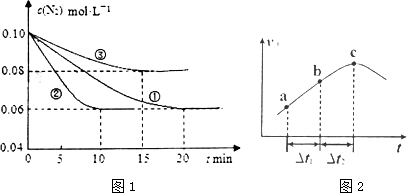
分析 (1)根据v=$\frac{△c}{△t}$计算反应速率,根据图象可知②到达平衡的时间比①短,到达平衡时N2的浓度与①相同,化学平衡不移动,故②与①相比加了催化剂,①和③比较可知,③的速率比①小,平衡时氮气的浓度高,即平衡逆向移动,故③减小了压强;
(2)①根据反应方程式,利用平衡常数的定义计算;
②根据温度对平衡常数的影响判断;
③向绝热密闭容器中通入一定量的NO2,根据图象可知,反应开始反应物浓度最大,但反应速率逐渐增大,据此判断;
(3)当a=b时,amol•L-1的氨水与b mol•L-1盐酸等体积混合,反应后溶液呈酸性,若溶液显中性,则酸的量要减少,故a>b,根据氨水的电离平衡常数的定义可计算电离平衡常数.
解答 解:(1)根据像可知,②在10min时达到平衡,此时氮气的浓度变化为0.04mol/L,根据方程式或知,氨气的浓度变化了0.08mol/L,根据v=$\frac{△c}{△t}$可知v(NH3)=$\frac{0.08mol/L}{10min}$=0.008mol•L-1•min-1,根据图象可知②到达平衡的时间比①短,到达平衡时N2的浓度与①相同,化学平衡不移动,故②与①相比加了催化剂,故选e,①和③比较可知,③的速率比①小,平衡时氮气的浓度高,即平衡逆向移动,故③升减小了压强,故选b,
故答案为:0.008mol•L-1•min-1;e;b;
(2)①2 NO2(g)?N2O4(g)
起始时 0.2mol•L-1 0
转化 0.1mol•L-1 0.05mol•L-1
平衡时 0.1mol•L-1 0.05mol•L-1
故平衡常数K=$\frac{c({N}_{2}{O}_{4})}{{c}^{2}(N{O}_{2})}$=$\frac{0.05}{0.{1}^{2}}$L•mol-1=5L•mol-1,
故答案为:5L•mol-1;
②温度升高,此平衡向逆反应方向移动,K值减小,
故答案为:减小;
③反应开始反应物浓度最大,但反应速率逐渐增大,说明反应为放热反应,
A.c点反应速率最大,但没有达到平衡状态,反应继续向正反应方向进行,c点时转化率不是最大,错误;
B.反应向正反应进行,随着反应的进行,反应物浓度逐渐降低,故错误;
C、随反应的进行,体系是的温度越来越高,反应速率逐渐增大,当时间相同时,转化率逐渐增大,正确,
故答案为:C;
(3)当a=b时,amol•L-1的氨水与b mol•L一1盐酸等体积混合,反应后溶液呈酸性,若溶液显中性,则酸的量要减少,故a>b.
反应后溶液显中性,溶液中c(OH-)=1×10-7mol/L,根据电荷守恒溶液中c(NH4+)=c(Cl-)=$\frac{b}{2}$mol/L,反应前c(NH3•H2O)=$\frac{a}{2}$mol/L,
则反应后一水合氨的浓度为:c(NH3•H2O)=(a/2-b/2)mol/L,所以氨水的电离平衡常数为:K=$\frac{c(N{{H}_{4}}^{+})c(O{H}^{-})}{c(N{H}_{3}•{H}_{2}O)}$═$\frac{b×1{0}^{-7}}{a-b}$mol/L;
故答案为:>;$\frac{{b×{{10}^{-7}}}}{a-b}mol•{L^{-1}}$.
点评 本题主要考查了物质的量或浓度随时间的变化曲线、化学平衡常数的含义、化学平衡的影响因素、化学反应速率的影响因素、酸碱混合时的定性判断及有关平衡常数的计算,中等难度,答题时注意电解质溶液基础知识的灵活运用.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
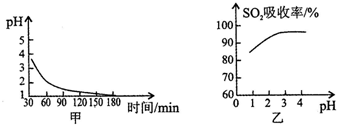 2SO2(g)+2O2(g)?2SO3(g)是生产硫酸的主要反应之一.下表是原料气按V(SO2):V(O2):V(N2)=7:11:82投料,在1.01×105Pa时,不同温度下SO2的平衡转化率.
2SO2(g)+2O2(g)?2SO3(g)是生产硫酸的主要反应之一.下表是原料气按V(SO2):V(O2):V(N2)=7:11:82投料,在1.01×105Pa时,不同温度下SO2的平衡转化率.| 温度/ | 400 | 500 | 600 |
| SO2转化率/% | 99.2 | 93.5 | 73.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2+H2O=H2CO3 | B. | CaCO3$\frac{\underline{\;高温\;}}{\;}$CO2↑+CaO | ||
| C. | CaCO3+2HCl=CaCl2+H2O+CO2↑ | D. | 2Na+Cl2$\frac{\underline{\;点燃\;}}{\;}$NaCl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(Na+)+c(H+)=c(OH-)+2c(S2-)+c(HS-) | B. | c(OH-)=c(HS-)+c(H+)+2c(H2S) | ||
| C. | c(Na+)=2c(S2-)+2c(HS-)+2c(H2S) | D. | c(OH-)=c(HS-)+c(H+)+c(H2S) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com