
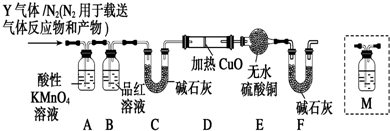
·ÖĪö £Ø1£©³£ĪĀĻĀ£¬ĢśŅ×ŗĶÅØĮņĖį·¢Éś¶Ū»ÆĻÖĻ󣬓Ӷų×čÖ¹½ųŅ»²½·“Ó¦£»
£Ø2£©¢Ł¶ž¼ŪĢśĄė×Ó¾ßÓŠĒæµÄ»¹ŌŠŌ£¬Äܹ»Ź¹ĖįŠŌµÄøßĆĢĖį¼ŲĶŹÉ«£¬¼ģŃéFe2+£¬æÉĄūÓĆ+2¼ŪŃĒĢśĄė×ÓÄÜŹ¹Ėį»ÆµÄøßĆĢĖį¼ŲĶŹÉ«Ą“¼ģŃ飻
¢ŚÉś³ÉµÄSO2¾ßÓŠ»¹ŌŠŌ£¬ĶØČė×ćĮæäåĖ®ÖŠ£¬·¢ÉśSO2+Br2+2H2O=2HBr+H2SO4£¬ĄūÓĆĮņŌŖĖŲµÄŹŲŗć£¬½įŗĻ¹ŲĻµŹ½£ŗSO2”«BaSO4Ēó³öSO2µÄĢå»ż·ÖŹż£»
£Ø3£©¶žŃõ»ÆĮņÄÜŹ¹Ę·ŗģČÜŅŗĶŹÉ«£¬“Ó¶ų¼ģŃ鶞Ńõ»ÆĮņŹĒ·ń³ż¾”£»
£Ø4£©¼ÓČČĢõ¼žĻĀ£¬CŗĶÅØĮņĖį·“Ӧɜ³É¶žŃõ»ÆĢ¼£»
£Ø5£©ŌŚČ·¶Ø²»“ęŌŚ¶žŃõ»ÆĮņĢõ¼žĻĀ£¬½«ĘųĢåĶØČė³ĪĒåŹÆ»ŅĖ®¼ģŃéŹĒ·ńŗ¬ÓŠ¶žŃõ»ÆĢ¼£»
£Ø6£©ĒāĘų¾ßÓŠ»¹ŌŠŌ£¬ÄÜ»¹ŌŠŌ£¬ÄÜ»¹ŌŗŚÉ«µÄŃõ»ÆĶÉś³ÉŗģÉ«µÄĶµ„ÖŹ£¬Ķ¬Ź±Éś³ÉĖ®£¬Ė®ÄÜŹ¹ĪŽĖ®ĮņĖįĶ±äĄ¶É«£®
½ā“š ½ā£ŗ£Ø1£©³£ĪĀĻĀ£¬FeŅ×ŗĶÅØĮņĖį·¢ÉśŃõ»Æ»¹Ō·“Ӧɜ³ÉÖĀĆܵÄŃõ»ÆĪļ±”Ĥ¶ų×čÖ¹½ųŅ»²½±»Ńõ»Æ£¬øĆĻÖĻóĪŖ¶Ū»ÆĻÖĻó£¬ĖłŅŌ·ÅČėÅØĮņĖįŗóµÄĢ¼ĖŲøÖ¼ÓČėĮņĖįĶČÜŅŗÖŠĪŽ±ä»Æ£¬ĖµĆ÷Fe±ķĆę·¢ÉśĮĖ¶Ū»Æ£¬Éś³ÉĮĖŅ»²ćŃõ»ÆĪļĤ£¬
¹Ź“š°øĪŖ£ŗFe±ķĆę·¢ÉśĮĖ¶Ū»Æ£¬Éś³ÉĮĖŅ»²ćŃõ»ÆĪļĤ£»
£Ø2£©¢ŁŃĒĢśĄė×ÓÄÜŹ¹ĖįŠŌøßĆĢĖį¼ŲĶŹÉ«£¬ČÜŅŗÖŠŅŃ¾ÓŠČż¼ŪĢśĄė×Ó£¬Ń”Ōńa»įŌģ³ÉøÉČÅ£¬bÄܼģŃéČż¼ŪĢśĄė×ӵēęŌŚ£¬Ń”cÉś³ÉĮ½ÖÖ³Įµķ£¬ŹÜĒāŃõ»ÆĢś³ĮµķŃÕÉ«µÄÓ°ĻģĪŽ·Ø·Ö±ę£¬
¹ŹŃ”£ŗd£»
¢ŚSO2¾ßÓŠ»¹ŌŠŌ£¬ĶØČė×ćĮæäåĖ®ÖŠ£¬·¢Éś·“Ó¦£ŗSO2+Br2+2H2O=2HBr+H2SO4£¬n£ØĘųĢåY£©=$\frac{0.336L}{22.4L/mol}$=0.015mol
SO2 ”«BaSO4
1mol 233g
n 2.33g
½āµĆ£ŗn=0.01mol£¬ŌņSO2µÄĢå»ż·ÖŹż£ŗ$\frac{0.01}{0.015}$”Į100%=66.7%£»
¹Ź“š°øĪŖ£ŗ66.7%£»
£Ø3£©A³żČ„¶žŃõ»ÆĮņ£¬¶žŃõ»ÆĮņÄÜŹ¹Ę·ŗģČÜŅŗĶŹÉ«£¬ĖłŅŌBæÉŅŌ¼ģŃéAÖŠŹĒ·ńĶźČ«³żČ„¶žŃõ»ÆĮņ£»
¹Ź“š°øĪŖ£ŗ¼ģŃéSO2ŹĒ·ń³ż¾”£»
£Ø4£©¼ÓČČĢõ¼žĻĀ£¬CŗĶÅØĮņĖį·“Ӧɜ³É¶žŃõ»ÆĢ¼£¬ĖłŅŌQŹĒ¶žŃõ»ÆĢ¼£¬·“Ó¦·½³ĢŹ½ĪŖ£ŗC+2H2SO4£ØÅØ£©$\frac{\underline{\;\;”÷\;\;}}{\;}$2SO2”ü+CO2”ü+2H2O£»
¹Ź“š°øĪŖ£ŗC+2H2SO4£ØÅØ£©$\frac{\underline{\;\;”÷\;\;}}{\;}$2SO2”ü+CO2”ü+2H2O£»
£Ø5£©ŹµŃéŹŅÓĆ³ĪĒåŹÆ»ŅĖ®¼ģŃ鶞Ńõ»ÆĢ¼£¬µ«¶žŃõ»ÆĮņŅ²ÄÜŹ¹³ĪĒåŹÆ»ŅĖ®±ä»ė×Ē£¬ŅŖ¼ģŃ鶞Ńõ»ÆĢ¼Ó¦øĆÅųż¶žŃõ»ÆĮņµÄøÉČÅ£¬ĖłŅŌŌŚČ·¶Ø²»“ęŌŚ¶žŃõ»ÆĮņĢõ¼žĻĀ£¬½«ĘųĢåĶØČė³ĪĒåŹÆ»ŅĖ®¼ģŃéŹĒ·ńŗ¬ÓŠ¶žŃõ»ÆĢ¼£¬øĆ¼ģŃé×°ÖĆÓ¦øĆŌŚB-CÖ®¼ä£¬
¹ŹŃ”£ŗc£»
£Ø6£©ĒāĘų¾ßÓŠ»¹ŌŠŌ£¬ÄÜ»¹ŌŠŌ£¬ÄÜ»¹ŌŗŚÉ«µÄŃõ»ÆĶÉś³ÉŗģÉ«µÄĶµ„ÖŹ£¬Ķ¬Ź±Éś³ÉĖ®£¬Ė®ÄÜŹ¹ĪŽĖ®ĮņĖįĶ±äĄ¶É«£¬ÕāŹĒ¼ģŃéĖ®µÄĢŲÕ÷·“Ó¦£¬ĖłŅŌČē¹ūDÖŠŃõ»ÆĶ±äŗģ£¬EÖŠĪŽĖ®ĮņĖįĶ±äĄ¶£¬ŌņÖ¤Ć÷ŗ¬ÓŠĒāĘų£¬
¹Ź“š°øĪŖ£ŗDÖŠŗŚÉ«·ŪÄ©±äŗģ£¬EÖŠ°×É«·ŪÄ©±äĄ¶£»
µćĘĄ ±¾Ģā×ŪŗĻæ¼²éŌŖĖŲ»ÆŗĻĪļÖŖŹ¶£¬ŠŌÖŹŹµŃé·½°øÉč¼Ę£¬ŹģĻ¤Ļą¹ŲĪļÖŹµÄŠŌÖŹŹĒ½āĢā¹Ų¼ü£¬×¢Ņā¶ž¼ŪĢśĄė×Ó”¢Čż¼ŪĢśĄė×ӵļģŃé·½·Ø£¬ĢāÄæÄѶČÖŠµČ


 ʷѧĖ«ÓžķĻµĮŠ“š°ø
ʷѧĖ«ÓžķĻµĮŠ“š°ø Š”ѧʌĩ³å“Ģ100·ÖĻµĮŠ“š°ø
Š”ѧʌĩ³å“Ģ100·ÖĻµĮŠ“š°ø ĘŚÄ©ø“Ļ°¼ģ²āĻµĮŠ“š°ø
ĘŚÄ©ø“Ļ°¼ģ²āĻµĮŠ“š°ø ³¬ÄÜѧµäµ„ŌŖĘŚÖŠĘŚÄ©×ØĢā³å“Ģ100·ÖĻµĮŠ“š°ø
³¬ÄÜѧµäµ„ŌŖĘŚÖŠĘŚÄ©×ØĢā³å“Ģ100·ÖĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÓĆĶŠÅĢĢģĘ½³ĘČ”150kgµÄŹ³ŃĪ | B£® | ÓĆpHŹŌÖ½²āµĆijČÜŅŗµÄpHĪŖ6.72 | ||
| C£® | ÓĆĘÕĶØĪĀ¶Č¼Ę²āµĆŹŅĪĀĪŖ34.68”ę | D£® | ÓĆ10mLĮæĶ²ĮæČ”7.5mLĖ® |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| X | ||
| Y | Z | W |
| T |
| A£® | X”¢W”¢Z ŌŖĖŲµÄĘųĢ¬Ēā»ÆĪļµÄČČĪČ¶ØŠŌ¾łŅĄ“ĪµŻ¼õ | |
| B£® | Y”¢Z”¢W ŌŖĖŲŌŚ×ŌČ»½ēÖŠ¾ł²»ÄÜŅŌÓĪĄėĢ¬“ęŌŚ£¬ĖüĆĒµÄ×īøß¼ŪŃõ»ÆĪļµÄĖ®»ÆĪļµÄĖįŠŌŅĄ“ĪµŻŌö | |
| C£® | ŅŗĢ¬WX3 Ęų»Æ¾łŠčæĖ·ž·Ö×Ó¼ä×÷ÓĆĮ¦ | |
| D£® | øł¾ŻŌŖĖŲÖÜĘŚĀÉ£¬æÉŅŌĶĘ²āT ŌŖĖŲµÄµ„ÖŹ¾ßÓŠ°ėµ¼ĢåµÄĢŲŠŌ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
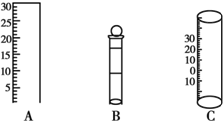 ČēĶ¼ĖłŹ¾ĪŖ֊ѧ»ÆѧŹµŃéÖŠ¼øÖÖ³£¼ūŅĒĘ÷µÄ²æ·Ö½į¹¹£ŗ
ČēĶ¼ĖłŹ¾ĪŖ֊ѧ»ÆѧŹµŃéÖŠ¼øÖÖ³£¼ūŅĒĘ÷µÄ²æ·Ö½į¹¹£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŅŗĢ¬HCl”¢¹ĢĢ¬NaCl¾ł²»µ¼µē£¬ĖłŅŌHCl”¢NaCl¾ł²»ŹĒµē½āÖŹ | |
| B£® | ŻĶČ”²Ł×÷Ź±£¬æÉŅŌŃ”ÓĆCCl4»ņ¾Ę¾«×÷ĪŖŻĶČ”¼Į“ÓäåĖ®ÖŠŻĶČ”äå | |
| C£® | ĒāŃõ»ÆĢś½ŗĢåµÄµēÓ¾ŹµŃéÄÜÖ¤Ć÷ĒāŃõ»ÆĢś½ŗĢå“ųÕżµē | |
| D£® | ŌŚĢå»żĻąĶ¬µÄĮ½øöĆܱÕČŻĘ÷ÖŠ·Ö±š³äĀśO2ŗĶO3ĘųĢ壬µ±ÕāĮ½øöČŻĘ÷ÄŚĪĀ¶ČŗĶĘųĢåĆܶČĻąµČŹ±£¬Į½ÖÖĘųĢåµÄŃõŌ×ÓŹżÄæĻąµČ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | æÉŅŌÓĆĪŽĖ®CuSO4¼ģŃé¾Ę¾«ÖŠŹĒ·ńŗ¬Ė® | |
| B£® | ĆŗµÄøÉĮó¹ż³ĢŹĒø“ŌÓµÄĪļĄķŗĶ»Æѧ¹ż³Ģ | |
| C£® | ±ź×¼×“æöĻĀ£¬22.4L¶žĀČ¼×ĶéµÄ·Ö×ÓŹżŌ¼ĪŖNAøö | |
| D£® | ÓĆ½žÅŻ¹żøßĆĢĖį¼ŲČÜŅŗµÄ¹čĶĮĪüŹÕĖ®¹ūŹĶ·ÅµÄŅŅĻ©£¬æÉ“ļµ½Ė®¹ū±£ĻŹµÄÄæµÄ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com