
分析 甲同学有pH试纸,可以通过测定溶液的pH大小判断HA属于弱酸;乙:将1ml pH=1的HA溶液,加水稀释为100mL,体积扩大100倍,如果是弱电解质,溶液的PH增加不到两个单位,所以pH小于3;丙:用蒸馏水配制少量NaA溶液,测其pH大于7,说明水解呈碱性,是强碱弱酸盐,由此分析解答.
解答 解:甲:称取一定量的HA配制0.1mol/L的溶液100mL,用pH试纸测定0.1mol/L的HA溶液,若是pH=1,说明HA为强酸;若溶液的pH大于1,说明HA部分电离出氢离子,属于弱酸;
乙:将1ml pH=1的HA溶液,加水稀释为100mL,体积扩大100倍,如果是弱电解质,溶液的PH增加不到两个单位,所以pH小于3;
丙:用蒸馏水配制少量NaA溶液,测其pH大于7,说明水解呈碱性,是强碱弱酸盐,酸根对应的酸是弱酸,
故答案为:大于1;小于3;大于7.
点评 本题考查了弱电解质的判断,注意电解质的强弱是根据其电离程度划分的,丙溶液呈碱性说明盐是强碱弱酸盐,为易错点.


科目:高中化学 来源: 题型:选择题
| A. | 氢氧化钡溶液与硫酸的反应 OH-+H+═H2O | |
| B. | 澄清的石灰水与稀盐酸反应 Ca(OH)2+2H+═Ca2++2H2O | |
| C. | 铜片插入硝酸银溶液中 Cu+Ag+═Cu2++Ag | |
| D. | 碳酸钙溶于稀盐酸中 CaCO3+2H+═Ca2++H2O+CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 编号 | Na2SO4溶液 | AgNO3溶液 | 现象 | ||
| 体积/mL | 浓度/(mol•L-1) | 体积 | 浓度/(mol•L-1) | ||
| ① | 1 | 1 | 3滴 | 2 | 出现大量白色沉淀 |
| ② | 1 | 1 | 3滴 | 0.5 | 出现少量白色沉淀 |
| ③ | 1 | 1 | 3滴 | 0.1 | 有些许浑浊 |
| ④ | 1 | 1 | 3滴 | 0.01 | 无明显变化 |
| 编号 | AgNO3浓度/(mol•L-) | 稀释后Ag+浓度/(mol•L-1) | 混合溶液中SO42-的最小理论检出浓度/(mol•L-1) |
| ① | 2 | 0.2 | 0.0003 |
| ② | 0.5 | 0.0048 | |
| ③ | 0.1 | 0.01 | 0.12 |
| ④ | 0.01 | 0.001 |
| 编号 | AgNO3浓度/(mol•L-1) | 现象 | 向沉淀中滴加硝酸后的现象 |
| ① | 2 | 出现大量白色沉淀 | 滴加稀硝酸,沉淀大量溶解;改加浓硝酸,沉淀较快消失 |
| ② | 0.5 | 出现少量白色沉淀 | 滴加稀硝酸,沉淀基本消失 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Mg2+、Fe3+、Cl-、OH- | B. | Ba2+、HCO3-、Cl-、Na+ | ||
| C. | Fe2+、SO42-、H+、NO3- | D. | K+、NH4+、SO42-、OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 给定条件下,Mg(OH)2$\stackrel{盐酸}{→}$MgCl2(aq)$\stackrel{电解}{→}$Mg,物质间转化能一步实现 | |
| B. | 工业上,常用电解熔融AlCl3的方法冶炼金属铝 | |
| C. | 火法炼铜:Cu2S+O2$\frac{\underline{\;高温\;}}{\;}$2Cu+SO2,其中Cu2S既作氧化剂又作还原剂 | |
| D. | 铝热法炼铁:2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3,反应物刚好完全反应,反应后固体质量增加 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
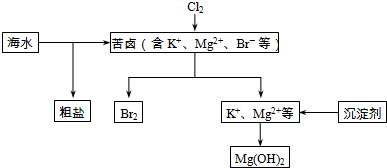
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al2O3是两性氧化物,既能与所有的酸反应,也能与所有的碱反应 | |
| B. | 铝制容器可盛装热的浓H2SO4 | |
| C. | 明矾[KAl(SO4)2•12H2O]的水溶液能够杀菌消毒,可用做净水剂 | |
| D. | 向AlCl3溶液中加入过量氨水后,蒸干并灼烧可得到Al2O3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由苯制环己环 由氯乙烯制备聚氯乙烯 | |
| B. | 乙烯使酸性高锰酸钾褪色 乙醇制乙醛 | |
| C. | 苯和液溴在铁粉催化下反应 乙炔使溴水褪色 | |
| D. | 乙醇与浓硫酸共热制乙烯 乙醇与浓硫酸共热制乙醚 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com