


科目:高中化学 来源: 题型:
| A、用稀硝酸洗涤试管内壁的银镜:Ag+4H++3NO3-=Ag++NO↑+2H2O |
| B、用小苏打治疗胃酸过多:CO32-+2H+=CO2↑+H2O |
| C、用KIO3氧化酸性溶液中的KI:5I-+IO3-+3H2O=3I2+6OH- |
| D、用碳酸钠溶液浸泡锅炉水垢:CaSO4+CO32-=CaCO3+SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 操作及现象 | 结论 |
| A | 通入CO2,溶液变浑浊,继续通入无明显变化 | 可能为Na2SiO3溶液 |
| B | 通入CO2,溶液变浑浊,继续通CO2至过量,浑浊消失 | 一定为氢氧化钙溶液 |
| C | 通入CO2,溶液变浑浊,继续通入沉淀消失,再加入品红溶液,红色褪去. | 可能Ca(ClO)2溶液 |
| D | 通入足量CO2,溶液变浑浊,加热至沸腾后有气泡产生,浑浊消失 | 可能是苯酚钠溶液 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素代号 | X | Y | Z | W |
| 原子半径/pm | 160 | 143 | 70 | 66 |
| 主要化合价 | +2 | +3 | +5、+3、-3 | -2 |
| A、X离子的氧化性比Y离子氧化性弱 |
| B、一定条件下,Z单质与W的常见单质直接生成ZW2 |
| C、Y的最高价氧化物对应的水化物能溶于稀氨水 |
| D、一定条件下,W单质可以将Z单质从其氢化物中置换出来 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
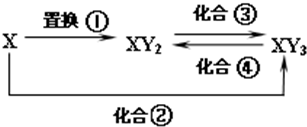 元素X的单质、Y单质及X与Y形成的化合物能按如下图所示的关系发生转化,图中化合反应均为与X或Y单质的反应,且Y单质为气体,
元素X的单质、Y单质及X与Y形成的化合物能按如下图所示的关系发生转化,图中化合反应均为与X或Y单质的反应,且Y单质为气体,查看答案和解析>>
科目:高中化学 来源: 题型:
| A、再充入2mol A,平衡正移,A的转化率增大 |
| B、如果升高温度,C的体积分数增大 |
| C、如果增大压强,化学平衡一定向正反应方向移动,B的体积分数减小 |
| D、再充入1mol C,C的物质的量浓度将增大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com