
【题目】焦亚硫酸钠(Na2S2O5)是常用的脱氧剂,其制备方法是向Na2CO3溶液中通入SO2,生成NaHSO3和CO2,一定条件下NaHSO3转化为Na2S2O5。完成下列填空:
(1)碳原子的原子结构示意图是_____________;CO2中所含共价键的类型_____________。
(2)从原子结构的角度,解释氧元素的非金属性比硫元素强的原因。_______________。
(3)SO2 与Na2CO3溶液反应生成NaHSO3和CO2,其化学方程式为_______________________,证明NaHSO3溶液中HSO3-的电离程度大于水解程度,可采用的实验方法是_________________。
(4)Na2S2O5作脱氧剂时的反应原理为Na2S2O5+O2+ H2O→Na2SO4+H2SO4,该反应中,氧化产物是______;若反应中转移了0.04mol的电子,有________g Na2S2O5参加反应。
(5)连二亚硫酸钠Na2S2O4俗称保险粉,广泛用于纺织工业的还原性染色、清洗、印花、脱色以及织物的漂白等。Na2S2O4属于强还原剂,暴露于空气中易被氧气氧化。Na2S2O4遇KMnO4酸性溶液发生反应:5Na2S2O4+6KMnO4+4H2SO4=5Na2SO4+3K2SO4+6MnSO4+4H2O。
为了测定保险粉纯度。称取5.0g Na2S2O4样品溶于冷水中,配成100mL溶液,取出10mL 该溶液于锥形瓶中,用0.1000mol/L的KMnO4 溶液滴定。重复上述操作2 次,平均消耗KMnO4 溶液21.00mL。则该样品中Na2S2O4的质量分数为__________(杂质不参与反应)。(保留至0.1%)
(6)“钢是虎,钒是翼,钢含钒犹如虎添翼”,钒是“现代工业的味精”。钒对稀酸是稳定的,但室温下能溶解于浓硝酸中生成VO2+。请写出金属钒与浓硝酸反应的离子方程式:_______________________________________。
(7)V2O5是两性氧化物,与强碱反应生成钒酸盐(阴离子为VO43-),溶于强酸生成含钒氧离子(VO2+)的盐。请写出V2O5分别与烧碱溶液和稀硫酸反应生成的盐的化学式:__________、_________。
【答案】![]() 极性共价键 氧原子的半径比硫原子小,吸引力电子能力强 2SO2+Na2CO3+H2O=2NaHSO3+CO2 取样,测定溶液的pH,若pH小于7,说明电离程度大于水解程度 Na2SO4、H2SO4 1.90 60.9% V+6H++5NO3-===VO2++5NO2 ↑+3H2O Na3VO4 (VO2)2SO4
极性共价键 氧原子的半径比硫原子小,吸引力电子能力强 2SO2+Na2CO3+H2O=2NaHSO3+CO2 取样,测定溶液的pH,若pH小于7,说明电离程度大于水解程度 Na2SO4、H2SO4 1.90 60.9% V+6H++5NO3-===VO2++5NO2 ↑+3H2O Na3VO4 (VO2)2SO4
【解析】
(1)碳原子核电荷数为6,核外两个电子层,最外层4个电子,二氧化碳为共价化合物,碳氧键为极性共价键;
(2)O和S位于同一主族,从上到下原子半径增大,原子半径越小,元素的非金属性越强;
(3)SO2与Na2CO3溶液反应生成NaHSO3和CO2,亚硫酸氢根离子水解呈碱性,电离呈酸性,可以测定溶液酸碱性;
(4)Na2S2O5作脱氧剂反应原理为:Na2S2O5+O2+H2O→Na2SO4+H2SO4,该反应中,氧化产物是元素化合价升高做还原剂的物质,硫元素化合价+4升高为+6价,电子转移4e-,氧气中氧元素化合价0价变化为-2价,电子转移4e-,电子转移总数4e-,Na2S2O5+O2+H2O=Na2SO4+H2SO4,以此计算;
(5)根据5S2O42-~6MnO4-,计算样品中Na2S2O4的质量,再计算样品中Na2S2O4的质量分数。
(6)金属钒与浓硝酸反应成VO2+,二氧化氮和水,写出离子反应方程式;
(7)V2O5是两性氧化物,与强碱反应生成钒酸盐(阴离子为VO43-),溶于强酸生成含钒氧离子(VO2+)的盐,所以V2O5分别与烧碱溶液生成盐的金属阳离子是钠离子、酸根离子为VO43-,得盐的化学式,溶于稀硫酸生成含钒氧离子(VO2+)的盐,阳离子是VO2+,酸根是硫酸根,所以盐的化学式为:(VO2)2SO4;
(1)碳原子核电荷数为6,核外两个电子层,最外层4个电子,原子结构示意图为:![]() ,
,
二氧化碳为共价化合物,含有C=O键,为极性共价键;
(2)O和S位于同一主族,同主族元素从上到下原子半径增大,原子核对核外电子的吸引能力减小,原子半径越小,元素的非金属性越强;
(3)SO2与Na2CO3溶液反应生成NaHSO3和CO2,化学方程式为:2SO2+Na2CO3+H2O=2NaHSO3+CO2,亚硫酸氢根离子水解呈碱性,电离呈酸性,取样,测定溶液的pH,若pH小于7,说明电离程度大于水解程度。
(4)Na2S2O5作脱氧剂反应原理为Na2S2O5+O2+H2O→Na2SO4+H2SO4,该反应中,硫元素化合价+4升高为+6价,电子转移4e-,升高失电子发生氧化反应,得到氧化产物为:Na2SO4、H2SO4,氧气中氧元素化合价0价变化为-2价,电子转移4e-,电子转移总数4e-,Na2S2O5+O2+H2O=Na2SO4+H2SO4,若反应中转移了4mol的电子,有1molNa2S2O5参加反应,若反应中转移了0.04mol的电子,Na2S2O5参加反应的质量=0.01mol×190g·mol-1=1.90g。
(5)Na2S2O4与KMnO4反应产物为Na2SO4和MnSO4,硫元素共升高6价,锰元素共降低5价,化合价升降相同,故关系为
5S2O42-~6MnO4-,
5 6
n 21×10-3 L×0.1mol·L-1
则3.0g 样品中Na2S2O4的质量分数为=![]()
![]() ;
;
(6)金属钒与浓硝酸反应成VO2+,二氧化氮和水,离子方程式为:V+6H++5NO3-=VO2++5NO2↑+3H2O;
(7)V2O5是两性氧化物,与强碱反应生成钒酸盐(阴离子为VO43-),溶于强酸生成含钒氧离子(VO2+)的盐,V2O5分别与烧碱溶液生成盐的阳离子是钠离子、酸根离子为VO43-,所以盐的化学式为Na3VO4,溶于稀硫酸生成含钒氧离子(VO2+)的盐,所以阳离子是VO2+,酸根是硫酸根,所以盐的化学式为:(VO2)2SO4;V2O5是两性氧化物,与强碱反应生成钒酸盐(阴离子为VO43-)。


科目:高中化学 来源: 题型:
【题目】下列指定反应的离子方程式正确的是
A. 澄清石灰水中通入过量二氧化碳:OH-+CO2=HCO3-
B. 酸化NaIO3和NaI的混合溶液:I +IO3+6H+![]() I2+3H2O
I2+3H2O
C. 漂白粉溶液吸收少量二氧化硫气体:SO2+H2O+ClO- = SO42-+Cl-+2H+
D. 下图所示装置中反应:Zn+Cu2+= Cu + Zn2+
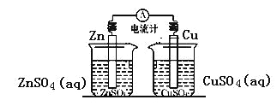
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】表中a、b、c表示相应仪器中加入的试剂,可用如图所示装置制取、净化、收集的气体是 ( )
编号 | 气体 | a | b | c |
A | NH3 | 浓氨水 | 生石灰 | 碱石灰 |
B | SO2 | 70%浓H2SO4 | Na2SO3固体 | 98%浓H2SO4 |
C | NO | 稀HNO3 | 铜屑 | H2O |
D | NO2 | 浓HNO3 | 铜屑 | NaOH溶液 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列分类正确的是( )
A.酸:CH3COOH、H2SO3、NaHCO3、HF
B.碱:Cu2(OH)2CO3、NaOH、Fe(OH)2、Mg(OH)2
C.盐:AgCl、BaSO4、NaH2PO4、Mg(NO3)2
D.氧化物:FeO、N2O5、COCl2、SiO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X、Y和Z三种元素的原子序数之和等于42。X元素原子的4p轨道上有3个未成对电子,Y元素原子的最外层2p轨道上有2个未成对电子。X跟Y可形成化合物X2Y3,Z元素可以形成负一价离子,下列说法正确的是 ( )
A. X元素原子基态时的电子排布式为[Ar]4s24p3
B. X元素是第四周期第ⅤA族元素
C. Y元素原子的电子排布图为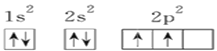
D. Z元素具有两性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2A+B![]() 3C+4D反应中,表示该反应速率最快的是()
3C+4D反应中,表示该反应速率最快的是()
A.v(A)=0.5 mol/(L·min) B.v(B)=0.3 mol/(L·min)
C.v(C)=0.8 mol/(L·min) D.v(D)=1 mol/(L·min)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按如图所示装置进行实验,将液体A逐滴加入到固体B中,下列叙述不正确的是
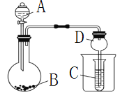
A. 若A为浓硫酸,B为K2SO3,C中盛品红溶液,则C中溶液褪色
B. 若A为浓氨水,B为生石灰,C中盛AlCl3溶液,则C中先变浑浊后澄清
C. 若A为醋酸,B为CaCO3,C中盛Na2SiO3溶液,则C中溶液中变浑浊
D. 若A为双氧水,B为MnO2,C中盛Na2S溶液,则C中溶液中变浑浊
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关如图装置的叙述不正确的是 ( )
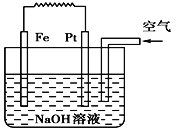
A. 这是电解NaOH溶液的装置
B. 该装置中Pt为正极,电极反应为O2+2H2O+4e- = 4OH-
C. 该装置中Fe为负极,电极反应为Fe+2OH-- 2e- = Fe(OH)2
D. 这是一个原电池装置
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com