
| A.28g以任意比组成的CO与N2混合气体中含有2NA 个原子 |
| B.22.4L H2的分子数为NA |
| C.1mol FeCl3充分反应,生成的Fe(OH)3胶体中胶粒数目为NA 个 |
| D.1L 1mol/L 的盐酸溶液中有NA个HCl分子 |
 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案科目:高中化学 来源:不详 题型:单选题
| A.物质的摩尔质量等于其相对分子(原子)质量 |
| B.“物质的量”是国际单位制中的一个基本单位 |
| C.0.012kg 12C 中所含的碳原子数为NA |
| D.1mol任何物质都含有约6.02×1023个原子 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

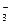 还原为N2,从而消除污染。
还原为N2,从而消除污染。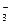 ,则至少需要含0.5%(质量分数)MgCl2的海水 kg。
,则至少需要含0.5%(质量分数)MgCl2的海水 kg。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.100mL 0.5mol/L MgCl2溶液 | B.200mL 0.25mol/L CaCl2溶液 |
| C.50mL 1mol/L NaCl溶液 | D.25mL 0.6mol/L HCl溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.标准状况下,5.6L四氯化碳含有的分子数为0.25NA |
| B.2.4g金属镁变为镁离子时失去的电子数为0.2NA |
| C.H2SO4的摩尔质量是98 g/mol |
D.物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl- 个数为1 NA 个数为1 NA |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.等pH值的氨水、KOH溶液、Ba(OH)2溶液中: c(NH4+)=c(K+)=2c(Ba2+) |
B.0.1 mol/L 的CH3COONa溶液中: c(CH3COO-) > c(Na+) >c(OH-) >c(H+) c(CH3COO-) > c(Na+) >c(OH-) >c(H+) |
| C.常温时向NH4HSO4溶液中滴加NaOH溶液至pH=7:c(NH4+)+c(Na+)= c(SO42-) |
D.将10 m L 0.1 mol/L Na2CO3溶液逐滴滴加到10 mL 0.1 mol/L盐酸中: L 0.1 mol/L Na2CO3溶液逐滴滴加到10 mL 0.1 mol/L盐酸中: |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.1mol/L的NaCl溶液是指此溶液中含有1mol NaCl |
| B.从1 L 0.5 mol/L,的NaCl溶液中取出100 mL溶液,其物质的量浓度变为0.05 mol/L, |
| C.25℃、1atm时,1molCl2的体积约为22.4L |
| D.50ml、l mol/L的CaCl2溶液和100ml、2 mol/L的NaCl溶液中的Cl-的物质的量浓度相同. |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com