
下列对物质的量理解正确的是()
A. 物质的量就是物质的质量
B. 物质的量是一种基本物理量
C. 物质的量就是物质的摩尔质量
D. 物质的量就是物质所含粒子的数量
考点: 物质的量的单位--摩尔;摩尔质量.
专题: 阿伏加德罗常数和阿伏加德罗定律.
分析: A.物质的量表示的为微观粒子的集体,单位为mol,而物质的质量单位为g;
B.物质的量为国际单位制中七个基本物理量之一;
C.物质的量的单位为mol,摩尔质量的单位为g/mol;
D.物质的量单位为mol,物质所含粒子数量的单位为个.
解答: 解:A.物质的量与物质的质量为两个不同的物理量,物质的量单位为mol,质量的单位为g,故A错误;
B.物质的量是国际单位制中的基本物理量,符号为n,单位为mol,故B正确;
C.物质的量的单位为mol,而摩尔质量的单位为g/mol,二者的单位不同,故C错误;
D.物质的量表示物质所含指定粒子的多少,物质的量是一个整体,不是物质所含粒子的数量,故D错误;
故选B.
点评: 本题考查了物质的量与物质的量质量、摩尔质量、粒子数之间的关系,题目难度不大,注意掌握物质的量的概念,明确物质的量与其它物理量之间的区别.


科目:高中化学 来源: 题型:
现有CH4、C2H2、C2H4、C2H6、C4H10五种有机物,质量相同时,完全燃烧消耗O2的物质的量的顺序为( )
|
| A. | CH4>C2H2>C4H10>C2H4>C2H6 | B. | CH4>C2H6>C4H10>C2H4>C2H2 |
|
| C. | C4H10>C2H6>C2H4>C2H2>CH4 | D. | C4H10>C2H6>CH4>C2H4>C2H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C三种强电解质,它们在水中电离出的离子如下表所示:
| 阳离子 | Ag+ Na+ |
| 阴离子 | NO3- SO42- Cl- |
下图所示装置中,甲、乙、丙三个烧杯依次分别盛放足量的A、B、C三种溶液,电极均为石墨电极。

接通电源,经过一端时间后,测得乙中c电极质量增加了27克。常温下各烧杯中溶液的pH与电解时间t的关系图如上。据此回答下列问题:
(1)M为电源的 极(填写“正”或“负”),甲、乙电解质分别为 、 (填写化学式)。
(2)要使电解后丙中溶液恢复到原来的状态,应加入 物质。(填写化学式)
(3) 若电解后甲溶液的体积为25L,且产生的气体全部逸出。该溶液常温时的pH为 。
(4)写出乙烧杯中发生反应的离子方程式
(5)写出甲烧杯中发生反应的离子方程式
查看答案和解析>>
科目:高中化学 来源: 题型:
稀土元素又称“二十一世纪黄金”,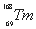 、
、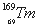 和
和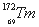 属于稀土元素,铥(Tm)可用来指导不需要电源的手提式X射线机。下列说法不正确的是
属于稀土元素,铥(Tm)可用来指导不需要电源的手提式X射线机。下列说法不正确的是
A.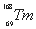 和
和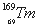 互为同位素 B.
互为同位素 B.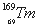 和
和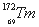 是不同的核素
是不同的核素
C.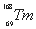 和
和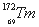 的中子数相差4 D.
的中子数相差4 D.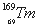 和
和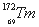 的电子数相差3
的电子数相差3
查看答案和解析>>
科目:高中化学 来源: 题型:
金属钛性能优越,被誉为继Fe、Al后应用广泛的“第三金属”。
(1)Ti基态原子的电子排布式为
(2)钛能与B、C、 N、 O等非金属元素形成稳定的化合物。电负性:C (填“>”或“<”下同)B;第一电离能: N O。
(3)月球岩石——玄武岩的主要成分为钛酸亚铁(FeTiO3) 。 FeTiO3与80%的硫酸反应可 生成TiOSO4。SO42-的空间构型为 形,其中硫原子采用 杂化.
(4)磷酸钛〔Ti3 (PO4 )4]锂离子电池能量密度大、安全性高。Ti3 (PO4 )4可由TiOSO4与
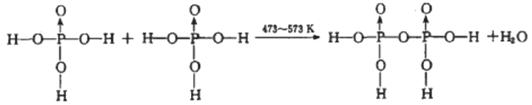 H3PO4反应制得。两分子H3PO4发生脱水生成焦磷酸;
H3PO4反应制得。两分子H3PO4发生脱水生成焦磷酸;
则三分子H3PO4脱去两分子H2O生成三磷酸,其结构式为 ,四分子H3PO4 脱去四分子H2O生成的四偏磷酸属于 元酸。
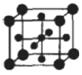
(5)Ti的氧化物和CaO相互作用能形成钛酸盐CaTiO3,CaTiO3的晶体结构如图所示(Ti4+位于立方体的顶点)。该晶体中,Ti4+和周围 个O2-相紧邻.
(6)Fe能形成多种氧化物,其中FeO晶胞结构为NaCI型。晶体中实际上存在空位、错位、杂质原子等缺陷,晶体缺陷对晶体的性质会产生重大影响。由于晶体缺陷,在晶体中Fe和O的个数比发生了变化,变为FexO(x<1)中,若测得某FexO晶体密度为5.71 g·cm-3,晶胞边长为4.28X10-10 m,则FexO中x=_。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各溶液中,Na+物质的量浓度最大的是()
A. 2L 0.5mol/L NaCl溶液 B. 3L 0.3mol/L Na2SO4溶液
C. 1L 0.4mol/L Na2CO3溶液 D. 4L 0.15mol/L Na3PO4溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应中铁元素被还原的是()
A. 2Fe(OH)3 Fe2O3+3H2O B. Fe+CuSO4=Cu+FeSO4
Fe2O3+3H2O B. Fe+CuSO4=Cu+FeSO4
C. Fe(OH)3+3HCl=FeCl3+3H2O D. 2Fe2O3+3C 4Fe+3CO2↑
4Fe+3CO2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应方程式正确的是()
A. 2Na+CuSO4═Cu+Na2SO4 B. 4Na+O2 2Na2O
2Na2O
C. 2KNO3+CuCl2═Cu(NO3)2+2KCl D. Cu+2AgNO3═Cu(NO3)2+2Ag
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com