
【题目】下列说法正确的是()
A.向 AgCl 、 AgBr 的饱和溶液中滴加少量 AgNO3 溶液,溶液中![]() 不变
不变
B.向0.1mol L1 的CH3COOH 溶液中加入少量水,溶液中![]() 减小
减小
C.0.1mol K2Cr2O7 被完全还原为Cr3 时,转移的电子数约为1.806 1023
D.一定条件下,反应 2NO(g) 2CO(g) N 2(g) 2CO 2(g) 能自发进行,该反应的ΔH>0
科目:高中化学 来源: 题型:
【题目】研究小组进行右图所示实验,试剂A为0.2mol/LCuSO4溶液,发现铝条表面无明显变化,于是改变实验条件,探究铝和CuSO4溶液、CuCl2溶液反应的影响因素。用不同的试剂A进行实验1~实验4,并记录实验现象:
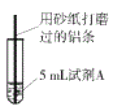
实验序号 | 试剂A | 实验现象 |
1 | 0.2mol/LCuCl2溶液 | 铝条表面有气泡产生,并有红色固体析出 |
2 | 0.2mol/LCuSO4溶液,再加入一定质量的NaCl固体 | 开始铝条表面无明显变化,加NaCl后,铝条表面有气泡产生,并有红色固体析出 |
3 | 2mol/LCuSO4溶液 | 铝条表面有少量气泡产生,并有少量红色固体 |
4 | 2mol/LCuCl2溶液 | 反应非常剧烈,有大量气泡产生,溶液变成棕褐色,有红色固体和白色固体生成 |
(1)实验1中,铝条表面析出红色固体的反应的离子方程式为_________。
(2)实验2的目的是证明铜盐中的阴离子Cl-是导致实验1中反应迅速发生的原因,实验2中加入NaCl固体的质量为______g。
(3)实验3的目的是_________ 。
(4)经检验可知,实验4中白色固体为CuCl。甲同学认为产生白色固体的原因可能是发生了Cu+CuCl2=2CuCl的反应,他设计了右图所示实验证明该反应能够发生。
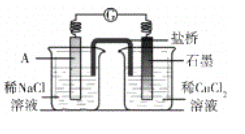
①A极的电极材料是_________。
②能证明该反应发生的实验现象是_________ 。
(5)为探究实验4中溶液呈现棕褐色的原因,分别取白色CuCl固体进行以下实验:
实验序号 | 实验操作 | 实验现象 |
i | 加入浓NaCl溶液 | 沉淀溶解,形成无色溶液 |
ii | 加入饱和AlCl3溶液 | 沉淀溶解,形成褐色溶液 |
iii | 向i所得溶液中加入2mol/LCuCl2溶液 | 溶液由无色变为褐色 |
查阅资料知:CuCl难溶于水,能溶解在Cl-浓度较大的溶液中,生成[CuCl2]
①由述球实验及资料可推断,实验4中溶液呈棕褐色的原因可能是[CuCl2]-与_____作用的结果。
②为确证实验4所得的棕褐色溶液中含有[CuCl2]-,应补充的实验是_______。
(6)上述实验说明,铝和CuSO4溶液、CuCl2溶液的反应现象与______有关。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应2SO2(g)+O2(g)![]() 2SO3(g)是硫酸工业的最重要反应,因该反应中使用催化剂而被命名为接触法制硫酸。
2SO3(g)是硫酸工业的最重要反应,因该反应中使用催化剂而被命名为接触法制硫酸。
(1)使用V2O5催化该反应时,涉及到催化剂V2O5的热化学反应有:
①V2O5(s)+SO2(g)![]() V2O4(s)+SO3(g) △H1=+59.6kJ·mol-1
V2O4(s)+SO3(g) △H1=+59.6kJ·mol-1
②2V2O4(s)+O2(g)![]() 2V2O5(s) △H2=-315.4kJ·mol-1
2V2O5(s) △H2=-315.4kJ·mol-1
则2SO2(g)+O2(g)![]() 2SO3(g) △H3=__________kJ·mol-1
2SO3(g) △H3=__________kJ·mol-1
(2)向10 L密闭容器中加入V2O4(s)、SO2(g)各1 mol及一定量的O2,改变加入O2的量,在常温下反应一段时间后,测得容器中V2O4、V2O5、SO2和SO3的量随反应前加入O2的变化如图甲所示,图中没有生成SO3的可能原因是_________________________
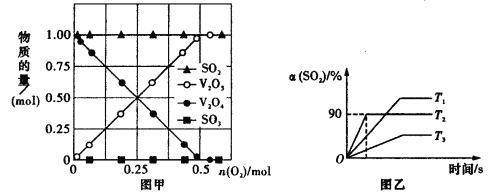
(3)在原10 L的恒容装置中,加入V2O5(s)、SO2(g)各0.6 mol,O2(g)0.3 mol,分别在T1、T2、T3时进行反应,测得容器中SO2的转化率如图乙所示。
①T2时,2SO2(g)+O2(g)![]() 2SO3(g)的平衡常数K=__________。
2SO3(g)的平衡常数K=__________。
②结合化学方程式及相关文字,解释反应为什么在T3条件下比T2条件下的速率慢:_____
(4)在温度T2使用V2O5进行反应:2SO2(g)+O2(g)![]() 2SO3(g),在保证O2(g)的浓度不变的条件下,增大容器的体积,平衡__________(填字母代号)。
2SO3(g),在保证O2(g)的浓度不变的条件下,增大容器的体积,平衡__________(填字母代号)。
A.向正反应方向移动 B.向逆反应方向移动
C.不移动 D.无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】配离子的稳定性可用K不稳衡量,例如Ag(NH3)2]+的K不稳=![]() 。在一定温度下,向0.1 mol/L硝酸银溶液中滴入稀氨水,发生反应Ag++2NH3[Ag(NH3)2]+]。溶液中pNH3与δ(X)的关系如图。其中pNH3=-lg[c(NH3)]、δ(X)=
。在一定温度下,向0.1 mol/L硝酸银溶液中滴入稀氨水,发生反应Ag++2NH3[Ag(NH3)2]+]。溶液中pNH3与δ(X)的关系如图。其中pNH3=-lg[c(NH3)]、δ(X)=![]() (X代表Ag+或Ag(NH3)2]+。下列说法不正确的是
(X代表Ag+或Ag(NH3)2]+。下列说法不正确的是
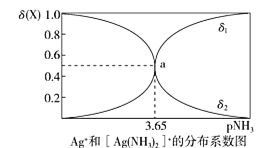
A.图中δ2代表的是δ([Ag(NH3)2]+])B.向溶液中滴入稀硝酸,δ(Ag+)减小
C.该溶液中c(NH4+)+c(H+)=c(OH-)D.该温度时,K不稳([Ag(NH3)2]+)=10-7.3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环丁基甲酸是重要的有机合成中间体,如图是用烯烃A和羧酸D合成环丁基甲酸的路线。
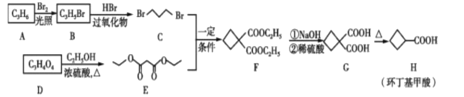
请回答下列问题:
(1)A的结构简式为____。
(2)B中官能团的名称为____、____。
(3)B→C的反应类型为____。D→E的反应类型为__________
(4)C+E→F的化学方程式为________
(5)满足下列条件的H的所有同分异构体(不考虑立体异构)共有____种,其中核磁共振氢谱有3组峰的结构简式为____。
①能使溴的四氯化碳溶液褪色
②能与NaOH溶液反应
③能与银氨溶液发生银镜反应
④不含环状结构
(6)以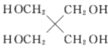 和
和![]() 为原料,选用必要的无机试剂,写出合成
为原料,选用必要的无机试剂,写出合成![]() 的路线________(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)
的路线________(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某科研小组模拟“人工树叶”电化学装置如下图所示,该装置能将H2O和CO2转化为糖类(C6H12O6)和O2,X、Y是特殊催化剂型电极,下列说法正确的是
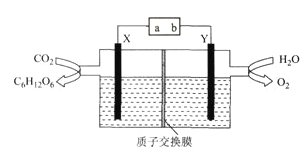
A. 电源a极为正极
B. 该装置中Y电极发生还原反应
C. X电极的电极反应式为6CO2+24H++24e-=C6H12O6+6H2O
D. 理论上,每生成22.4L(标准状况下)O2,必有4mol H+由X极区向Y极区迁移
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镇痛药物J的合成方法如下:
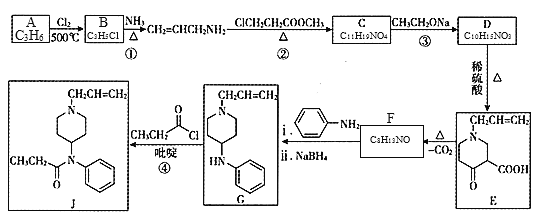
已知:
![]() +Cl-R3
+Cl-R3![]()
![]() +HCl
+HCl
R1COOR2+R3CH2COOR4![]()
![]() +R2OH
+R2OH
![]()
![]()
![]()
(R1、R2、R3、R4为氢或烃基)
(1)B的名称为______;F的结构简式为______。
(2)C中含氧官能团名称为______;②的反应类型为______反应。
(3)③的化学方程式为______。
(4)有机物K分子组成比F少两个氢原子,符合下列要求的K的同分异构体有______种。
A.遇FeCl3显紫色 B.苯环上有三个取代基
(5)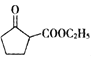 是一种重要的化工中间体。以环已醇(
是一种重要的化工中间体。以环已醇(![]() )和乙醇为起始原料,结合己知信息选择必要的无机试剂,写出
)和乙醇为起始原料,结合己知信息选择必要的无机试剂,写出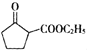 的合成路线______。(已知:RHC=CHR
的合成路线______。(已知:RHC=CHR![]() RCOOH+R′COOH,R、R′为烃基。用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)
RCOOH+R′COOH,R、R′为烃基。用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:MOH碱性比NOH强。常温下,用HCl气体分别改变浓度均为0.1mol·L-1的MOH溶液和NOH溶液的pH(溶液体积变化忽略不计),溶液中M+、N+的物质的量浓度负对数与溶液的pH关系如下图,pR=-lgc(M+)或-lgc(N+),下列说法错误的是( )
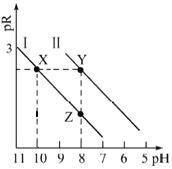
A.曲线I表示-lgc(M+)与pH关系
B.常温下,电离常数![]() =100
=100
C.溶液中水的电离程度:Y>X
D.对应溶液中c(Cl-):Y>Z
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用酸解法制钛白粉产生的废液[含有大量![]() 和少量
和少量![]() 、
、![]() ],生产铁红和补血剂乳酸亚铁。其生产步骤如下:
],生产铁红和补血剂乳酸亚铁。其生产步骤如下:
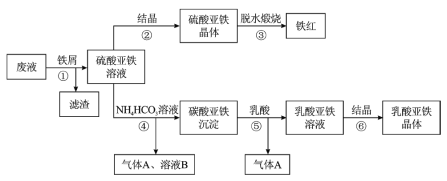
已知:![]() 可溶于水,在水中可以电离为
可溶于水,在水中可以电离为![]() 和
和![]() 水解成
水解成![]() 沉淀为可逆反应;乳酸亚铁晶体的化学式为:
沉淀为可逆反应;乳酸亚铁晶体的化学式为:![]() 。请回答:
。请回答:
(1)步骤①加入铁屑的目的一是还原少量![]() ;二是使少量
;二是使少量![]() 转化为
转化为![]() 滤渣,用平衡移动的原理解释得到滤渣的原因________。
滤渣,用平衡移动的原理解释得到滤渣的原因________。
(2)硫酸亚铁在空气中煅烧生成铁红和三氧化硫,该反应中氧化剂和还原剂的物质的量之比为________。
(3)步骤④的离子方程式是______。
(4)步骤⑥所得溶液需隔绝空气______、________过滤、洗涤、干燥得乳酸亚铁晶体。该晶体存放时应____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com