
| A. | 标准状况下,5.6L CO2与足量Na2O2反应转移的电子数为0.5NA | |
| B. | 2L 0.5 mol•L-1 亚硫酸溶液中含有的H+数为2NA | |
| C. | 分子总数为NA的SO2和CO2混合气体中含有的氧原子数为2NA | |
| D. | 1mol FeI2与足量氯气反应时转移的电子数为2NA |
分析 A.依据方程式:2Na2O2+2CO2=2Na2CO3+O2,消耗2mol二氧化碳,转移2mol电子;
B.亚硫酸是弱酸,在溶液中不能完全电离;
C.1个二氧化硫分子和1个二氧化碳分子都含有2个氧原子;
D.碘化亚铁与氯气反应生成氯化铁和单质碘,1mol碘化亚铁反应失去3mol电子.
解答 解:A.标准状况下,5.6LCO2物质的量为$\frac{5.6L}{22.4L/mol}$=0.25mol,依据方程式:2Na2O2+2CO2=2Na2CO3+O2,消耗2mol二氧化碳,转移2mol电子,所以转移电子数为:0.25 NA,故A错误;
B.亚硫酸是弱酸,在溶液中不能完全电离,故溶液中的氢离子的个数小于2NA个,故B错误;
C.1个二氧化硫分子和1个二氧化碳分子都含有2个氧原子,所以分子总数为NA的SO2和CO2混合气体中含有的氧原子数为2NA,故C正确;
D.碘化亚铁与氯气反应生成氯化铁和单质碘,1mol FeI2与足量氯气反应时转移的电子数为3NA,故D错误;
故选:C.
点评 本题考查阿伏加德罗常数的综合应用,熟练地运用与物质的量相关的计算公式,明确物质的结构是解题关键,注意氧化还原反应中电子转移数目的计算,题目难度不大.


 华东师大版一课一练系列答案
华东师大版一课一练系列答案 孟建平名校考卷系列答案
孟建平名校考卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 海水蒸发→云→降水,这是地球水循环的过程,该过程主要是物理变化 | |
| B. | 海水中所含的常量元素大部分以盐的形式存在,其中含量最高的盐是氯化钠 | |
| C. | 海洋是化学元素的集散地,元素周期表所有的元素在海水中都能找到 | |
| D. | 由海水制备镁、氯、溴、碘等单质均需要涉及氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
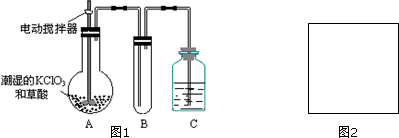 X+5H2O,则X的化学式NaCl.
X+5H2O,则X的化学式NaCl.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na多 | B. | Mg多 | C. | Al多 | D. | 一样 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 过氧化钠与水反应时,生成22.4L氧气转移的电子数为2 NA | |
| B. | 18g D2O中含有的电子数和中子数均为10 NA | |
| C. | 密闭容器中2mol NO与1mol O2充分反应,产物的分子数为2 NA | |
| D. | 1mol Na与足量的O2反应,生成Na2O和Na2O2的混合物,钠失去 NA个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 保存FeCl2溶液时,通常在溶液中加少量的单质铁 | |
| B. | 常温下,浓硝酸可以用铁罐车贮运 | |
| C. | 可用湿润的蓝色石蕊试纸检验氨气 | |
| D. | 除去CO2中混有的HCl,可通过盛有饱和NaHCO3溶液的洗瓶 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 黏土 | B. | 纯碱 | C. | 石灰石 | D. | 熟石灰 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com