
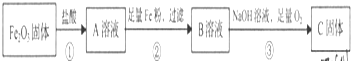
分析 氧化铁是碱性氧化物与盐酸反应生成氯化铁和盐酸的混合溶液,加入足量的铁粉过滤,滤液中含有氯化亚铁,通入氢氧化钠和氧气,得到氢氧化铁,由此分析解答.
解答 解:氧化铁是碱性氧化物与盐酸反应生成氯化铁和盐酸的混合溶液,加入足量的铁粉过滤,滤液中含有氯化亚铁,通入氢氧化钠和氧气,得到氢氧化铁,
(1)反应①是碱性氧化物和酸反应,是复分解反应、②是铁离子与铁发生氧化还原反应、③氢氧化亚铁被氧化成氢氧化铁,属于氧化还原反应的是②、③,故答案为:②、③;
(2)向A溶液是氯化铁溶液,所以滴入儿滴KSCN溶液后,可观察到的现象是溶液呈血红色,故答案为:溶液呈血红色;
(3)C的化学式是Fe(OH)3,故答案为:Fe(OH)3;
(4)写出反应①是氧化铁与盐酸反应生成氯化铁与水,化学方程式为Fe2O3+6HCl═2FeCl3+3H2O,反应②是铁与铁离子的氧化还原反应,离子方程式为:2Fe3++Fe=3Fe2+,故答案为:Fe2O3+6HCl═2FeCl3+3H2O;2Fe3++Fe=3Fe2+.
点评 本题考查金属及其化合物的性质,为高频考点,把握铁及其化合物的性质及发生的氧化还原反应为解答的关键,侧重分析与应用能力的考查,综合性较强,涉及离子反应、化学反应等,题目难度不大.


 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案科目:高中化学 来源: 题型:解答题
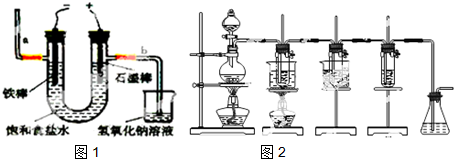
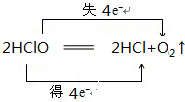 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X、Z两种元素可形成X2Z和X2Y2两种常见共价化合物 | |
| B. | 工业上常用电解熔融的W和M氯化物的方法分别制取W、M两种单质 | |
| C. | M的最高价氧化物与Y、W两元素最高价氧化物对应水化物均能反应生成盐和水 | |
| D. | X与W可形成离子化合物,且该离子化合物具有较强还原性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1 mol | B. | 0.15 mol | C. | 0.22 mol | D. | 0.05 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:2:4 | B. | 1:2:3 | C. | 3:2:1 | D. | 2:5:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | N2→NH3→NO→NO2→HNO3 | B. | Na→Na2O2→NaOH→Na2CO3 | ||
| C. | S→SO3→H2SO4→Na2SO4 | D. | Si→SiO2→Na2SiO3→H2SiO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com