
1.52g铜镁合金完全溶解于50 mL密度为1.40g/cm3、质量分数为63%的浓硝酸中,得到NO2和N2O4 的混合气体1120mL (标准状况),向反应后的溶液中加入1.0mol·L-1NaOH溶液,当金属离子全部沉淀时,得到2.54 g沉淀。下列说法不正确的是
A.该合金中铜与镁的物质的量之比是2:1
B.该浓硝酸中HNO3的物质的量浓度是14.0mol·L-1
C.NO2和N2O4的混合气体中,NO2和N2O4的物质的量之比是1:4
D.得到2.54g沉淀时,加入NaOH溶液的体积是640mL
科目:高中化学 来源:2015-2016学年浙江省金兰教育合作组织高一上学期期中联考化学试卷(解析版) 题型:选择题
当温度与压强不变时,气体体积主要取决于
A.气体分子间的平均距离 B.气体分子数目的多少
C.气体的摩尔质量大小 D.气体密度的大小
查看答案和解析>>
科目:高中化学 来源:2016届湖南省十校共同体高三上学期12月联考化学试卷(解析版) 题型:填空题
NH3是一种重要的化工产品。
(1)根据氨气还原氧化铜的反应,可设计测定铜元素相对原子质量Ar(Cu)(近似值)的实验。先称量反应物氧化铜的质量m(CuO),反应完全后测定生成物水的质量m(H2O),由此计算Ar(Cu)。为此,提供的实验仪器及试剂如下(根据实验需要,装置可重复选择,加入的NH4 Cl与Ca(OH)2的量足以产生使CuO完全还原为N2的氨气)。

请回答下列问题:
①氨气还原炽热氧化铜的化学方程式为_______________;
②从所提供的仪器及试剂中选择并组装本实验的一套合理、简单的装置,按气流方向的连接顺序为(用图中标注的字母表示)A→ ;
③在本实验中,若测得m( CuO) =ag,m(H2O)=b g,则Ar(Cu)= ;
④在本实验中,使测定结果Ar(Cu)偏大的是 (填字母);
A.CuO未完全起反应 B.CuO不干燥
C.CuO中混有不反应的杂质 D.NH4 Cl与Ca(OH)2混合物不干燥

(2)按右图装置进行NH3性质实验。
①先打开旋塞1,B瓶中的现象是 原因是
②稳定后,关闭旋塞1,再打开旋塞2,B瓶中的现象是 。
查看答案和解析>>
科目:高中化学 来源:2016届江苏省高三上第二次阶段测化学试卷(解析版) 题型:实验题
某化学兴趣小组利用某废弃的氧化铜锌矿制取活性ZnO,实验流程如下:

请回答下列问题:
(1)氧化铜锌矿中含有少量的CuS和ZnS,在H2SO4的作用下ZnS可以溶解而CuS不溶,则相同温度下:Ksp(CuS)__________ Ksp(ZnS)(选填“>”“<”或“=”).
(2)甲、乙两同学选用下列仪器,采用不同的方法制取氨气。
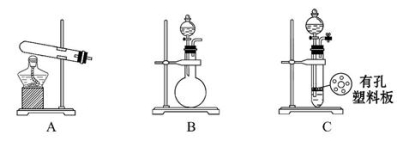
①甲同学使用的药品是熟石灰与氯化铵,则应选用装置__________(填写装置代号)
②乙同学选用了装置B,则使用的两种药品的名称为_________。
(3)沉淀过程需降温冷却的原因为 、 。
(4)除铁后得到的Fe(OH)3可用KClO溶液在碱性环境将其氧化得到一种高效的多功能水处理剂--K2FeO4,写出该反应的离子方程式 。
查看答案和解析>>
科目:高中化学 来源:2016届江苏省南京市六校高三上学期12月联考化学试卷(解析版) 题型:实验题
工业上利用废铁屑(含少量氧化铝、氧化铁等)生产碱式硫酸铁[Fe(OH)SO4]的工艺流程如下:

已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 |
开始沉淀 | 2.3 | 7.5 | 3.4 |
完全沉淀 | 3.2 | 9.7 | 4.4 |
回答下列问题:
(1)加入少量NaHCO3的目的是 ,该工艺中“搅拌”的作用是 。
(2)反应Ⅱ中的离子方程式为 ,在实际生产中,反应Ⅱ常同时通入O2以减少NaNO2的用量,O2的作用是 。(用化学方程式表示)
(3)生产中碱式硫酸铁溶液蒸发时需要在减压条件下的原因是 。
(4)在医药上常用硫酸亚铁与硫酸、硝酸的混合液反应制备碱式硫酸铁。根据我国质量标准,产品中不得含有Fe2+及NO3-。为检验所得产品中是否含有Fe2+,应使用的试剂为 。(填写字母)
A.氯水 B.KSCN溶液 C.NaOH溶液 D.酸性KMnO4溶液
查看答案和解析>>
科目:高中化学 来源:2016届江西省高三上学期第三次月考化学试卷(解析版) 题型:选择题
Al、Fe、Cu都是重要而常见的金属,下列有关说法正确的是
A.三者的单质在常温下都能溶于浓硫酸和浓硝酸
B.三者的单质放置在空气中均只生成氧化物
C.三者所对应的氢氧化物在水中都存在溶解平衡
D.工业上制备这三种金属的方法依次为电解法、热分解法和热还原法
查看答案和解析>>
科目:高中化学 来源:2016届上海市十三校高三上学期第一次联考化学试卷(解析版) 题型:填空题
氮元素在自然界中存在多种价态,结合题干回答下列问题:
23.氮元素原子核外有 个未成对电子,最外层有 种能量不同的电子。
24.氮和磷是同主族元素,下列能说明二者非金属性相对强弱的是 (填编号)。
a.NH3比PH3稳定性强
b.氮气与氢气能直接化合,磷与氢气很难直接化合
c.硝酸显强氧化性,磷酸不显强氧化性
d.氮气常温是气体,磷单质是固体
25.已知,氯胺NH2Cl熔点-66℃,NH4Cl熔点340℃,氯胺的电子式为 ,从物质结构的角度解释两者熔点相差较大的原因 。
26.NH2Cl比HClO稳定性高,易水解,因水解后能产生可杀菌消毒的物质而成为饮用水的缓释消毒剂,NH2Cl发生水解的化学方程式为 。
27.工业上利用铝粉除去含氮废水中的NO3-,当控制溶液pH在10.7左右时,反应过程中生成AlO2-、氮气和氨气,若氮气和氨气的体积比为4 : 1,则还原剂和氧化剂的物质的量之比为 ,若氮气和氨气的体积比为1 : 1,则除去0.1mol NO3-,消耗铝______g。
查看答案和解析>>
科目:高中化学 来源:2016届浙江省高三上学期第三次月考化学试卷(解析版) 题型:选择题
设阿伏伽德罗常数为NA,下列说法正确的是
A.标准状况下,22. 4L甲醛完全燃烧产生NA个CO2分子
B.1L1mol/L Na2CO3溶液中,阴离子个数等于NA
C.100 g 98%的浓硫酸中含氧原子个数为4NA
D.常温常压下,1mol白磷中含有共价键为4NA
查看答案和解析>>
科目:高中化学 来源:2016届河北省张家口市四校高三上学期联考化学试卷(解析版) 题型:选择题
下列关于有机物的命名中不正确的是
A.2,2─二甲基戊烷 B.2─乙基戊烷
C.3,4─二甲基辛烷 D.3─甲基己烷
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com