
 Al、Ti、Fe、Cu是几种常见的重要金属.根据要求回答下列问题:
Al、Ti、Fe、Cu是几种常见的重要金属.根据要求回答下列问题:| 元素 | A | B | |
| 电离能(kJ/mol) | I1 | 717 | 759 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 | |
分析 (1)由反应物、生成物可知化学反应;
(2)Fe的原子序数为26,位于第ⅤⅢ族,3d电子半满为稳定结构;
(3)[Cu(NH3)4]SO4•H2O中[Cu(NH3)4]2+为平面正四边形结构,水为V型,SO42-中S为sp3杂化,且不存在孤对电子,N为sp3杂化,有1对孤对电子;
(4)由均摊法计算氧化亚铜晶胞中Cu原子和O原子的数目,根据密度计算公式ρ=$\frac{m}{V}$计算即可.
解答 解:(1)铝粉与石墨、TiO2高温下反应生成TiC和另外一种耐高温物质X,结合原子守恒可知反应为4Al+3C+3TiO2$\frac{\underline{\;高温\;}}{\;}$3TiC+2Al2O3,
故答案为:4Al+3C+3TiO2$\frac{\underline{\;高温\;}}{\;}$3TiC+2Al2O3;
(2)Fe的原子序数为26,位于第ⅤⅢ族,Fe原子的价电子排布式为3d64s2,气态Mn2+再失去一个电子比气态Fe2+再失去一个电子难,可知Mn易失去2个电子达到3d电子半满的稳定结构,而Fe失去2个电子达到3d电子半满的稳定结构,B为Fe的电离能数据,
故答案为:3d64s2;B;
(3)[Cu(NH3)4]SO4•H2O中[Cu(NH3)4]2+为平面正四边形结构,水为V型,SO42-中S为sp3杂化,且不存在孤对电子,为正四面体结构;含5个原子且价电子数为32的等电子体的分子为SiF4、CCl4(GeCl4);N形成3个单键,且有1对孤对电子,N为sp3杂化,
故答案为:SO42-;SiF4、CCl4(GeCl4);sp3;
(4)由Cu2O的晶胞结构图可知,白球为1+8×$\frac{1}{8}$=2个,黑球为4个,则黑球为Cu+,Cu+周围有2个氧离子,则Cu+的配位数为2;该晶胞的边长为a pm,则Cu2O的密度为$\frac{\frac{144g/mol×2}{{N}_{A}}}{(a×1{0}^{-10}cm)^{3}}$=$\frac{288×1{0}^{30}}{{a}^{3}×{N}_{A}}$ g/cm3,故答案为:$\frac{288×1{0}^{30}}{{a}^{3}×{N}_{A}}$ g/cm3.
点评 本题考查晶胞计算及原子结构,为高频考点,把握晶体计算及杂化理论、电离能等为解答的关键,侧重原子结构与性质的考查,题目难度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 1 | B. | 2 | C. | 3 | D. | 4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
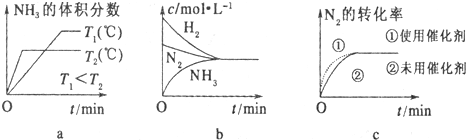
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 少量NaHCO3与过量Ca(OH)2反应:Ca2++2OH-+2HCO3-═CaCO3↓+2H2O+CO32- | |
| B. | 在CuSO4溶液中加Ba(OH)2溶液 SO42-+Ba2+═BaSO4↓ | |
| C. | Na2S溶液中通入H2S气体 S2-+H+═HS- | |
| D. | NaHCO3溶液与KHSO4溶液反应 HCO3-+H+═CO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 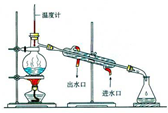 用如图装置分离甲苯和水 | |
| B. |  蒸干NH4Cl溶液制备NH4Cl晶体 | |
| C. |  证明Ag2S溶解度小于AgCl | |
| D. |  关闭分液漏斗活塞,向外拉动针筒活塞,松开后活塞恢复原位置,证明装置气密性良好 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 乳酸乙酯(2-羟基丙酸乙酯)常用于调制果香型、乳香型食用和酒用香精.为了在实验室制取乳酸乙酯,某研究性学习小组同学首先查阅资料,获得下列信息:
乳酸乙酯(2-羟基丙酸乙酯)常用于调制果香型、乳香型食用和酒用香精.为了在实验室制取乳酸乙酯,某研究性学习小组同学首先查阅资料,获得下列信息:| 物质 | 水 | 乙醇 | 乳酸 | 苯 | 乳酸乙酯 |
| 沸点/℃ | 100 | 78.4 | 122 | 80.10 | 154 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 右 (M+2Q) | B. | 左 (M+2Q) | C. | 右 (M+4Q) | D. | 左 (M+4Q) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al3+ | B. | Al(OH)3 | C. | AlO2- | D. | Al3+ Al(OH)3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com