


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、乙烯能使酸性高锰酸钾溶液褪色,是由于乙烯发生了氧化反应 |
| B、乙烯可在氧气中燃烧,该反应属于乙烯的氧化反应 |
| C、乙烯能使溴的四氯化碳溶液褪色,该反应属于加成反应 |
| D、将乙烯通入溴水中,反应后得到均一、透明的液体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
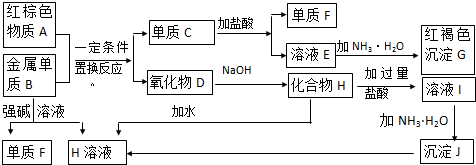
查看答案和解析>>
科目:高中化学 来源: 题型:
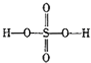 过硫酸:
过硫酸:
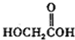 (b)
(b) 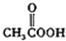 (c)H2O2(d)
(c)H2O2(d) 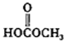 (e)
(e)  (f)
(f) 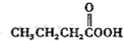 (g)O3(h)
(g)O3(h) 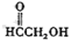
查看答案和解析>>
科目:高中化学 来源: 题型:
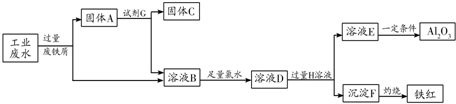
查看答案和解析>>
科目:高中化学 来源: 题型:
 以黄铜矿精矿为原料,制取硫酸铜及金属铜的工艺如下所示:
以黄铜矿精矿为原料,制取硫酸铜及金属铜的工艺如下所示:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
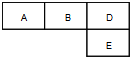 有M、A、B、D、N、E六种短周期元素,原子序数依次增大.M元素的单质是自然界最轻的气体,N元素的原子半径是所在周期原子半径最大的.A、B、D、E分别在右表(周期表的一部分)占有相应的位置,它们的原子序数之和为37.试回答:
有M、A、B、D、N、E六种短周期元素,原子序数依次增大.M元素的单质是自然界最轻的气体,N元素的原子半径是所在周期原子半径最大的.A、B、D、E分别在右表(周期表的一部分)占有相应的位置,它们的原子序数之和为37.试回答: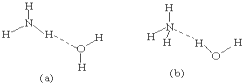
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com