
| A. | 共价化合物中只有共价键,一定没有离子键 | |
| B. | 金属和非金属一定形成离子化合物 | |
| C. | 含有离子键的化合物一定是离子化合物 | |
| D. | 离子化合物中可能含有极性共价键 |
分析 A.共价化合物中只有共价键;
B.金属与非金属元素可能形成共价键;
C.含有离子键的化合物是离子化合物;
D.离子化合物中一定有离子键,可能含有共价键.
解答 解:A.共价化合物中只有共价键,一定没有离子键,含有离子键的是离子化合物,故A正确;
B.金属与非金属元素可能形成共价键,如铝与氯气反应生成的氯化铝为共价化合物,只含有共价键,故B错误;
C.含有离子键的化合物是离子化合物,如NaCl中钠离子与氯离子形成离子键,故C正确;
D.离子化合物中一定有离子键,可能含有共价键,如NaOH中含有O-H共价键,故D正确.
故选B.
点评 本题主要考查了键的极性与分子极性、化学键与化合物的关系,难度不大,注意举例说明,侧重于基础知识的考查.


科目:高中化学 来源: 题型:解答题
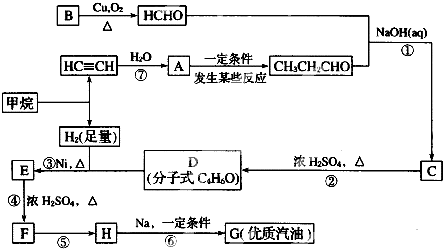
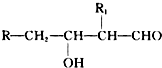
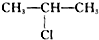
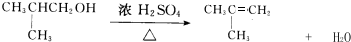 ;H→G
;H→G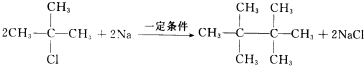 .
.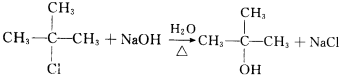 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③④⑤⑦⑧⑨ | B. | ③⑤⑥⑦⑧⑨ | C. | ②③④⑤⑦⑧ | D. | ①②④⑥⑧⑨ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③ | B. | ②④ | C. | ①④ | D. | ②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
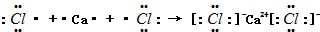 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | FeCl3 | B. | K2SO3 | C. | NaOH | D. | Na2S |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | AlO2- | B. | Al3+ | C. | Al(OH)3 | D. | Al(OH)3和Al3+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com