
【题目】通过NO传感器可监测NO的含量,其工作原理如图所示.下列说法错误的是( ) 
A.该装置实现化学能向电能的转化
B.该电池的总反应为2NO+O2═2NO2
C.NiO电极的电极反应式:NO+O2﹣﹣2e﹣═NO2
D.当有2.24L的O2参与反应时,转移了0.4mole﹣
科目:高中化学 来源: 题型:
【题目】含氯的物质与人们的生活密切相关.已知氯元素常见的化合价有﹣1、0、+1、+3、+5、+7六种,其不同价态的物质间可以相互转化.回答下列问题.
(1)氯原子的原子结构示意图;氯离子的电子式 .
(2)氯气能使湿润的有色布条褪色,起到漂白作用的物质是(写名称).漂粉精的主要有效成分是(写化学式).
(3)实验室制取氯化氢的化学方程式;
(4)工业上将含有氯气的尾气通过进行处理,在处理时发生的反应中氯气作为 . a.氧化剂 b.还原剂 c.既是氧化剂又是还原剂 d.既不是氧化剂又不是还原剂
(5)写出氯气的两种用途 , .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在实验室里制取乙烯,常因温度过高而使乙醇和浓硫酸反应生成少量的二氧化硫,有人设计实验图以确认上述混合气体中有C2H4和SO2 . 回答下列问题: 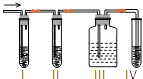
(1)实验室制备乙烯的反应方程式是:
(2)I、Ⅱ、Ⅲ、IV装置可盛放的试剂是I;Ⅱ;Ⅲ;Ⅳ . (将下列有关试剂的序号填入空格内). A.品红溶液 B.NaOH溶液 C.浓硫酸 D.酸性KMnO4溶液
(3)能说明SO2气体存在的现象是 .
(4)使用装置II的目的是 .
(5)使用装置III的目的是 .
(6)确定含有乙烯的现象是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学研究铝及其化合物的性质时设计了如下两个实验方案.
方案①:2.7g Al ![]() X溶液
X溶液 ![]() Al(OH)3沉淀
Al(OH)3沉淀
方案②:2.7g Al ![]() Y溶液
Y溶液 ![]() Al(OH)3沉淀
Al(OH)3沉淀
NaOH和HCl的浓度均是3mol/L,如图是向X溶液和Y溶液中分别加入NaOH和HCl时产生沉淀的物质的量与加入盐酸和氢氧化钠溶液体积之间的关系,下列说法不正确的是( )
A.b曲线表示的是向X溶液中加入NaOH溶液
B.在O点时两方案中所得溶液浓度相等
C.方案②中对应的O点HCl恰好反应完
D.X溶液显酸性,Y溶液显碱性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】写出有关反应的化学方程式:
(1)钠投入水中 .
(2)过氧化钠作为潜水艇和呼吸面具中氧气的来源; .
(3)实验室制取氯气时,多余的尾气用碱液来吸收: .
(4)漂白粉露置在空气中为什么会失效? .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】熔融碳酸盐燃料电池,是由多孔陶瓷阴极、多孔陶瓷电解质隔膜、多孔金属阳极、金属极板构成的燃料电池.其电解质是熔融态碳酸盐.如图是用熔融碳酸盐作电解质,氢气和氧气形成的燃料电池,下列说法不正确的是( ) 
A.该电池放电时,负极的反应式为:H2﹣2e﹣+CO32﹣═H2O+CO2
B.该电池中CO32﹣的为由左边移向右边移动
C.该电池放电时,正极的反应式为:O2+2CO2+4e﹣═2CO32﹣
D.该电池放电时,当转移4mol e﹣时正极消耗1mol O2和2mol CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定质量的铝铁合金溶于足量的NaOH溶液中,完全反应后产生3.36L气体(标准状况下);用同样质量的铝铁合金完全溶于足量的盐酸中,完全反应后产生6.72L气体(标准状况下),则该合金中铝、铁的物质的量之比为( )
A.1:1
B.2:3
C.3:2
D.3:5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在101kPa时,1mol纯物质完全燃烧生成稳定的氧化物时所放出的热量,叫做该物质的燃烧热,甲烷的燃烧热是890.3kJmol﹣1 , 则下列热化学方程式书写正确的是( )
A.CH4(g)+ ![]() O2(g)═CO(g)+2H2O(l)△H=﹣890.3kJmol﹣1
O2(g)═CO(g)+2H2O(l)△H=﹣890.3kJmol﹣1
B.CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=﹣890.3kJmol﹣1
C.CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=+890.3kJmol﹣1
D.CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=﹣890.3kJmol﹣1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com