
| A. | 1×10-1mol/L | B. | 1×10-6mol/L | C. | 1×10-3mol/L | D. | 1×10-13mol/L |
分析 溶液中溶质为HCl,溶液的pH=1,则溶液中c(H+)=10-pH =10-1 mol/L=0.1molo/L,由水电离出的c(H+)=呈(OH-)=$\frac{{K}_{w}}{c({H}^{+})}$.
解答 解:溶液中溶质为HCl,溶液的pH=1,则溶液中c(H+)=10-pH =10-1 mol/L=0.1molo/L,由水电离出的c(H+)=呈(OH-)=$\frac{{K}_{w}}{c({H}^{+})}$=$\frac{1{0}^{-14}}{0.1}$mol/L=1×10-13mol/L,
故选D.
点评 本题考查弱电解质的电离,为高频考点,侧重考查学生分析计算能力,酸或碱抑制水电离,含有弱离子的盐促进水电离,注意:酸溶液中水电离出的c(H+)不等于溶液中c(H+),为易错点.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,11.2L苯中含有分子数目为0.5NA | |
| B. | 常温下,1.8g水中含有的电子数为NA | |
| C. | 0.1 mol Cl2与足量氢氧化钠溶液反应,转移的电子数为0.2NA | |
| D. | 1L0.1mol/L的NH4CL溶液中含NH4+的数目为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C16H22O5 | B. | C14H16O4 | C. | C14H18O5 | D. | C14H20O5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 烧碱溶液存放在橡皮塞的试剂瓶中 | |
| B. | 金属钠着火燃烧时,用泡沫灭火器灭火 | |
| C. | 依据丁达尔现象可将分散系分为溶液、胶体和浊液 | |
| D. | 向石蕊试液中加入新制氯水,石蕊试液只变红 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | +99.7kJ•mol-1 | B. | +29.7kJ•mol-1 | C. | -20.6kJ•mol-1 | D. | -241.8kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,3.2g O 2所含的原子数为0.2NA | |
| B. | 标准状况下,18g H2 O所含的氧原子数目为NA | |
| C. | 常温常压下,92g NO2和N2O 4的混合气体中含有的原子总数为6 NA | |
| D. | 标准状况下,22.4LCH4与22.4L N2所含原子数均为2 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
.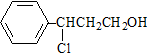 $→_{△}^{O_{2}/Cu}$$→_{Ⅱ}^{一定条件}$乙
$→_{△}^{O_{2}/Cu}$$→_{Ⅱ}^{一定条件}$乙 ,设计步骤Ⅰ的目的是保护碳碳双键,防止被氧化.
,设计步骤Ⅰ的目的是保护碳碳双键,防止被氧化.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com