
| A. | 都属于氧化还原反应 | |
| B. | 等物质的量的上述物质产生气体体积(相同状况)的大小关系是:Na2O2=CaC2<CaH2=Mg3N2 | |
| C. | Na2O2、CaH2与水反应时水作氧化剂 | |
| D. | CaH2与水反应时产生H2,它既是氧化产物和又是还原产物 |
分析 发生2Na2O2+2H2O=4NaOH+O2↑、CaH2+H2O=Ca(OH)2+H2↑、Mg3N2+6H2O═3Mg(OH)2+2NH3↑、CaC2+2H2O═Ca(OH)2+C2H2↑,结合元素的化合价判断,含元素化合价变化的反应为氧化还原反应,以此来解答.
解答 解:A.CaC2、Mg3N2与水反应生成C2H2和NH3,为水解反应,元素化合价没有发生变化,不属于氧化还原反应,故A错误;
B.设均为1mol,由原子守恒可知,1molNa2O2反应生成0.5molO2,1molCaC2反应生成1molC2H2,1molCaH2反应生成1molH2,1molMg3N2反应生成2molNH3,则生成气体的关系为Na2O2<CaC2<CaH2<Mg3N2,故B错误;
C.Na2O2自身发生氧化还原反应,水既不是氧化剂也不是还原剂,而CaH2+H2O=Ca(OH)2+H2↑中水为氧化剂,故C错误;
D.CaH2与水发生氧化还原反应,方程式为CaH2+H2O=Ca(OH)2+H2↑,反应中H2既是氧化产物又是还原产物,故D正确;
故选D.
点评 本题考查氧化还原反应,为高频考点,侧重于学生的分析能力的考查,注意把握常见水解反应的特点,根据相关反应的方程式进行判断,题目难度不大.


 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:填空题
| 食醋的体积/mL | 所用氢氧化钠溶液的体积/mL | |
| 第一次 | 20.00 | 19.8 |
| 第二次 | 20.00 | 21.2 |
| 第三次 | 20.00 | 19.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一个${\;}_{88}^{226}$Ra原子中含有138个中子 | |
| B. | Ra元素位于元素周期表中第六周期ⅡA族 | |
| C. | Ra不能和冷水反应置换氢气 | |
| D. | Ra(OH)2是一种两性氢氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 KHSO4、BaCl2、Na2CO3、FeSO4和氯水五种溶液,有如图所示的相互反应,图中每条连线两端的物质可以发生化学反应.下列说法不合理的是( )
KHSO4、BaCl2、Na2CO3、FeSO4和氯水五种溶液,有如图所示的相互反应,图中每条连线两端的物质可以发生化学反应.下列说法不合理的是( )| A. | X可能为KHSO4 | B. | M不可能是BaCl2 | C. | Y一定为Na2CO3 | D. | N可能是FeSO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一定含有乙烯 | B. | 一定含有甲烷和乙烯 | ||
| C. | 一定含有甲烷 | D. | 无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| t/min | 1 | 4 | 8 | 11 |
| n(H2)/mol | 6 | 2.6 | 2 | 2 |
| A. | 该温度下,平衡常数K=0.5 | |
| B. | 反应进行4min时,V(C02)=0.45 mol/(L•min) | |
| C. | 反应进行到9min时,H2的转化率比8min时高 | |
| D. | 反应进行11min后,若增大容器内压强,CO2的转化率一定增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 醛基的结构简式:-CHO | B. | 溴乙烷的电子式: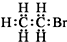 | ||
| C. | 乙炔分子的结构式:H-C≡C-H | D. | 乙醇的分子式:C2H6O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com