
����Ŀ��
��1��д��ͼ1����Ţ١������������ƣ���__����__����__����__���������١����У�ʹ��ǰ�������Ƿ�©ˮ����__����������ţ���
��2��ͼ2��ijѧУʵ���Ҵӻ�ѧ�Լ��̵���ص�Ũ�����Լ���ǩ�ϣ��ܶ�1.84 g��cm-3����������98%���IJ������ݣ����ø�Ũ��������480 mL 1 mol��L��1��ϡ���ᡣ�ɹ�ѡ�õ������У�
�ٽ�ͷ�ιܣ�����ƿ�����ձ�����ҩ�ף�����Ͳ����������ƽ��
��ش��������⣺
a��ͼ3��ʢ��Ũ������Լ�ƿ��ǩ��Ӧ��ӡ��ͼ��ʾ����е�__��д��Ǵ���A��D����
b������ϡ����ʱ������������������ȱ�ٵ�������__��__��д�������ƣ���
c�������㣬����480 mL 1 mol��L-1��ϡ���ᣬ��Ҫ����Ͳ��ȡ����Ũ��������Ϊ__mL������һλС���㣩��
���𰸡�Բ����ƿ ������ ��Һ©�� 100 mL ����ƿ �ۢ� D 500 mL����ƿ ������ 27.2
��������
��1����ͼʾ�����Ĺ����֪����ΪԲ����ƿ����Ϊ�����ܡ���Ϊ��Һ©������Ϊ100 mL����ƿ���ʴ�Ϊ��Բ����ƿ�������ܣ���Һ©����100 mL����ƿ��
��2��Բ����ƿ����������ʹ��֮ǰ����Ҫ����Ƿ�©ˮ������Һ©��������ƿ�ֱ���������ƿ����ʹ��ǰ��Ҫ��������Ƿ�©ˮ���ʴ�Ϊ���ۢܣ�
��3��a��Ũ������к�ǿ�ĸ�ʴ�ԣ�Ӧ������D����ʴƷ��ǣ��ʴ�Ϊ��D��
b������480mL��Һ����Ҫѡ��500mL����ƿ������ϡ������Һ�IJ���Ϊ�����㡢��ȡ��ϡ�͡���ȴ��ת�ơ�ϴ�ӡ����ݡ�ҡ�ȵȣ�ʹ�õ������У���Ͳ���ձ�����������500mL����ƿ����ͷ�ιܵȣ���ȱ�ٲ�������500mL����ƿ���ʴ�Ϊ����������500mL����ƿ��
c��ͼ2��Ũ��������ʵ���Ũ��Ϊ��![]() mol/L=18.4 mol/L������480mL1mol/L��ϡ���ᣬʵ�������Ƶ���500mL1mol/L��ϡ���ᣬ��ҪŨ��������Ϊ��V=
mol/L=18.4 mol/L������480mL1mol/L��ϡ���ᣬʵ�������Ƶ���500mL1mol/L��ϡ���ᣬ��ҪŨ��������Ϊ��V=![]() ��0.0272L=27.2mL���ʴ�Ϊ��27.2��
��0.0272L=27.2mL���ʴ�Ϊ��27.2��


 ���⿼����Ԫ���Ծ�ϵ�д�
���⿼����Ԫ���Ծ�ϵ�д� ��У���˳�̾�ϵ�д�
��У���˳�̾�ϵ�д� ��У���һ��ͨϵ�д�
��У���һ��ͨϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������������ɴ�ѧ��һ�����о�������һ����ΪEIDD2801����ҩ�����ı�ҽ�������¹ڷ��ķ�ʽ����Ч���ٷ����ˡ���ṹʽ��ͼ��
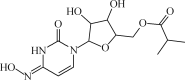
�����й�EIDD2801��˵����ȷ����(����)
A.EIDD2801���ڷ����廯����
B.EIDD2801����5������̼ԭ��
C.EIDD2801�ܺ�NaOH��Һ��Ӧ
D.EIDD2801����ʹ���Ը��������Һ��ɫ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ������������Ʒ����140 mL 5 mol��L��1������ǡ����ȫ�ܽ⣬������Һ������ͨ���0.56 L����(��״��)��Ӧ��ʹFe2��ȫ��ת��ΪFe3�������������Ϊ
A.Fe2O3B.Fe3O4C.Fe4O5D.Fe5O7
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧ��ȤС������NaI��Һ��ͨ������Cl2�õ������Һ�������ú����Һ��ȡNaI���壬ʵ���������£�

��֪��Ӧ����2I��+2Cu2++![]() +H2O
+H2O![]() 2CuI��+
2CuI��+![]() +2H+��
+2H+��
�ش��������⣺
��1������ʵ������Ҫ�IJ�����������ͨ©�����ձ���_____________��
��2����Ӧ����CuI����������ԭ����ֻ��NO2���÷�Ӧ�Ļ�ѧ����ʽΪ_________________������95.5 g CuI���뷴Ӧ������Ҫ�����______________L��O2���ܽ����ɵ�NO2��ˮ����ȫת��Ϊ���ᡣ
��3��������B�к�����Ԫ�أ���ԭ������һ��Ԫ��ԭ�ӵ����ʵ���֮��Ϊ3��8������B�Ļ�ѧʽΪ_____________��
��4����Ӧ�������ɺ�ɫ�������ɫ���壬��ɫ������׳�Ϊ��������������Ӧ���Ļ�ѧ����ʽΪ______��
��5����������Cl2ͨ�뺬12 g NaI����Һ�У�һ��ʱ������Һ���ɵõ����������Ϊ_________g��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��CO��N2O�������������������������Ӧ������������뷴Ӧ������ͼ��ʾ��
��һ����Fe*+N2O=FeO*+N2
�ڶ�����FeO*+CO=Fe*+CO2
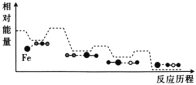
��������������ǣ� ��
A.Fe*�Ƿ�Ӧ�Ĵ���
B.������Ӧ����H��С��0
C.��һ����Ӧ�ȵڶ�����Ӧ��
D.�ܷ�ӦΪCO+N2O=N2+CO2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ������CO2������̼������ɱ�ĺ�ѹ�ܱ������з�Ӧ��C(s)��CO2(g)![]() 2CO(g)��ƽ��ʱ����ϵ����������������¶ȵĹ�ϵ����ͼ��ʾ��
2CO(g)��ƽ��ʱ����ϵ����������������¶ȵĹ�ϵ����ͼ��ʾ��
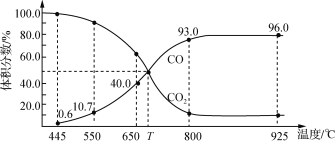
����˵����ȷ����
A.650 ��ʱ����Ӧ��ƽ���CO2��ת����Ϊ25.0%
B.550 ��ʱ��������������壬��(��)����(��)����С��ƽ�ⲻ�ƶ�
C.T ��ʱ��������������CO2��CO��ƽ�����淴Ӧ�����ƶ�
D.925 ��ʱ���˷�Ӧ��ƽ�ⳣ��K��2304�������¶Ȳ��䣬����С�����Kֵ����С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���¶�ΪTʱ����������ʼ�ݻ���Ϊ1 L�ĺ����ܱ�����������Ӧ��H2(g)��I2(g) ![]() 2HI(g)����H��0��ʵ���ã���������(H2)��������(I2)������k��c(H2)��c(I2)����������(HI)������k��c2(HI)��k����k��Ϊ���ʳ��������¶�Ӱ�졣����˵����ȷ����
2HI(g)����H��0��ʵ���ã���������(H2)��������(I2)������k��c(H2)��c(I2)����������(HI)������k��c2(HI)��k����k��Ϊ���ʳ��������¶�Ӱ�졣����˵����ȷ����
���� | ���ʵ���ʼŨ��(mol��L��1) | ���ʵ�ƽ��Ũ�� | ||
c(H2) | c(I2) | c(HI) | ||
��(����) | 0.1 | 0.1 | 0 | c(I2)��0.07 mol��L��1 |
��(��ѹ) | 0 | 0 | 0.6 | |
A.��ƽ��ʱ������������ͬʱ��ͨ��0.1 mol I2��0.1 mol HI�����ʱ����������
B.��������ƽ��ʱ��c(HI��������)��3c(HI��������)
C.��Ӧ�����У����������������е���ѹǿ֮��Ϊ3��1
D.�¶�һ�����������з�Ӧ�ﵽƽ��ʱ(ƽ�ⳣ��ΪK)����K��![]() ����
����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧƽ��������Ҫ�Ļ�ѧ��Ӧԭ��֮һ��
��1�������ݻ�Ϊ1L�ĺ��º����ܱ������������м���1molA�����1molB���������Ӧ��A(g)��B(g)![]() C(g) ��H=-qkJ��mol-1(q>0)��ts��Ӧ�ﵽƽ��״̬������0.5molC���壬�ų�����Q1kJ���ش��������⣺
C(g) ��H=-qkJ��mol-1(q>0)��ts��Ӧ�ﵽƽ��״̬������0.5molC���壬�ų�����Q1kJ���ش��������⣺
������������£�˵���÷�Ӧ�Ѿ��ﵽƽ��״̬����__������ţ���
A.����0.1molA��ͬʱ����0.1molC
B.�����������ѹǿ����ʱ����仯
C.������������ܶȲ���ʱ����仯
D.A��ת����Ϊ50%
�ڱ��������¶Ⱥ��ݻ����䣬����ʼʱ�������м���1molC���壬��Ӧ�ﵽƽ��ʱ����������Q2kJ����Q1��Q2��q����ֵ��ϵ��ȷ����___������ţ���
A.Q1��Q2=q B.Q1��2Q2<q C.Q1��2Q2>q D.Q1��Q2<q
����ԭƽ������ϣ����������¶Ⱥ��ݻ����䣬����������ͨ��amolA���壬���´�ƽ���B�����ת����Ϊ75%����a=__��
��2����һ�ݻ��ɱ���ܱ������г���10molCO��20molH2������CO(g)+2H2(g)![]() CH3OH(g)��Ӧ��CO��ƽ��ת����(��)���¶�(T)��ѹǿ(p)�Ĺ�ϵ��ͼ��ʾ��
CH3OH(g)��Ӧ��CO��ƽ��ת����(��)���¶�(T)��ѹǿ(p)�Ĺ�ϵ��ͼ��ʾ��

��A��B��C�����ƽ�ⳣ��KA��KB��KC�Ĵ�С��ϵΪ___��
�����ﵽƽ��״̬Aʱ�����������Ϊ8L������ƽ��״̬Bʱ���������Ϊ___L��
��3���Լ״�Ϊ��Ҫԭ�ϣ��绯ѧ�ϳ�̼��������Ĺ���ԭ����ͼ��ʾ�����Դ������Ϊ___������A������B������д�������ĵ缫��Ӧʽ___��
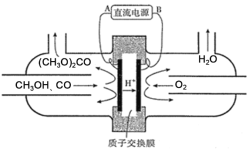
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���![]()
![]() ��Һ�ζ�
��Һ�ζ�![]()
![]()
![]() ��Һ����Һ
��Һ����Һ![]() �����
�����![]() ��Һ�������Ĺ�ϵ��ͼ��ʾ������˵���������( )
��Һ�������Ĺ�ϵ��ͼ��ʾ������˵���������( )
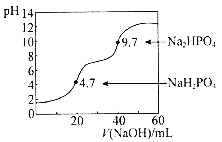
A.��![]() ʱ��
ʱ��![]()
B.��![]() ʱ��
ʱ��![]()
C.��![]() ʱ��
ʱ��![]()
D.��![]() ʱ��
ʱ��![]()
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com