
| A. | C3H7Cl | B. | C2H6O | C. | CH2Cl2 | D. | C3H6 |
分析 化学式若只能表示一种物质,则该化学式必须无同分异构体.而同分异构体是分子式相同,但结构不同的化合物,根据是否存在同分异构体判断正误.
解答 解:A.C3H7Cl可以存在同分异构体,CH3CH2CH2Cl,CH3CHClCH3,所以不能只表示一种物质,故A错误;
B.C2H6O可以存在同分异构体,可以是CH3CH2OH,CH3OCH3,所以不能只表示一种物质,故B错误;
C.CH2Cl2只有一种结构不存在同分异构体,所以能只表示一种物质,故C正确;
D.C3H6可以是丙烯,还可能是环丙烷,所以不能只表示一种物质,故D错误.
故选C.
点评 本题考查同分异构体,难度不大,注意化学式表示一种物质一定不存在同分异构体.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | (CH3)2CHCH2CH2C(CH3)3 | B. | CH3CH2C(CH3)2CH2C(CH3)2CH2CH3 | ||
| C. | CH3CH2C(CH3)2C(CH3)2CH2CH3 | D. | CH3CH(CH3)C(CH3)2CH2C(CH3)3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HCO3-+H2O?H3O++CO32- | B. | HCO3-+OH-=H2O+CO32- | ||
| C. | HCO3-+H2O?H2CO3+OH- | D. | HCO3-+H3O+=2H2O+CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. |  图甲表示一定温度下FeS和CuS的沉淀溶解平衡曲线,则Ksp(FeS)>Ksp(CuS) | |
| B. |  图乙表示pH=2的甲酸与乙酸溶液稀释时的pH变化曲线,则酸性:甲酸<乙酸 | |
| C. | 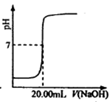 图丙表示用0.1000 mol•L-1NaOH溶液滴定25.00 mL盐酸的滴定曲线,则 c(HCl)=0.0800 mol•L-1 | |
| D. |  图丁表示反应N2(g)+3H2(g)?2NH3(g)平衡时NH3体积分数随起始<“m“:math dsi:zoomscale=150 dsi:_mathzoomed=1>n(N2)n(H2)$\frac{{n(N}_{2})}{n({H}_{2})}$变化的曲线,则转化率:αA(H2)=αB(H2) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 短周期元素是指1~20号元素 | |
| B. | 核素的种类和元素的种类一样多 | |
| C. | 元素周期表中共有18列、16个族 | |
| D. | 主族元素的最高正价均等于其族序数 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 32克O2和O3组成的混合气体中含有的氧原子数目为2NA | |
| B. | 常温常压下,22.4 L乙醇含有的分子数目为NA | |
| C. | 1 mol Na变为Na+时得到的电子数目为NA | |
| D. | 1mol/L NaCl溶液中含有Na+个数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com