
“毒胶囊”泛指利用由工业皮革废料为原料生产的含重金属铬(Cr)超标的胶囊,其中含有可能引起人体肾伤害的+6 价的铬.下列铬的化合物中铬呈+6 价的是( )
A.Cr2(SO4)3 B.Cr2O3 C.K2Cr2O7 D.Cr(OH)3
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案科目:高中化学 来源:2016-2017学年河北省高二上9.4周考化学卷(解析版) 题型:选择题
下列物质中可用于治疗胃酸过多的是( )
A.碳酸钠 B.氢氧化铝 C.氧化钙 D.碳酸钡
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省高二上入学考试化学试卷(解析版) 题型:选择题
下列叙述正确的是
A. 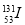 放出射线是一个自发的化学变化过程, 射线对人危害很大
放出射线是一个自发的化学变化过程, 射线对人危害很大
B.不同元素的原子构成的分子只含极性共价键
C. H2和T2是两种不同的物质,互称为同位素
H2和T2是两种不同的物质,互称为同位素
D.短周期第ⅣA与ⅦA族元素的原子间构成的分子,均满足原子最外层8电子结构
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省成都市高一入学考试化学卷(解析版) 题型:选择题
有甲、乙、丙、丁四种溶液,乙与丙混合产生的沉淀不溶于甲,乙与丁混合产生的沉淀可溶于甲。则该溶液组是( )

查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省成都市高一入学考试化学卷(解析版) 题型:选择题
将一严重锈蚀而部分变成铜绿[Cu2(OH)2CO3 ]的铜块研磨成粉末,在空气中充分灼烧成CuO,固体质量的变化情况可能是( )
A.增重30% B.一定增加 C.可能不变 D.减轻30%
查看答案和解析>>
科目:高中化学 来源:2017届广西省等三校高三上8月联考化学卷(解析版) 题型:填空题
【化学—选修3 物质结构与性质】
周期表中前四周期元素R、W、X、Y、Z的原子序数依次递增。R基态原子中,电子占据的最高能层符号为L,最高能级上只有两个自旋方向相同的电子。工业上通过分离液态空气获得X单质。Y原子的最外层电子数与电子层数之积等于R、W、X三种元素的原子序数之和。Z基态原子的最外能层只有一个电子,其他能层均已充满电子。请回答下列问题:
(1)Z2+基态核外电子排布式为: 。
(2)YX4-的空间构型是:__________;与YX4-互为等电子体的一种分子为__________(填化学式);HYX4酸性比HYX2强,其原因是:__________________________。
(3)结构简式为RX(WH2)2的化合物中R原子的杂化轨道类型为: ;1molRX(WH2)2分子中含有σ键数目为:_______________。(H为氢元素,下同)
(4)往Z的硫酸盐溶液中通入过量的WH3,可生成[Z(WH3)4]SO4,下列说法正确的是:__________。
A.[Z(WH3)4]SO4中所含的化学键有离子键、极性键和配位键
B.在[Z(WH3)4]2+中Z2+给出孤对电子,WH3提供空轨道
C.[Z(WH3)4]SO4组成元素中第一电离能最大的是氧元素
(5)某Y与Z形成的化合物的晶胞如右图所示(黑点代表Z原子)。

①该晶体的化学式为: 。
②已知Z和Y的电负性分别为1.9和3.0,则Y与Z形成的化合物属于 (填“离子”、“共价”)化合物。
③ 已知该晶体的密度为ρg·cm-3,阿伏加德罗常数为NA,则该晶体中Z原子和Y原子之间的最短距离为: cm(只写计算式)(Z原子位于体对角线上)。
查看答案和解析>>
科目:高中化学 来源:2017届广西省等三校高三上8月联考化学卷(解析版) 题型:选择题
工业上可由乙苯生产苯乙烯: ,下列说法正确的是
,下列说法正确的是
A. 可用酸性高锰酸钾溶液鉴别乙苯和苯乙烯
B. 苯乙烯能使溴水褪色,原因是两者发生了氧化反应
C. 该反应的反应类型为消去反应
D. 乙苯和苯乙烯分子内共平面的碳原子数最多均为7
查看答案和解析>>
科目:高中化学 来源:2017届北京市央民族大学附高三上9.12周练化学卷(解析版) 题型:实验题
侯德榜是我国著名科学家,1933年出版《纯碱制造》一书,创立了中国自己的制碱工艺。其纯碱制造原理如下图所示:
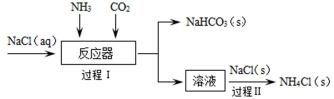
(1)由NaHCO3制备纯碱的化学方程式是_________________。
(2)过程Ⅰ通入NH3和CO2的顺序是__________________。
(3)过程Ⅱ析出NH4Cl(s)的原因是_____________。
(4)充分利用副产品NH4Cl生产NH3和HCl。直接加热分解NH4Cl,NH3和HCl的产率往往很低,原因是________________。
(5)采用MgO循环分解NH4Cl。加热,在300℃以下获得NH3;继续加热至350℃~600℃获得HCl气体。利用下列装置(加热及加持装置略)可测量NH3和HCl的产率。
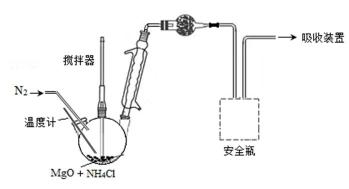
① 低于300℃时,干燥管盛装的干燥剂是_________。NH3吸收完全后,更换干燥剂和吸收装置中的吸收液。
② 产生NH3的化学反应方程式是_________________。
③ 在350℃~600℃,上图虚线框内应选择的安全瓶是________。

④ MgO可以循环分解NH4Cl制得NH3和HCl的原因是____________(结合化学方程式解释)。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年云南省高二上起点考试化学卷(解析版) 题型:选择题
时钟反应或振荡反应提供了迷人课堂演示实验,也是一个活跃的研究领域。测定含有I—浓度很小的碘化物溶液时,利用振荡反应进行化学放大,以求出原溶液中碘离子的浓度。
主要步骤如是:
①在中性溶液中,用溴将试样中I-氧化成IO3-,将过量的溴除去。
②再加入过量的KI,在酸性条件下,使IO3-完全转化成I2。
③将②中生成的碘完全萃取后,用肼将其还原成I-,方程式为:N2H4+2I2=4I-+N2+4H+
④将生成的I-萃取到水层后用①法处理。
⑤将④得到的溶液加入适量的KI溶液,并用硫酸酸化。
⑥将⑤反应后的溶 液以淀粉作指示剂,用Na2S2O3标准溶液滴定,方程式为:2Na2S2O3+I2=Na2S4O6+2NaI
液以淀粉作指示剂,用Na2S2O3标准溶液滴定,方程式为:2Na2S2O3+I2=Na2S4O6+2NaI
经过上述放大后,溶液中I-浓度放大为原溶液中I-浓度的(设前后溶液体积相等)( )
A.2倍 B.4倍 C.36倍 D.16倍
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com