
利用下图所示实验装置进行实验可以研究CO的还原性。

请填写下列空白:
(1)从A的长颈漏斗应加入的试剂是____________(填序号)
A.稀硫酸 B.浓硫酸 C.稀盐酸 D.浓硝酸
(2)装置B中最适宜的试剂是_________________。
(3)装置D中发生反应的化学方程式是_________________
(4)装置E中发生的现象是__________________________________。
(5)必须用装置C吸收除去气体中水蒸气的理由主要是_____________________。
(6)若根据F中澄清石灰水变浑浊的现象也能确认CO具有还原性,则应在原图所示装置____________与___________之间连接上下图的哪一种装置__________(填写序号)。目的是 _______________;
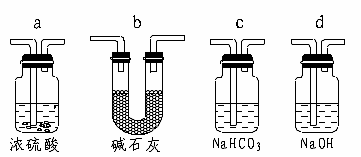
(7)由F装置排出的尾气需要点燃的原因是__________________________________。
科目:高中化学 来源: 题型:阅读理解

查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解

| 实验 序号 |
实验操作 | 现象 | 结论 |
| Ⅰ | 将氯水滴入品红溶液 | 溶液褪色 | 氯气与水反应的产物有漂白性 |
| Ⅱ | 氯水中加入碳酸氢钠粉末 | 有无色气 泡产生 |
氯气与水反应的产物具有酸性 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 实验序号 | 实验操作 | 现象 | 结论 |
| Ⅰ | 将氯水滴入品红溶液 | 溶液褪色 | 氯气与水反应的产物有漂白性 |
| Ⅱ | 氯水中加入 NaHCO3粉末 | 有无色气泡产生 | 氯气与水反应的产物具有较强的酸性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
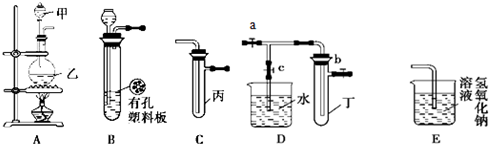
某化学兴趣小组的同学利用下图所示实验装置进行实验(图中a、b、c表示止水夹)。
(1)请利用上述装置设计一个简单的实验验证Cl—和Br—的还原性强弱。
①选择合理的装置连接: → → 。(填字母编号)
②从下列提供的试剂选择你所需的试剂: 。(填字母编号)
a. 固体氯化钠 b. 固体二氧化锰 c. 浓硫酸
d. 浓盐酸 e. 稀盐酸 f. 溴化钠溶液
③实验现象及结论: 。
(2)B、D、E装置相连后,在B中盛装浓硝酸和铜片(放在有孔塑料板上),可制得NO2并进行有关实验,其操作步骤为
①先关闭止水夹 ,再打开止水夹 ,使NO2充满试管乙。接着关闭止水夹 ,打开止水夹 ,最后微热试管乙,使烧杯中的水倒流进入试管乙。
②试管乙中的NO2与水充分反应后,若向试管内缓缓通入一定量的O2,直至试管 全部充满水,则所得溶液中溶质的物质的量浓度是 (气体按标准状况计算)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com