
 ŅŃÖŖĒ¦Šīµē³ŲµÄ·“Ó¦ŌĄķŹĒ£ŗPb£Øs£©+PbO2£Øs£©+2H2SO4£Øaq£©ØT2PbSO4£Øs£©+2H2O£Øl£©”÷H£¼0Ķ¼ĪŖĒ¦Šīµē³ŲµÄŹ¾ŅāĶ¼£®ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©
ŅŃÖŖĒ¦Šīµē³ŲµÄ·“Ó¦ŌĄķŹĒ£ŗPb£Øs£©+PbO2£Øs£©+2H2SO4£Øaq£©ØT2PbSO4£Øs£©+2H2O£Øl£©”÷H£¼0Ķ¼ĪŖĒ¦Šīµē³ŲµÄŹ¾ŅāĶ¼£®ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©| A£® | ³äµēŹ±£¬Ńō¼«µÄµē¼«·“Ó¦Ź½ĪŖ£ŗPbSO4+2e-ØTPb+SO42- | |
| B£® | ³äµēŹ±£¬ČōNĮ¬½ÓµēŌ“Õż¼«£¬ŌņøĆ¼«Éś³ÉPbO2 | |
| C£® | ·ÅµēŹ±£¬c£ØH2SO4£©²»±ä£¬Į½¼«µÄÖŹĮæŌö¼Ó | |
| D£® | ·ÅµēŹ±£¬NĪŖøŗ¼«£¬Ęäµē¼«·“Ó¦Ź½ĪŖ£ŗPbO2+SO42-+4H++2e-ØTPbSO4+2H2O |
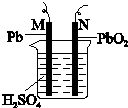
·ÖĪö ÓÉ×Ü·½³ĢŹ½æÉÖŖ£¬ĪŖŌµē³ŲŹ±£¬PbĪŖøŗ¼«£¬·¢ÉśŃõ»Æ·“Ó¦£¬µē¼«·½³ĢŹ½ĪŖPb+SO42--2e-=PbSO4£¬PbO2ĪŖÕż¼«£¬·¢Éś»¹Ō·“Ó¦£¬µē¼«·½³ĢŹ½ĪŖPbO2+4H++SO42--2e-=2H2O+PbSO4£¬ŌŚ³äµēŹ±£¬Ņõ¼«·¢ÉśµÄ·“Ó¦ŹĒPbSO4+2e-=Pb+SO42-£¬Ńō¼«·“Ó¦ĪŖPbSO4-2e-+2H2O=PbO2+SO42-+4H+£¬½įŗĻµē¼«·½³ĢŹ½½ā“šøĆĢā£®
½ā“š ½ā£ŗA£®³äµēŹ±£¬Ńō¼«·¢ÉśŃõ»Æ·“Ó¦£¬Ńō¼«·“Ó¦ĪŖPbSO4-2e-+2H2O=PbO2+SO42-+4H+£¬¹ŹA“ķĪó£»
B£®³äµēŹ±£¬ČōNĮ¬½ÓµēŌ“Õż¼«£¬ŌņN¼«ŹĒŃō¼«£¬øƵē¼«ÉĻŹĒĮņĖįĒ¦Ź§µē×Ó·¢ÉśŃõ»Æ·“Ó¦£¬Éś³ÉPbO2£¬¹ŹBÕżČ·£»
C£®ÓÉ·½³ĢŹ½Pb£Øs£©+PbO2£Øs£©+2H2SO4£Øaq£©ØT2PbSO4£Øs£©+2H2O£Øl£©æÉÖŖ£¬·ÅµēŹ±£¬c£ØH2SO4£©¼õŠ”£¬Į½¼«¶¼²śÉśĮņĖįĒ¦£¬µē¼«µÄÖŹĮæŌö¼Ó£¬¹ŹC“ķĪó£»
D£®µē³Ų·ÅµēŹ±£¬Õż¼«·¢Éś»¹Ō·“Ó¦£¬·“Ó¦·½³ĢŹ½ĪŖ£ŗPbO2+2e-+4H++SO42-=PbSO4+2H2O£¬NĪŖÕż¼«£¬¹ŹD“ķĪó£»
¹ŹŃ”B£®
µćĘĄ ±¾Ģāæ¼²éŌµē³ŲŗĶµē½ā³ŲÖŖŹ¶£¬²ąÖŲӌѧɜµÄ·ÖĪöÄÜĮ¦ŗĶµē»ÆѧÖŖŹ¶µÄ×ŪŗĻ漲飬ĪŖøßæ¼³£¼ūĢāŠĶŗĶøßĘµæ¼µć£¬×¢Ņā°ŃĪÕµē½ā·½³ĢŹ½µÄŹéŠ“£¬ÄŃ¶Č²»“ó£®


 ½ĢѧĮ·ŠĀĶ¬²½Į·Ļ°ĻµĮŠ“š°ø
½ĢѧĮ·ŠĀĶ¬²½Į·Ļ°ĻµĮŠ“š°ø æĪĒ°æĪŗóĶ¬²½Į·Ļ°ĻµĮŠ“š°ø
æĪĒ°æĪŗóĶ¬²½Į·Ļ°ĻµĮŠ“š°ø æĪĢĆŠ”×÷ŅµĻµĮŠ“š°ø
æĪĢĆŠ”×÷ŅµĻµĮŠ“š°ø »ĘøŌŠ”דŌŖæŚĖćĖŁĖćĮ·Ļ°²įĻµĮŠ“š°ø
»ĘøŌŠ”דŌŖæŚĖćĖŁĖćĮ·Ļ°²įĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | µāĖ®£¬±äĄ¶É«£»ÅØĻõĖį£¬±ä»ĘÉ«£»ŠĀÖĘCu£ØOH£©2£¬×©ŗģÉ«³Įµķ | |
| B£® | ÅØĻõĖį£¬±ä»ĘÉ«£»ŠĀÖĘCu£ØOH£©2£¬×©ŗģÉ«³Įµķ£»µāĖ®£¬±äĄ¶É« | |
| C£® | ŠĀÖĘCu£ØOH£©2£¬×©ŗģÉ«³Įµķ£»µāĖ®£¬±äĄ¶É«£»ÅØĻõĖį£¬±ä»ĘÉ« | |
| D£® | µāĖ®£¬±äĄ¶É«£»ŠĀÖĘCu£ØOH£©2£¬×©ŗģÉ«³Įµķ£»ÅØĻõĖį£¬±ä»ĘÉ« |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | CH4 | B£® | C2H4 | C£® | C6H14 | D£® | C2H2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | CµÄĢå»ż·ÖŹż²»ŌŁ·¢Éśøıä | |
| B£® | A”¢B”¢CµÄĪļÖŹµÄĮæÅضČĻąµČ | |
| C£® | A”¢B”¢CµÄĪļÖŹµÄĮæÖ®±ČĪŖ1£ŗ3£ŗ2 | |
| D£® | µ„Ī»Ź±¼äÉś³Én mol A£¬Ķ¬Ź±Éś³É3n mol B |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ±źæöĻĀ£¬2.24LHFÖŠĖłŗ¬µē×ÓŹżĪŖ0.1NA | |
| B£® | ³£ĪĀ³£Ń¹ĻĀ£¬4.4 gŅŅČ©Ėłŗ¬¦Ņ¼üŹżÄæĪŖ0.7NA | |
| C£® | 3 molµ„ÖŹFeĶźČ«×Ŗ±äĪŖFe3O4£¬Ź§Č„8 NAøöµē×Ó | |
| D£® | 1 mol Na2O2¹ĢĢåÖŠŗ¬Ąė×Ó×ÜŹżĪŖ4NA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĻõĖįŅųČÜŅŗÖŠ¼ÓČėĶ·Ū£ŗAg++CuØTCu2++Ag | |
| B£® | Ba£ØOH£©2ÓėĻ”H2SO4·“Ó¦£ŗBa2++OH-+H++SO42-ØTBaSO4”ż+H2O | |
| C£® | Ļņ³ĪĒåŹÆ»ŅĖ®ÖŠĶØČė×ćĮ涞Ńõ»ÆĢ¼£ŗOH-+CO2ØTHCO3- | |
| D£® | Ģ¼ĖįøĘČÜÓŚ“×ĖįÖŠ£ŗCaCO3+2H+ØTCa2++2H2O+CO2”ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¾ßÓŠ½ĻøßÄÜĮæµÄ·Ö×ÓŹĒ»ī»Æ·Ö×Ó | |
| B£® | »ī»Æ·Ö×Ó¼äµÄÅöײŅ»¶ØŹĒÓŠŠ§Åöײ | |
| C£® | ²»Ķ¬»Æѧ·“Ó¦ŠčŅŖµÄ»ī»ÆÄÜÓŠæÉÄܲī±šŗÜ“ó | |
| D£® | ·“Ó¦µÄ»ī»ÆÄܓ󊔲»»įÓ°Ļģ»Æѧ·“Ó¦ĖŁĀŹ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com