
 �봼�γɵ���������Ҫ�����л��ϳɡ�ʳƷ����ױƷ��ҽҩ��ɱ����������Ҳ���������Ϸ�����������˵������ȷ���ǣ�������
�봼�γɵ���������Ҫ�����л��ϳɡ�ʳƷ����ױƷ��ҽҩ��ɱ����������Ҳ���������Ϸ�����������˵������ȷ���ǣ�������| A���Ჴ��������NaOH��Һ��Ӧʱ��������1mol NaOH |
| B���Ჴ���������ӽṹ�У�������6��̼ԭ����һ��ƽ���� |
| C���Ჴ����������4mol H2�����ӳɷ�Ӧ |
D���Ჴ�������ɶ��ǻ���������1-�����γɵ������ṹ��ʽ��ͼ��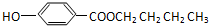 |
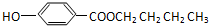 ����D��ȷ��
����D��ȷ��

 ��ѧ�����ϵ�д�
��ѧ�����ϵ�д� �·Ƿ��̸����100��ϵ�д�
�·Ƿ��̸����100��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��S��s��+O2��g��=SO2��g������H=-297.23kJ?mol-1 |
| B��2H2��g��+O2��g��=2H2O��1������H=-571.6 kJ |
| C��CaCO3��s��=CaO��s��+CO2��g������H=178.5 kJ?mol |
| D��Zn+CuSO4��aq��=ZnSO4��aq��+Cu����H=-216kJ?mol-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

| A���û������ܷ�����ȥ��Ӧ |
| B��1mol�û�������NaOH��Һ��ȫ��Ӧ����������6moINaOH |
| C���û������ܺ����CCl4��Һ�����ӳɷ�Ӧ |
| D���û�������ϡ���������ˮ�����ò���֮һ�ɷ�����ȥ��Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ������ŵ����һ���˷ܼ����ṹ��ʽ��ͼ���йظ����ʵ�˵����ȷ���ǣ�������
������ŵ����һ���˷ܼ����ṹ��ʽ��ͼ���йظ����ʵ�˵����ȷ���ǣ�������| A����ʹ������Ȼ�̼��Һ��ɫ |
| B��1mol������������6molH2�����ӳɷ�Ӧ |
| C�������ʽΪC27H32O3 |
| D����NaOH��Һ��ˮ�������������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
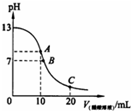 25��ʱ����20ml 0.1mol?L-1NaOH��Һ����μ���0.2mol?L-1������Һ��������ͼ��ʾ���й�����Ũ�ȹ�ϵ�ıȽ��У�����ȷ���ǣ�������
25��ʱ����20ml 0.1mol?L-1NaOH��Һ����μ���0.2mol?L-1������Һ��������ͼ��ʾ���й�����Ũ�ȹ�ϵ�ıȽ��У�����ȷ���ǣ�������| A����A�㣺c��Na+����c��CH3COO-����c��OH-����c��H+�� |
| B����B�㣺c��Na+��=c��CH3COO-����c��OH-��=c��H+�� |
| C����C�㣺c��Na+��+c��H+��=c��CH3COO-��+c��OH-�� |
| D����C�㣺c��Na+��=c��CH3COO-��+c��CH3COOH�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��ǿ����ʺ�������ʵı����������ڵ���̶ȵIJ�ͬ |
| B��������Һ�м�û��H+Ҳû��OH- |
| C��pH=4����Һϡ��10000�������Ϊ������Һ |
| D������Һ�м�������������ʱ����Һ��pH�����������仯 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
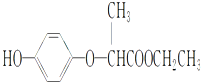
| A��1 mol HPE�����Ժ�2 mol NaOH��Ӧ |
| B��HPE���ܸ�Ũ��ˮ��Ӧ |
| C��HPE��1H�˴Ź���������8�ַ� |
| D�������ʲ��ܷ����ڼӳɷ�Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ʵ���� | �� | �� | �� | �� |
| ϡ�������/mL | 100 | 200 | 300 | 400 |
| ʣ���������/g | 9.0 | 4.8 | 0 | 0 |
| NO���/L | 1.12 | 2.24 | 3.36 | V |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com