
一只规格为a mL的滴定管,其尖嘴部分充满溶液,管内液面在m mL处,当液面降到n mL处时,下列判断正确的是
A.流出溶液的体积为(m-n) mL B.流出溶液的体积为(n-m) mL
C.管内溶液体积等于(a-n) mL D.管内溶液体积多于n mL
科目:高中化学 来源:2016届河南省八市高三9月教学质量监测考试化学试卷(解析版) 题型:选择题
已知常温下Ksp(AgCl)=1.8×l0-10,Ksp(AgBr)=5×10 -13,下列有关说法错误的是
A.在饱和AgCl、AgBr的混合溶液中: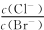 = 360
= 360
B.向AgCl悬浊液中滴加浓NaBr溶液会产生淡黄色沉淀
C.AgCl在水中溶解度及Ksp均比在NaCl溶液中的大
D.欲用1 L NaCl溶液将0.01 mol AgBr转化为AgCl,则c(NaCl)≥3.61 mol/L
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川省雅安市高二9月月考化学试卷(解析版) 题型:选择题
下面的电子结构中,第一电离能最小的原子可能是
A.ns2np3 B.ns2np5 C.ns2np4 D.ns2np6
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北正定中学高二上学期第一次联考化学试卷(解析版) 题型:选择题
一定条件下,体积为10 L的密闭容器中,1 mol X和1 mol Y进行反应:
2X(g)+Y(g)? ?Z(g),经60 s达到平衡,生成0.3 mol Z。下列说法正确的是
?Z(g),经60 s达到平衡,生成0.3 mol Z。下列说法正确的是
A.以X浓度变化表示的反应速率为0.001 mol/(L·s)
B.将容器体积变为20 L,Z的平衡浓度变为原来的
C.若增大压强,则物质Y的转化率减小
D.若升高温度,X的体积分数增大,则该反应的ΔH>0
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北正定中学高二上学期第一次联考化学试卷(解析版) 题型:选择题
常温下0.1 mol·L-1氨水的pH=a,下列能使溶液pH=(a+1)的措施是
A.加入适量的氢氧化钠固体 B.将溶液稀释到原体积的10倍
C.加入等体积0.2 mol·L-1氨水 D.降低溶液的温度
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北大名县第一中学高二上学期第一次月考试化学试卷(解析版) 题型:选择题
下列对化学反应的认识正确的是
A.化学反应过程中,分子的种类和数目一定发生改变
B.如果某化学反应的△H和△S均小于0,则反应一定能自发进行
C.化学反应过程中,一定有化学键的断裂和形成
D.放热反应的反应速率一定比吸热反应的反应速率大
查看答案和解析>>
科目:高中化学 来源:2016届云南省高三上学期第一次月考化学试卷(解析版) 题型:选择题
在含有Cu(NO3)2、Zn(NO3)2、Fe(NO3)3、AgNO3各0.1 mol的混合溶液中加入0.1 mol铁粉,充分搅拌后铁完全反应,溶液中不存在Fe3+,同时析出0.1 mol Ag。则下列结论中不正确的是
A.反应后溶液中Cu2+与Fe2+的物质的量之比为1∶2
B.氧化性:Ag+>Cu2+>Fe3+>Zn2+
C.含Fe3+的溶液可腐蚀铜板
D.1 mol Fe可还原2 mol Fe3+
查看答案和解析>>
科目:高中化学 来源:2016届甘肃省张掖市高三上学期第一次质量检测化学试卷(解析版) 题型:填空题
〔化学——选修3:物质结构与性质〕举世瞩目的中国探月工程三期再入返回试验器于2014年10月24日凌晨成功发射,为实现月球采样和首次地月往返踏出了成功的第一步。探月工程三期的主要目标是实现无人自动采样返回,突破月面采样、月面上升、月球轨道交会对接等核心关键技术。已知所用火箭推进剂为肼(N2H4)和过氧化氢(H2O2),火箭箭体一般采用钛合金材料。
请回答下列问题:
(1)N2H4、H2O2分子中电负性最大的元素在周期表中的位置为 ,第一电离能最大的元素为 。
(2)钛的原子序数为22,其基态电子排布式示意图为 。
(3)1 mol N2H4分子中含有的键数目为 。
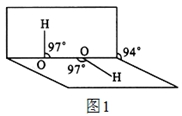
(4)H2O2分子结构如图1,其中心原子杂化轨道为 ,估计它难溶于CS2,简要说明原因 。
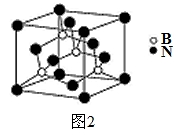
(5)氮化硼其晶胞如图2所示,则处于晶胞顶点上的原子的配位数为 ,若立方氮化硼的密度为g·cm-3,阿伏加德罗常数为NA,则两个最近N原子间的距离为________cm。
查看答案和解析>>
科目:高中化学 来源:2016届天津一中高三零月考化学试卷(解析版) 题型:填空题
碳、氮及其化合物在工农业生产生活中有着重要作用。请回答下列问题:
(1)用CH4 催化还原NOx 可以消除氮氧化物的污染。例如:
CH4(g) + 4NO2(g) = 4NO(g)+CO2(g) + 2H2O(g) ΔH1=-574 kJ·mol-1
CH4(g) + 4NO(g) = 2 N2(g)+CO2(g) + 2H2O(g) ΔH2
若2 mol CH4 还原NO2 至N2,整个过程中放出的热量为1734 kJ,则ΔH2= ;
(2)据报道,科学家在一定条件下利用Fe2O3与甲烷反应可制取“纳米级”的金属铁。其反应如下: Fe2O3(s) + 3CH4(g)  2Fe(s) + 3CO(g) +6H2(g) ΔH>0
2Fe(s) + 3CO(g) +6H2(g) ΔH>0
① 若反应在5L的密闭容器中进行,1min后达到平衡,测得Fe2O3在反应中质量减少3.2g。则该段时间内CO的平均反应速率为 ________________ 。
② 若该反应在恒温恒压容器中进行,能表明该反应达到平衡状态的是_____(选填序号)
a.CH4的转化率等于CO的产率
b.混合气体的平均相对分子质量不变
c.v(CO)与v(H2)的比值不变
d.固体的总质量不变
③ 该反应达到平衡时某物理量随温度变化如图所示,当温度由T1升高到T2时,平衡常数KA ______KB(填“>”、“ <”或“=”)。纵坐标可以表示的物理量有哪些 。
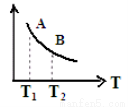
a.H2的逆反应速率
b.CH4的的体积分数
c.混合气体的平均相对分子质量
(3)若往20mL 0.0lmol·L-l的弱酸HNO2溶液中逐滴加入一定浓度的烧碱溶液,测得混合溶液的温度变化如图所示,下列有关说法正确的是________
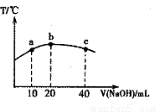
①该烧碱溶液的浓度为0.02mol·L-1
②该烧碱溶液的浓度为0.01mol·L-1
③ HNO2的电离平衡常数:b点>a点
④从b点到c点,混合溶液中一直存在:c(Na+)>c(NO2-)>c(OH )> c(H+)
)> c(H+)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com