
下列电离方程式正确的是( )
|
| A. | H2SO4=2H++S6++4O2﹣ | B. | H2CO3=2H++CO32﹣ |
|
| C. | Ba(OH)2=Ba2++2OH﹣ | D. | Na2CO3=Na2++CO32﹣ |
考点:
电离方程式的书写.
专题:
电离平衡与溶液的pH专题.
分析:
强电解质的电离用“═”,弱电解质的电离用“⇌”,弱酸的电离分步进行,以第一步为主,遵循电荷守恒及质量守恒定律,并注意原子团不可拆分,以此来解答.
解答:
解:A.H2SO4为强电解质,电离方程式为H2SO4=2H++SO42﹣,故A错误;
B.H2CO3为弱电解质,电离方程式为H2CO3⇌H++HCO3﹣,故B错误;
C.Ba(OH)2为强电解质,电离方程式为Ba(OH)2=Ba2++2OH﹣,故C正确;
D.Na2CO3为强电解质,电离方程式为Na2CO3=2Na++CO32﹣,故D错误;
故选C.
点评:
本题考查电离方程式的书写,明确电解质的强弱及电离方程式遵循电荷守恒及质量守恒定律即可解答,易错点为学生忽略物质中的原子团.


科目:高中化学 来源: 题型:
一定条件下,在密闭容器中充入SO3,发生化学反应:2SO32SO2+O2,反应一段时间后,又向其中充入18O2,在重新达到化学平衡状态后,18O原子存在于( )
A.SO3中 B.SO2中
C.O2中 D.三种物质中都有
查看答案和解析>>
科目:高中化学 来源: 题型:
已知氢气在氯气中燃烧时产生苍白色火焰.在反应过程中,破坏1mol氢气中的化学键消耗的能量为Q1kJ,破坏1mol氯气中的化学键消耗的能量为Q2kJ,形成1mol氯化氢中的化学键释放的能量为Q3kJ,则下列关系式中一定正确的是( )
|
| A. | Q1+Q2<2Q3 | B. | Q1+Q2>2Q3 | C. | Q1+Q2<Q3 | D. | Q1+Q2=Q3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
NA表示阿伏加德罗常数的值,下列说法正确的是( )
|
| A. | 标准状况下,0.5NA个H2O分子所占体积约为11.2L |
|
| B. | 20g重氧水(H218O)中含有的中子数为8NA |
|
| C. | 在铁与氯气的反应中,1mol铁失去的电子数为2NA |
|
| D. | 常温常压下,16gO2和16gO3所含氧原子数都是NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
欲使0.1mol/L的NaHCO3溶液中c(H+)、c(CO32﹣)、c(HCO3﹣)都减少,其方法是( )
|
| A. | 通入二氧化碳气体 | B. | 加入氢氧化钠固体 |
|
| C. | 通入氯化氢气体 | D. | 加入饱和石灰水溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关实验的叙述,正确的是( )
|
| A. | 将固体加入容量瓶中溶解并稀释至刻度,配置成一定物质的量浓度的溶液 |
|
| B. | 某溶液与BaCl2溶液反应生成白色沉淀,说明原溶液中有SO42﹣ |
|
| C. | 用NaOH溶液洗涤并灼烧铂丝后,再进行焰色反应 |
|
| D. | 可以用湿润的淀粉KI试纸检验电解饱和食盐水的阳极产物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
有8 g Na2O2、Na2O、Na2CO3、NaOH的混合物与200 g质量分数为3.65%的盐酸恰好反应,蒸干溶液,最终得固体质量为 ( )
A.8 g B.15.5 g C.11.7 g D.无法计算
查看答案和解析>>
科目:高中化学 来源: 题型:
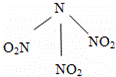
科学家最近研制出可望成为高效火箭推进剂的N(NO2)3(如图所示).已知该分子中N﹣N﹣N键角都是108.1°,下列有关N(NO2)3的说法正确的是( )
|
| A. | 分子中N、O间形成的共价键是非极性键 |
|
| B. | 分子中四个氧原子共平面 |
|
| C. | 该物质既有氧化性又有还原性 |
|
| D. | 15.2g该物质含有6.02×1022个原子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com