
| 选项 | 陈述I | 陈述Ⅱ |
| A | HClO具有强氧化性 | HClO有杀菌消毒作用 |
| B | 铝比铁活泼 | 铝比铁更容易被腐蚀 |
| C | 与水反应时,钠浮在水面上 | 钠与水反应是放热反应 |
| D | 浓硝酸具有强氧化性 | 浓硝酸能和浓氨水反应产生白烟 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.次氯酸具有强的氧化性,能够使蛋白质变性;
B.铝性质活泼,空气中容易被氧气氧化生成致密氧化膜,阻止反应继续进行;
C.钠的密度小于水;
D.依据浓硝酸的挥发性解答.
解答 解:A.次氯酸具有强的氧化性,能够使蛋白质变性,所以具有杀菌消毒作用,陈述Ⅰ、Ⅱ正确并且有因果关系,故A正确;
B.铝性质活泼,空气中容易被氧气氧化生成致密氧化膜,阻止反应继续进行,所以铝比铁耐腐蚀,陈述Ⅱ错误,故B错误;
C.钠的密度大于水,所以钠与水反应浮在水面,与反应放热无关,所以陈述Ⅰ、Ⅱ正确单身没有因果关系,故C错误;
D.浓硝酸的挥发性,能够与浓氨水反应生成硝酸铵白色固体,产生大量白烟,所以陈述Ⅰ、Ⅱ正确单身没有因果关系,故D错误;
故选:A.
点评 本题综合考查元素化合物知识,为高考常见题型,侧重于学生的分析能力和元素化合物知识的综合理解和运用的考查,注意相关基础知识的积累,难度不大.


 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
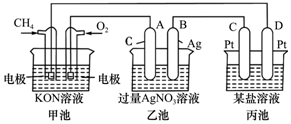 根据下列电化学装置,回答下列问题:
根据下列电化学装置,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验室制取氨气时,将尾气直接通入水中吸收 | |
| B. | 金属钠着火,立即用泡沫灭火器灭火 | |
| C. | 大量氯气泄漏时,迅速离开现场并尽量往高处去 | |
| D. | 皮肤上不慎沾上浓NaOH溶液,立即用盐酸冲洗 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向碳酸氢钠溶液中加入氢氧化钙溶液时,溶液没有浑浊 | |
| B. | 夏日的傍晚常常看到万丈霞光,该现象属于胶体的丁达尔效应 | |
| C. | 过氧化钠是一种强氧化剂,不可作为氧气来源 | |
| D. | 胶体和浊液的分散质都不能通过滤纸的孔隙 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NO的摩尔质量为30g | |
| B. | 常温常压下,14g一氧化碳所占体积为11.2 L | |
| C. | 等物质的量的Na2O2和Na2O中所含阴阳离子总数相等 | |
| D. | 设阿伏加德罗常数为NA,常温常压下O2与O3的混合物32g,含有分子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 在自行车的钢圈表面镀镍 | B. | 在地下钢铁管道上连接铜块 | ||
| C. | 改变金属内部结构制成不锈钢 | D. | 健身器村刷油漆或包上一层塑料层 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol FeCl3完全水解转化为氢氧化铁胶体后能生成NA个胶粒 | |
| B. | 0.1 L 3 mol•L-1的NH4NO3溶液中含有的NH4+数目为0.3×6.02×1023 | |
| C. | 5.6g铁粉与硝酸反应失去的电子数一定为0.3×6.02×1023 | |
| D. | 4.5gSiO2晶体中含有的硅氧键数目为0.3×6.02×1023 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com