

| ±ū·Ö×ÓŹ½ | C16H14O2 |
| ²æ·ÖŠŌÖŹ | ÄÜŹ¹Br2/CCl4ĶŹÉ« |
| ÄÜŌŚĻ”H2SO4ÖŠĖ®½ā |

 $”ś_{”÷}^{O_{2}/Cu}$Y$”ś_{¢ņ}^{Ņ»¶ØĢõ¼ž}$ŅŅ
$”ś_{”÷}^{O_{2}/Cu}$Y$”ś_{¢ņ}^{Ņ»¶ØĢõ¼ž}$ŅŅ £Ø×¢Ć÷·“Ó¦Ģõ¼ž£©£®
£Ø×¢Ć÷·“Ó¦Ģõ¼ž£©£®
 £®
£® £®
£® £®
£® ·ÖĪö £Ø1£©¼×ÖŠŗ¬ÓŠĢ¼Ģ¼Ė«¼üŗĶ“¼ōĒ»ł£¬ŅŅÖŠŗ¬ÓŠĢ¼Ģ¼Ė«¼üŗĶČ©»ł£»
£Ø2£©¼×ÖŠÓŠĢ¼Ģ¼Ė«¼ü£¬ÄÜ·¢Éś¼Ó¾Ū·“Ó¦£»
£Ø3£©ÓÉĪļÖŹµÄ½į¹¹æÉÖŖ£¬·“Ó¦¢ńŹĒ¼×ÖŠĢ¼Ģ¼Ė«¼üÓėHCl·¢Éś¼Ó³É·“Ӧɜ³É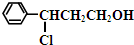 £¬Č»ŗó
£¬Č»ŗó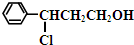 ÖŠ“¼ōĒ»ł·¢ÉśŃõ»Æ·“Ӧɜ³ÉYĪŖ
ÖŠ“¼ōĒ»ł·¢ÉśŃõ»Æ·“Ӧɜ³ÉYĪŖ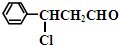 £¬·“Ó¦¢ņŹĒY·¢ÉśĀ±“śĢžµÄĻūČ„·“Ӧɜ³ÉŅŅ£»
£¬·“Ó¦¢ņŹĒY·¢ÉśĀ±“śĢžµÄĻūČ„·“Ӧɜ³ÉŅŅ£»
£Ø4£©ŅŅ·¢ÉśŠÅĻ¢ÖŠŃõ»Æ·“Ӧɜ³ÉAÓėB£¬Č©AŗĶÅØNaOH·“ӦȻŗóĖį»ÆµĆµ½E£¬½įŗĻŠÅĻ¢æÉÖŖAÉś³ÉōČĖįŗĶ“¼£¬¶ųEµÄĻą¶Ō·Ö×ÓÖŹĮæĪŖ76£¬ŌņAÖŠ²»æÉÄÜŗ¬ÓŠ±½»·£¬ŌņAĪŖOHC-CHO£¬EĪŖHOCH2COOH£¬BĪŖ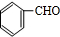 £¬FŹĒÓÉĮ½·Ö×ÓEÉś³ÉµÄĮłŌŖ»·£¬ŌņFĪŖ
£¬FŹĒÓÉĮ½·Ö×ÓEÉś³ÉµÄĮłŌŖ»·£¬ŌņFĪŖ £¬ŅŅÓėŠĀÖĘĒāŃõ»ÆĶ·¢ÉśŃõ»Æ·“Ó¦”¢Ėį»ÆÉś³ÉDĪŖ£¬ŌņDĪŖ
£¬ŅŅÓėŠĀÖĘĒāŃõ»ÆĶ·¢ÉśŃõ»Æ·“Ó¦”¢Ėį»ÆÉś³ÉDĪŖ£¬ŌņDĪŖ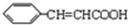 £¬±ūµÄ·Ö×ÓŹ½ĪŖC16H14O2£¬±ūÄÜŹ¹Br2/CCl2ĶŹÉ«ÄÜŌŚĻ”ĮņĖįÖŠĖ®½ā£¬ĖµĆ÷±ūÖŠÓŠĢ¼Ģ¼²»±„ŗĶ¼üŗĶõ„»ł£¬CÓėDŌŚÅØĮņĖį”¢¼ÓČČĢõ¼žÉś³É±ū£¬Ó¦ŹĒ·¢Éśõ„»Æ·“Ó¦£¬¹ŹBÓėĒāĘų·¢Éś¼Ó³É·“Ӧɜ³ÉCĪŖ
£¬±ūµÄ·Ö×ÓŹ½ĪŖC16H14O2£¬±ūÄÜŹ¹Br2/CCl2ĶŹÉ«ÄÜŌŚĻ”ĮņĖįÖŠĖ®½ā£¬ĖµĆ÷±ūÖŠÓŠĢ¼Ģ¼²»±„ŗĶ¼üŗĶõ„»ł£¬CÓėDŌŚÅØĮņĖį”¢¼ÓČČĢõ¼žÉś³É±ū£¬Ó¦ŹĒ·¢Éśõ„»Æ·“Ó¦£¬¹ŹBÓėĒāĘų·¢Éś¼Ó³É·“Ӧɜ³ÉCĪŖ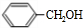 £¬±ūĪŖ
£¬±ūĪŖ £¬¾Ż“Ė½ā“š£®
£¬¾Ż“Ė½ā“š£®
½ā“š ½ā£ŗ£Ø1£©¼×ÖŠŗ¬ÓŠĢ¼Ģ¼Ė«¼üŗĶ“¼ōĒ»ł£¬Ęäŗ¬Ńõ¹ŁÄÜĶÅŹĒōĒ»ł£¬ŅŅÖŠŗ¬ÓŠĢ¼Ģ¼Ė«¼üŗĶČ©»ł£¬Ęäŗ¬Ńõ¹ŁÄÜĶÅŹĒČ©»ł£¬¼×ÖŠŗ¬ÓŠĢ¼Ģ¼Ė«¼üŗĶ±½»·¶¼ÄÜÓėĒāĘų·¢Éś¼Ó³É·“Ó¦£¬1mol¼××ī¶ąæÉŅŌŗĶ4molH2·¢Éś¼Ó³É·“Ó¦
¹Ź“š°øĪŖ£ŗōĒ»ł£»Č©»ł£»4£»
£Ø2£©¼×ÖŠÓŠĢ¼Ģ¼Ė«¼ü£¬ÄÜ·¢Éś¼Ó¾Ū·“Ӧɜ³ÉKĪŖ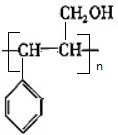 ·“Ó¦µÄ·½³ĢŹ½ĪŖ
·“Ó¦µÄ·½³ĢŹ½ĪŖ £¬
£¬
¹Ź“š°øĪŖ£ŗ £»
£»
£Ø3£©ÓÉĪļÖŹµÄ½į¹¹æÉÖŖ£¬·“Ó¦¢ńŹĒ¼×ÖŠĢ¼Ģ¼Ė«¼üÓėHCl·¢Éś¼Ó³É·“Ӧɜ³É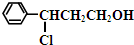 £¬Č»ŗó
£¬Č»ŗó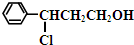 ÖŠ“¼ōĒ»ł·¢ÉśŃõ»Æ·“Ӧɜ³ÉYĪŖ
ÖŠ“¼ōĒ»ł·¢ÉśŃõ»Æ·“Ӧɜ³ÉYĪŖ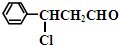 £¬·“Ó¦¢ņŹĒY·¢ÉśĀ±“śĢžµÄĻūČ„·“Ӧɜ³ÉŅŅ£¬ĖłŅŌ·“Ó¦¢ńµÄ·“Ó¦ĄąŠĶĪŖ¼Ó³É·“Ó¦£¬·“Ó¦¢ņµÄ»Æѧ·½³ĢŹ½ĪŖ
£¬·“Ó¦¢ņŹĒY·¢ÉśĀ±“śĢžµÄĻūČ„·“Ӧɜ³ÉŅŅ£¬ĖłŅŌ·“Ó¦¢ńµÄ·“Ó¦ĄąŠĶĪŖ¼Ó³É·“Ó¦£¬·“Ó¦¢ņµÄ»Æѧ·½³ĢŹ½ĪŖ £¬
£¬
¹Ź“š°øĪŖ£ŗ¼Ó³É£» £»
£»
£Ø4£©ŅŅ·¢ÉśŠÅĻ¢ÖŠŃõ»Æ·“Ӧɜ³ÉAÓėB£¬Č©AŗĶÅØNaOH·“ӦȻŗóĖį»ÆµĆµ½E£¬½įŗĻŠÅĻ¢æÉÖŖAÉś³ÉōČĖįŗĶ“¼£¬¶ųEµÄĻą¶Ō·Ö×ÓÖŹĮæĪŖ76£¬ŌņAÖŠ²»æÉÄÜŗ¬ÓŠ±½»·£¬ŌņAĪŖOHC-CHO£¬EĪŖHOCH2COOH£¬BĪŖ £¬FŹĒÓÉĮ½·Ö×ÓEÉś³ÉµÄĮłŌŖ»·£¬ŌņFĪŖ
£¬FŹĒÓÉĮ½·Ö×ÓEÉś³ÉµÄĮłŌŖ»·£¬ŌņFĪŖ £¬ŅŅÓėŠĀÖĘĒāŃõ»ÆĶ·¢ÉśŃõ»Æ·“Ó¦”¢Ėį»ÆÉś³ÉDĪŖ£¬ŌņDĪŖ
£¬ŅŅÓėŠĀÖĘĒāŃõ»ÆĶ·¢ÉśŃõ»Æ·“Ó¦”¢Ėį»ÆÉś³ÉDĪŖ£¬ŌņDĪŖ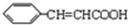 £¬±ūµÄ·Ö×ÓŹ½ĪŖC16H14O2£¬±ūÄÜŹ¹Br2/CCl2ĶŹÉ«ÄÜŌŚĻ”ĮņĖįÖŠĖ®½ā£¬ĖµĆ÷±ūÖŠÓŠĢ¼Ģ¼²»±„ŗĶ¼üŗĶõ„»ł£¬CÓėDŌŚÅØĮņĖį”¢¼ÓČČĢõ¼žÉś³É±ū£¬Ó¦ŹĒ·¢Éśõ„»Æ·“Ó¦£¬¹ŹBÓėĒāĘų·¢Éś¼Ó³É·“Ӧɜ³ÉCĪŖ
£¬±ūµÄ·Ö×ÓŹ½ĪŖC16H14O2£¬±ūÄÜŹ¹Br2/CCl2ĶŹÉ«ÄÜŌŚĻ”ĮņĖįÖŠĖ®½ā£¬ĖµĆ÷±ūÖŠÓŠĢ¼Ģ¼²»±„ŗĶ¼üŗĶõ„»ł£¬CÓėDŌŚÅØĮņĖį”¢¼ÓČČĢõ¼žÉś³É±ū£¬Ó¦ŹĒ·¢Éśõ„»Æ·“Ó¦£¬¹ŹBÓėĒāĘų·¢Éś¼Ó³É·“Ӧɜ³ÉCĪŖ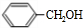 £¬±ūĪŖ
£¬±ūĪŖ £¬
£¬
¢Łøł¾ŻÉĻĆęµÄ·ÖĪöæÉÖŖ£¬±ūĪŖ £¬¹Ź“š°øĪŖ£ŗ
£¬¹Ź“š°øĪŖ£ŗ £»
£»
¢ŚCĪŖ £¬ÄÜÓėÄĘ²śÉśĒāĘų£¬ÓėŅŅĖį·¢Éśõ„»Æ·“Ó¦£¬²»ÄÜÓėĒāŃõ»ÆÄĘ·“Ó¦£¬Ņ²²»ÄÜÓėĢ¼ĖįÄĘČÜŅŗ·“Ó¦£¬¹ŹŃ”bc£»
£¬ÄÜÓėÄĘ²śÉśĒāĘų£¬ÓėŅŅĖį·¢Éśõ„»Æ·“Ó¦£¬²»ÄÜÓėĒāŃõ»ÆÄĘ·“Ó¦£¬Ņ²²»ÄÜÓėĢ¼ĖįÄĘČÜŅŗ·“Ó¦£¬¹ŹŃ”bc£»
¢Ūøł¾ŻÉĻĆęµÄ·ÖĪöæÉÖŖ£¬FµÄ½į¹¹¼ņŹ½ĪŖ £¬¹Ź“š°øĪŖ£ŗ
£¬¹Ź“š°øĪŖ£ŗ £»
£»
¢ÜDµÄ½į¹¹¼ņŹ½ĪŖ £¬ĘäĶ¬·ÖŅģ¹¹Ģå·ūŗĻĻĀĮŠĢõ¼ž£¬
£¬ĘäĶ¬·ÖŅģ¹¹Ģå·ūŗĻĻĀĮŠĢõ¼ž£¬
a£®»ÆŗĻĪļŹĒ¶žČ”“ś±½£¬ĖµĆ÷ŗ¬ÓŠ±½»·£¬ĒŅ±½»·ÉĻŗ¬ÓŠĮ½øöČ”“ś»ł£»
b£®·Ö×ÓÖŠÓŠ5ÖÖ²»Ķ¬»·¾³µÄĒāŌ×Ó£¬ĘäøöŹż±ČĪŖl£ŗ2£ŗ2£ŗ1£ŗ2£¬ŌņøĆ·Ö×ÓÖŠŗ¬ÓŠ5ÖÖHŌ×Ó£»
c£®ÄÜŹ¹äåµÄCCl4ČÜŅŗĶŹÉ«£¬ĒŅŌŚĖįŠŌĢõ¼žĻĀæÉŅŌ·¢ÉśĖ®½ā·“Ó¦£¬ĖµĆ÷ŗ¬ÓŠĢ¼Ģ¼Ė«¼üŗĶõ„»ł£»
d£®ŹōÓŚ·ÓĄą£¬
Ōņ·ūŗĻĢõ¼žµÄDµÄĶ¬·ÖŅģ¹¹ĢåĪŖ±½»·ÉĻĮ¬ÓŠ-OH”¢-CH=CH2”¢-CHO£¬øł¾Ż¶Ø¶ž¶ÆŅ»µÄŌŌņæÉÖŖÕāŃłµÄ½į¹¹ÓŠ10ÖÖ£¬Čē µČ£¬
µČ£¬
¹Ź“š°øĪŖ£ŗ10£» £®
£®
µćĘĄ ±¾Ģāæ¼²éÓŠ»śĪļĶʶĻ£¬Ķ¬Ź±æ¼²éѧɜ»ńČ”ŠÅĻ¢”¢¼Ó¹¤ŠÅĻ¢”¢ĶʶĻÄÜĮ¦£¬øł¾ŻĪļÖŹÖŠµÄ¹ŁÄÜĶÅČ·¶ØĘä¾ßÓŠµÄŠŌÖŹ£¬×¢Ņā·“Ó¦Ģõ¼žµÄŌĖÓĆ£¬ÄѵćŹĒĶ¬·ÖŅģ¹¹ĢåÖÖĄąÅŠ¶Ļ£¬ĢāÄæÄѶČÖŠµČ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 £¬ŹōÓŚČ”“ś ·“Ó¦£»
£¬ŹōÓŚČ”“ś ·“Ó¦£»²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŅŅĻ©ŹĒŹÆÓĶĮŃ½āŗóµÄ²śĪļ | |
| B£® | ·¼ĻćĢžÖ÷ŅŖĄ“×ŌÓŚĆŗµÄøÉĮóŗóµÄĆŗ½¹ÓĶ | |
| C£® | ĘūÓĶ”¢ĆŗÓĶ”¢²ńÓĶÖ÷ŅŖĄ“×ŌÓŚŹÆÓĶµÄ³£Ń¹ÕōĮó | |
| D£® | ĮŃ»ÆĘūÓĶ²»ÄÜŹ¹äåĖ®ĶŹÉ« |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | C2H4 | B£® | C4H8 | C£® | C3H8 | D£® | SiO2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com