
常温下,向100ml0.01mol/LHA的溶液中逐滴加入0.02mol/LMOH溶液,如图所示,曲线表示混合溶液的pH变化情况(溶液体积变化忽略不计)。下列说法中不正确的是
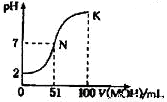
A.HA为一元强酸,MOH为一元强碱
B.N点水的电离程度大于K点水的电离程度
C.滴入MOH溶液的体积为50ml时,c(M+)>c(A-)
D.K点时,则有c(MOH)+(M+)=0.02mol/L
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2016-2017学年广西省高二上9月月考化学卷(解析版) 题型:选择题
下列图示与对应的叙述相符的是( )
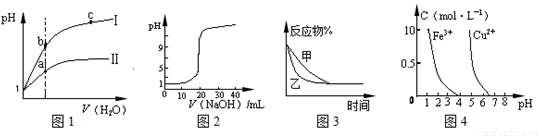
A.图1表示同温度下,pH = 1的盐酸和醋酸溶液分别加水稀释时pH的变化曲线,其中曲线II 为盐酸.且b点溶液的导电性比a点强
B.图2表示0.1000 mol/L CH3COOH溶液滴定20.00mL0.1000mol/LNaOH溶液所得到的滴定曲线
C.图3表示压强对可逆反应2A(g)+2B(g) 3C(g)+D(s)的影响,乙的压强比甲的压强大
3C(g)+D(s)的影响,乙的压强比甲的压强大
D.据图4,若除去CuSO4溶液中的Fe3+可向溶液中加入适量CuO至pH 在4左右
查看答案和解析>>
科目:高中化学 来源:2017届四川省高三上学期10月月考化学试卷(解析版) 题型:实验题
以下是有关SO2、Cl2的性质实验。
某小组设计如图所示的装置图(图中夹持和加热装置略去),分别研究SO2和Cl2的性质。

①若从左端分别通入SO2和Cl2,装置A中观察到的现象是否相同? (填“相同”或“不相同”);若D中盛铜粉,通入足量的Cl2,D中的现象是___________;若装置D中装的是五氧化二钒(催化剂),通入SO2时,打开K通入适量O2的化学反应方程式为 。
②SO2通入B中,碘水褪色,则该反应的离子方程式为 。
③E中盛有______________溶液。
某同学将足量的SO2通入一支装有氯化钡溶液的试管,未见沉淀生成,若向该试管中加入足量(填字母) ,则可以看到白色沉淀产生。
A.氨水 B.硝酸钠溶液 C.氯化钙溶液
若由元素S和O组成–2价酸根离子X,X中S和O的质量比为4∶3;当Cl2与含X的溶液完全反应后,得澄清溶液,取少量该溶液加入盐酸酸化的氯化钡溶液,有白色沉淀产生。写出Cl2与含X的溶液反应的离子方程式 。
查看答案和解析>>
科目:高中化学 来源:2017届四川省高三上学期10月阶段测化学卷(解析版) 题型:选择题
下列离子方程式,书写正确的是
A.用惰性电极电解熔融氯化钠:2Cl-+ 2H2O Cl2↑+ H2↑+ 2OH-
Cl2↑+ H2↑+ 2OH-
B.铁粉溶于稀硫酸:2Fe + 6H+ = 2Fe3+ + 3H2↑
C.用 CuSO4 溶液吸收 H2S:Cu2+ + H2S = CuS↓+ 2H+
D.向 NH4HSO4 溶液中滴加少量的 Ba(OH)2 溶液:NH4++H++SO42-+Ba2++2OH-=BaSO4↓+NH3•H2O+H2O
查看答案和解析>>
科目:高中化学 来源:2017届山西省高三上学期10月月考化学试卷(解析版) 题型:推断题
欲确定某无色透明溶液中是否含有下列离子: Cl-、I-、SO42-、HCO3-、NO3-、Na+、Mg2+、Al3+、Fe2+、Ba2+,取适量溶液分别装进①②③④号试管,进行如下实验,请依实验现象回答问题:
①加几滴石蕊试液, 溶液变红色
②浓缩,加Cu片和浓H2SO4,加热, 有无色气体产生,后在空气中又变成红棕色
③加BaCl2溶液, 立即白色沉淀生成。取上层清液,加AgNO3溶液, 出现白色沉淀,且不溶于HNO3
④加NaOH溶液, 有白色沉淀生成,当NaOH过量时沉淀部分溶解
(1)溶液中肯定存在的离子是 。
(2)溶液中肯定不存在的离子是 。
(3)为进一步确定其他离子,应该补充的实验是 。
(4)写出实验④中所有反应的离子方程式__________________
查看答案和解析>>
科目:高中化学 来源:2017届山西省高三上学期10月月考化学试卷(解析版) 题型:选择题
能正确表示下列反应的离子方程式的是
A.用浓盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:2MnO4-+ 6H+ + 5H2O2= 2Mn2+ + 5O2↑ + 8H2O
B.向次氯酸钙溶液通入过量CO2:Ca2++2ClO-+CO2+H2O =CaCO3↓+2HClO
C.向次氯酸钙溶液通入SO2:Ca2++2ClO-+SO2+H2O= CaSO3↓+2HClO
D.FeBr2溶液与等物质的量的Cl2反应:2Fe2++ 2Br-+2Cl2=2Fe3++4Cl-+Br2
查看答案和解析>>
科目:高中化学 来源:2017届山西省高三上学期10月月考化学试卷(解析版) 题型:选择题
下列表述正确的是
A.1mol H2燃烧放出的热量为H2的燃烧热
B.稀豆浆、硅酸、氯化铁溶液均为胶体
C.NH4Br的电子式: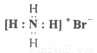
D.丙烯的结构简式:CH3CH=CH2
查看答案和解析>>
科目:高中化学 来源:2017届湖南省长沙市高三上月考二化学试卷(解析版) 题型:选择题
某溶液能与Al粉反应放出H2,该溶液中可能大量共存的离子组是
A.NH4+、Ba2+、HCO3-、Cl-、 B.K+、Al3+、S2-、ClO-
C.Na+、Fe3+、Cl-、SO42- D.NH4+、Mg2+、SO42-、NO3-
查看答案和解析>>
科目:高中化学 来源:2017届广西省高三上9月月考化学试卷(解析版) 题型:实验题
某小组同学在实验室里对Fe3+与I﹣的反应进行探究,实现Fe3+与Fe2+相互转化.
(1)甲同学首先进行了如下实验:
编号 | 操作 | 现象 |
Ⅰ | 先向2mL0.1mol•L﹣1FeCl2溶液中滴加KSCN溶液,再滴加新制氯水 | ___________________ ___________________ |
Ⅱ | 先向2mL0.1mol•L﹣1FeCl3溶液中滴加KSCN溶液,再滴加0.1mol•L﹣1KI溶液 | 滴加KSCN溶液后,溶液变成血红色;滴加0.1mol•L﹣1KI溶液后,血红色无明显变化 |
实验Ⅰ中发生反应的离子方程式为 , .
(2)实验II的现象与预测不同,为探究可能的原因,甲同学又进行了如下实验,
操作及现象如下:
编号 | 操作 | 现象 |
Ⅲ | 向2mL0.1mol•L﹣1KI溶液中滴加1mL 0.1mol•L﹣1FeCl3溶液,再滴加KSCN溶液 | 滴加FeCl3溶液后,溶液变成黄色;滴加KSCN溶液后,溶液变成血红色 |
根据实验Ⅲ,该同学认为Fe3+有可能与I﹣发生氧化还原反应.请结合实验现象说明得出该结论的理由: .
(3)乙同学认为,还需要进一步设计实验才可证明根据实验Ⅲ中现象得出的结论.
请补全下表中的实验方案:
编号 | 操作 | 预期现象及结论 |
Ⅳ | 向2mL0.1mol•L﹣1KI溶液中滴加1mL 0.1mol•L﹣1 FeCl3,溶液变黄色,取该溶液于两支试管中, 试管①中滴加 , 试管②中滴加 . | 预期现象① , ② . 结论 . |
(4)上述实验结果表明,Fe3+有可能与I﹣发生氧化还原反应.进一步查阅资料知,参加反应的Fe3+和I﹣物质的量相同.该小组同学结合上述实验结论,分析了实验Ⅲ中加入KSCN后溶液变血红色的原因,认为Fe3+与I﹣反应的离子方程式应写为: .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com