
下列实验或操作方法正确的是
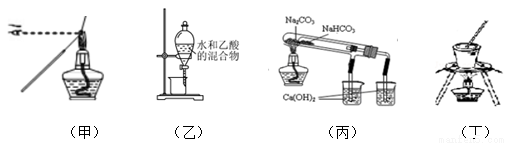
A.甲图装置:用蘸有待测液的铁丝,检验K+
B.乙图装置:分离水和乙酸
C.丙图装置:验证NaHCO3和Na2CO3的热稳定性
D.丁图装置:从食盐水中提取食盐
科目:高中化学 来源:2015-2016学年安徽师大附中高二下期中化学试卷(解析版) 题型:选择题
恒温下,容积为2L的定容密闭容器中,充入3molA、ymolB,发生反应:3A(g)+2B(g) 2C(g)+xD(g)。2min后达到平衡,测得从反应开始到平衡时C的速率为0.3mol·L-1·min-1.下列推断的结论正确的是
2C(g)+xD(g)。2min后达到平衡,测得从反应开始到平衡时C的速率为0.3mol·L-1·min-1.下列推断的结论正确的是
A.y 1.2
1.2
B.增大反应体系的压强,反应速率不一定增大
C.v正(A)>v逆(C),不可能为平衡状态
D.混合气体的密度不再变化,一定为平衡状态
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省高一下期中化学试卷(解析版) 题型:选择题
下列反应既是氧化还原反应,又是吸热反应的是
A.铝片与稀硫酸反应 B.Ba(OH)2·8H2O与NH4Cl的反应
C.灼热的炭与CO2反应 D.甲烷在O2中的燃烧
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省高二下期中化学试卷(解析版) 题型:选择题
下列设计的实验方案能达到实验目的的是
A. 将苯和溴水混合后加入Fe粉制溴苯
B. 为检验皂化反应进行程度,取几滴反应液,滴入装有热水的试管中,振荡,若无油滴浮在液面上,说明油脂已完全反应
C. 检验淀粉在稀硫酸催化条件下水解产物的方法是:取适量水解液于试管中,加入少量新制Cu(OH)2悬浊液,加热煮沸,观察是否出现红色沉淀
D. 探究化学反应的限度:取5ml 0.1mol/LKI溶液,滴加0.1mol/LFeCl3溶液5-6滴,充分反应,根据溶液中是否含有碘单质和碘离子判断该反应有一定限度
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省高二下期中化学试卷(解析版) 题型:选择题
下列离子方程式与所述事实相符且正确的是
A. 氯气和水反应:Cl2 + H2O  2H+ + Cl- + ClO-
2H+ + Cl- + ClO-
B. 碳酸钙与醋酸溶液反应:CaCO3 + 2H+ = Ca2+ + H2O + CO2↑
C. 200 mL 2 mol/L的FeBr2溶液中通入11.2 L标准状况下的氯气:
4Fe2+ + 6Br-+ 5Cl2 == 4Fe3+ + 3Br2 + 10Cl-
D. Na2S水解的离子方程式:S2- + 2H2O  H2S + 2OH-
H2S + 2OH-
查看答案和解析>>
科目:高中化学 来源:2015-2016学年云南省高一下期中化学试卷(解析版) 题型:填空题
I.锌与稀硫酸的反应既是氧化还原反应,又是 反应(填“放热”或“吸热”,实验室可将该反应设计成原电池,应采用 作为负极材料,正极的电极反应式为 ,若有1mol电子流过导线,理论上正极产生的气体在标准状况下的体积是 L。
II.某同学在用稀硫酸与锌制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率。请回答下列问题:
(1)硫酸铜溶液可以加快氢气生成速率的原因是 ;
(2)实验室中现有Na2SO4、MgSO4、Ag2SO4、K2SO4等4种溶液,可与实验中CuSO4溶液起相似作用的是 ;
(3)要加快上述实验中气体产生的速率,还可采取的措施有 (答两种);
(4)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验。将表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需时间。

①请完成此实验设计,其中:V1= ,V6= ,V9= ;
②该同学最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高。但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年云南省高一下期中化学试卷(解析版) 题型:选择题
日常所用锌-锰干电池的电极分别为锌筒和石墨棒,以糊状NH4Cl作电解质,电极反应为:Zn-2e-=Zn2+,2MnO2+2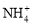 +2e-=Mn2O3+2NH3+H2O。下列有关锌-锰干电池的叙述中,正确的是
+2e-=Mn2O3+2NH3+H2O。下列有关锌-锰干电池的叙述中,正确的是
A.干电池中锌筒为正极,石墨棒为负极
B.干电池长时间连续工作后,糊状物可能流出,腐蚀用电器
C.干电池工作时,电流方向是由锌筒经外电路流向石墨棒
D.干电池可实现化学能向电能和电能向化学能的相互转化
查看答案和解析>>
科目:高中化学 来源:2015-2016学年新疆生产建设兵团二中高一下期中化学试卷(解析版) 题型:填空题
一定温度下,在容积为V L的密闭容器中进行aN(g) bM(g)的放热反应,M、N物质的量随时间的变化曲线如图所示:
bM(g)的放热反应,M、N物质的量随时间的变化曲线如图所示:

(1)此反应的化学方程式中=______。
(2)t2时两线交叉点__平衡状态(填“是”或“不是”),v正__v逆(填“>”“<” 或“=”)。
(3)此反应达到平衡时,反应物的转化率为____________。
(4)下列描述能说明上述反应达到平衡状态的是__________。
①反应中M与N物质的量之比为2∶5 ②混合气体的总物质的量不随时间的变化而变化③M的转化率达到最大 ④如容器为绝热容器,体系内温度不再变化
II某温度时,把1 mol N2O4气体通入体积为10 L的真空密闭容器中,立即出现红棕色[因为发生N2O4(无色) 2NO2(红棕色)的反应],反应进行4 s时,NO2的浓度为0.04mol·L-1,再经过一段时间后反应达到平衡状态,这时容器内压强为开始时的1.8倍,则
2NO2(红棕色)的反应],反应进行4 s时,NO2的浓度为0.04mol·L-1,再经过一段时间后反应达到平衡状态,这时容器内压强为开始时的1.8倍,则
(1)前4 s以N2O4浓度变化表示的平均反应速率为 。
(2)在4 s末时容器内的压强是开始时的 倍。
(3)平衡时容器内NO2的浓度是 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南省高二下期中化学试卷(解析版) 题型:选择题
在核磁共振氢谱中出现两组峰,其氢原子数之比为3∶2的化合物是 ( )
A.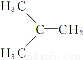 B.
B.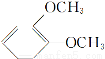
C.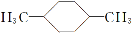 D.
D.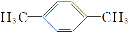
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com