
| A、MnO4- Cl- NH4+ Na+ |
| B、CO32- NO3- Ca2+Na+ |
| C、SO42- HCO3- K+ Na+ |
| D、SO42-NO3-K+ Na+ |


科目:高中化学 来源: 题型:
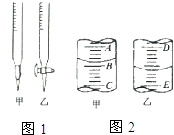 实验室中有一未知浓度的稀盐酸,某学生为测定盐酸的浓度在实验室中进行如下实验.请你完成下列填空:
实验室中有一未知浓度的稀盐酸,某学生为测定盐酸的浓度在实验室中进行如下实验.请你完成下列填空:| 实验编号 | NaOH溶液的浓度 (mol/L) | 滴定完成时,消耗NaOH溶液的体积(mL) | 待测盐酸溶液的体积(mL) |
| 1 | 0.10 | 22.02 | 20.00 |
| 2 | 0.10 | 22.00 | 20.00 |
| 3 | 0.10 | 21.98 | 20.00 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、3.38g |
| B、34.58g |
| C、4.16g |
| D、34.41g |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、K+、Cu2+、Na+、Cl- |
| B、SO42-、Na+、NO3-、CO32- |
| C、Na+、H+、NO3-、SO42- |
| D、Al3+、Na+、Cl-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向CuS04溶液中加入铁时会置换出铜,可推向CuS04溶液中加入钠时也会置换出铜 |
| B、氢氟酸的酸性比盐酸弱,故非金属性是F>Cl |
| C、丁达尔效应是胶体的本质特征 |
| D、MgO可以除去MgCl2溶液中含有的FeCl3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、乙烯和聚乙烯都能使溴的四氯化碳溶液褪色 |
| B、淀粉和纤维素都可以作为工业上生产葡萄糖的原料 |
| C、油脂的水解反应,都是皂化反应 |
| D、蔗糖是高分子化合物,其水解产物能发生银镜反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com