
| A. | 水电离出的c(H+)=10-12mol/L的溶液:Ba2+、Na+、NO3-、Cl- | |
| B. | 含有大量NO3-的水溶液中:NH4+、Fe2+、SO42-、H+ | |
| C. | 在pH=7的溶液中:Na+、Fe3+、SO42-、Br- | |
| D. | 强碱性溶液中:ClO-、S2-、HSO3-、Na+ |
分析 A.水电离出的c(H+)=10-12mol/L的溶液,为酸或碱溶液;
B.离子之间发生氧化还原反应;
C.铁离子在pH为4.4左右沉淀完全;
D.离子之间发生氧化还原反应,且碱性溶液中不能大量存在酸式酸根离子.
解答 解:A.水电离出的c(H+)=10-12mol/L的溶液,为酸或碱溶液,酸、碱溶液中该组离子之间均不反应,可大量共存,故A正确;
B.Fe2+、NO3-、H+发生氧化还原反应,不能大量共存,故B错误;
C.铁离子在pH为4.4左右沉淀完全,则pH=7的溶液中不能大量存在Fe3+,故C错误;
D.ClO-、S2-发生氧化还原反应,且碱性溶液中不能大量存在HSO3-,故D错误;
故选A.
点评 本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重复分解反应、氧化还原反应的离子共存考查,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②③ | C. | ①④ | D. | ③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 全部 | B. | ①②③④⑤ | C. | ①②③⑤ | D. | ②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 37Cl与39K所含的中子数不同 | |
| B. | 12C和14C是不同的核素,但质子数相等 | |
| C. | H3O+与OH-的质子数和电子数均相同 | |
| D. | Mg2+与O2-的核外电子排布不相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 序号 | ① | ② | ③ | ④ | ⑤ | ⑥ |
| 仪器及装置图 |  | 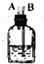 |  |  |  | 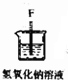 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | +1 | B. | +2 | C. | +3 | D. | +4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 热稳定性:Na2CO3>NaHCO3 | |
| B. | 常温下在水中的溶解度:Na2CO3>NaHCO3 | |
| C. | Na2CO3溶液和NaHCO3溶液可用澄清石灰水鉴别 | |
| D. | 相同物质的量Na2CO3和NaHCO3与盐酸完全反应,产生的CO2一样多,消耗HCl的物质的量之比为2:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题

| A. | △H>0,m+n>x+y | B. | △H<0,m+n>x+y | C. | △H<0,m+n>x | D. | △H>0,m+n<x |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com