A、B、C、D、E是位于短周期的主族元素,其中A、B为金属元素,D的最外层电子数是其内层电子数的三倍.已知:①热稳定性:H
mD>H
mC;②C
m-、E
(m-1)-具有相同的电子层结构;③B与E在同一周期,在该周期中,E的原子半径最小,B的离子半径最小;④A、B所形成的单核离子具有相同的电子层结构,B的最高价氧化物对应的水化物与A、E的最高价氧化物对应的水化物都能反应.依据上述信息回答下列问题:
(1)H
mD的电子式:
.A和E形成的化合物的晶体类型属
离子晶体
离子晶体
;该晶体结构中离A最近的A有
12
12
个.
(2)能证明C
m-、E
(m-1)-还原性强弱的反应的离子方程式为
Cl2+S2-═2Cl-+S↓
Cl2+S2-═2Cl-+S↓
.
(3)用化学用语表示B的最高正价氧化物对应的水化物在水溶液中的电离过程
H2O+H++AlO2-?Al(OH)3?Al3++3OH-
H2O+H++AlO2-?Al(OH)3?Al3++3OH-
.
(4)已知17g H
mC在一定条件下完全燃烧生成稳定化合物时放出热量为a kJ,写出能表示该物质燃烧热的热化学方程式
2H2S(g)+3O2(g)?2SO2(g)+2H2O(l)△H=-4akJ/mol
2H2S(g)+3O2(g)?2SO2(g)+2H2O(l)△H=-4akJ/mol
.
(5)常温下,将等物质的量浓度的H
mC溶液和A的最高价氧化物对应的水化物溶液等体积混合,所得溶液显碱性,溶液中离子浓度由大到小的顺序为
c(Na+)>c(HS-)>c(OH-)>c(H+)>c(S2-)
c(Na+)>c(HS-)>c(OH-)>c(H+)>c(S2-)
.

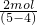 =2mol;
=2mol;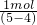 =1mol;
=1mol;








