
| A. | c(CH3COO-)>c(NH4+)>c(H+)=c(OH-) | B. | c(NH4+)>c(CH3COO-)>c(H+)=c(OH-) | ||
| C. | c(CH3COO-)=c(NH4+)>c(H+)=c(OH-) | D. | c (CH3COO-)>c(NH4+)>c(H+)>c(OH-) |
分析 常温下,醋酸和氨水等体积混合后溶液的pH=7,溶液呈中性,则c(H+)=c(OH-),根据电荷守恒判断c(NH4+)、c(CH3COO-)相对大小,中性溶液中水的电离程度较小,据此分析解答.
解答 解:常温下,醋酸和氨水等体积混合后溶液的pH=7,溶液呈中性,则c(H+)=c(OH-),根据电荷守恒得c(NH4+)=c(CH3COO-),中性溶液中水的电离程度较小,所以溶液中离子浓度大小顺序是c(CH3COO-)=c(NH4+)>c(H+)=c(OH-),故选C.
点评 本题考查离子浓度大小比较,为高频考点,根据溶液酸碱性结合电荷守恒、物料守恒是解离子浓度大小比较题的重要方法,题目难度不大.


科目:高中化学 来源: 题型:解答题
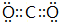 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 所有分散系,分散剂必须是液态的 | |
| B. | 胶体区别于其它分散系的本质原因是分散质和分散剂不同 | |
| C. | 从物质分类的角度讲,分散系是混合物 | |
| D. | 所有的分散系都能均匀稳定的长期存在 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 纯净物 | 混合物 | 强电解质 | 弱电解质 | 非电解质 | |
| A | 水玻璃 | 盐酸 | 硫酸 | 次氯酸 | 干冰 |
| B | 冰 | 氨水 | 碳酸钙 | 水 | 氨气 |
| C | 氯水 | 漂白粉 | 苛性钠 | 碳酸 | 氯化银 |
| D | 苏打 | 赤铁矿 | 氯化钡 | 氢硫酸 | 氯气 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙醇 | B. | 乙醛 | C. | 乙酸 | D. | 甲酸乙酯 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化学反应过程中既有物质变化又有能量变化,能量的释放或吸收以物质变化为基础 | |
| B. | 研究化学反应进行的方向、快慢和限度是化学反应原理的重要内容 | |
| C. | 电解质在水溶液中的反应反应速率很高,是因为这类反应不需要活化能来引发 | |
| D. | 大力发展火电以满足工业发展对电力的需求,符合节能减排的要求 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com