
【题目】下列变化必须加入氧化剂才能实现的是
A.Brˉ→ Br2B.H2SO4→SO2C.Na2CO3→CO2D.Fe2O3→Fe
科目:高中化学 来源: 题型:
【题目】下列有关化学用语的表述正确的( )
A. 醋酸的电离方程式:CH3COOH= CH3COO-+H+
B. H216O、H218O互为同位素
C. 质子数为53,中子数为78的碘原子:13153I
D. 氯离子的结构示意图:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】⑴室温时,在下列物质中:①Na ②Cl2 ③Na2O ④FeCl2溶液 ⑤NaHCO3 ⑥蔗糖 ⑦NH3⑧NaCl晶体 ⑨HClO ⑩ Fe(OH)2
属于碱性氧化物的是(用序号填写,下同) __________,属于酸的是________,属于强电解质的是____________,属于非电解质的是____________,能导电的是___________。
⑵下列各组化学用语中:①3He、4He ② 2H2 O、1H2O ③ 1H、3H ④14N和13C质子数相同的有_________,中子数相同的有________,互为同位素的有________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酸氯(ClNO)可由NO与Cl2在通常条件下反应得到,化学方程式为:2NO(g)+Cl2(g)![]() 2ClNO(g)。
2ClNO(g)。
(1)在一定温度下,该反应于一恒容密闭容器中达到平衡继续通入Cl2,逆反应速率____(填增大、减少、不变)。
(2)已知几种化学键的键能数据如下表(NO的结构为:N≡O;亚硝酸氯的结构为Cl-N=O)
化学键 | N≡O | Cl-Cl | Cl-N | N=O |
键能(kJ/mol) | 630 | 243 | a | 607 |
2NO(g)+Cl2(g)![]() 2ClNO(g) △H=-111kJ/mol则a=______。
2ClNO(g) △H=-111kJ/mol则a=______。
(3)在1L的恒容密闭容器中充入2molNO(g)和1molCl2(g),在不同温度下测得c(ClNO)与时间的关系如图A:
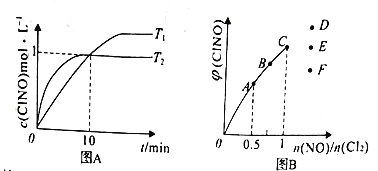
①该反应的T1______T2(填“>”<”或“=”)。
②反应开始到10min时NO的平均反应速率v(NO)=_______mol/(L.min)。
③T2时该反应的平衡常数K=________。
(4)一定条件下在恒温恒容的密闭容器中按一定比例充入NO(g)和Cl2(g),平衡时ClNO的体积分数随n(NO)/n(Cl2)的变化图象如图B,则A、B、C三状态中,NO的转化率最大的是_____点,当n(NO)/n(Cl2)=1.5时,达到平衡状态ClNO的体积分数可能是D、E、F三点中的____点。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室需用80mL1mol/L的氢氧化钠溶液,配制此溶液的正确操作是
A.称取3.2g氢氧化钠,溶于水80mL水中
B.称取4.0g氢氧化钠,溶于水100mL水中
C.称取3.2g氢氧化钠,溶于水配成80mL溶液
D.称取4.0g氢氧化钠,溶于水配成100mL溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】M是第四周期元素,最外层只有1个电子,次外层的所有原子轨道均充满电子。元素Y的负一价离子的最外层电子数与次外层的相同。回答下列问题:
(1)在元素周期表中M位于_____区,基态M原子的价层电子排布图为_____,第四能层s轨道上电了数目和M元素相同的元素还有_____(填元素符号)。
(2)元素Y基态原子的核外电子排布式为_______,其同周期元素中,第一电离能最大的是____(写元素符号)。元素Y的含氧酸中,酸性最强的是_____(写化学式),该酸根离子的立体构型为_______。
(3)Z与元素Y同主族,在该族中原子序数最小,Z的气态氢化物的稳定性大于Y的气态氢化物的稳定性,原因是__________,Z的气态氢化物的沸点大于Y的气态氢化物的沸点,原因是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】被誉为“光纤之父”的华裔科学家高锟因为在“光在纤维中的传输用于光学通信”的成就而获 得 2009 年诺贝尔物理学奖,光导纤维的主要成分是
A.SiB.SiO2C.Na2SiO3D.SiCl4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应FeO(s) +C(s)= CO(g) + Fe(s) △H>0,(假设△H,△S不随温度变化而变化),下列叙述中正确的是 ( )
A. 高温下为自发过程,低温下为非自发过程B. 任何温度下为非自发过程
C. 低温下为自发过程,高温下为非自发过程D. 任何温度下为自发过程
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com