
·ÖĪö Ķ¬Ņ»ŗĖĶāƻӊĮ½øöµē×ÓµÄø÷øö²ĪŹżĶźČ«ĻąĶ¬£¬Ō×ÓŗĖĶāĆæøöµē×ÓµÄŌĖ¶ÆדĢ¬¶¼ŹĒ²»Ķ¬µÄ£¬YµÄ»łĢ¬Ō×ÓŗĖĶāµē×ÓÓŠ5ÖÖ²»Ķ¬µÄŌĖ¶ÆדĢ¬£¬YĪŖB£¬X”¢Y·Ö±š“ś±ķŌ×ÓŠņŹżŅĄ“ĪŌö“óµÄ¶ĢÖÜĘŚÖ÷×åŌŖĖŲ£¬XŌŖĖŲŌ×ÓµÄÖŹ×ÓŹżµČÓŚĘäµē×Ó²ćŹż£¬XĪŖH£¬Ķ¬ÖÜĘŚĖęŌ×ÓŠņŹżŌö“óŌ×Ó°ė¾¶¼õŠ”£¬µē×Ó²ćŌ½¶ąŌ×Ó°ė¾¶Ō½“ó£¬RŌŖĖŲµÄŌ×Ó°ė¾¶ŌŚ¶ĢÖÜĘŚÖ÷×åŌŖĖŲÖŠ×ī“ó£¬ĪŖÄĘŌŖĖŲ£¬X”¢Y”¢Z”¢R”¢T”¢U·Ö±š“ś±ķŌ×ÓŠņŹżŅĄ“ĪŌö“óµÄ¶ĢÖÜĘŚÖ÷×åŌŖĖŲ£¬ZÓėTĶ¬Ö÷×åĒŅŌ×ÓŠņŹżTŹĒZµÄĮ½±¶£¬ZĪŖŃõŌŖĖŲ£¬TĪŖĮņŌŖĖŲ£¬ŌņUĪŖĀČŌŖĖŲ£®
£Ø1£©ZĪŖŃõŌŖĖŲ£¬Ō×ÓŗĖĶāÓŠ8øöµē×Ó£¬øł¾Ż¼Ū²ćµē×Ó¶Ō»„³āĄķĀŪ·ÖĪö£¬¼Ū²ćµē×Ó¶Ō=¦Ņ ¼üµē×Ó¶Ō+ÖŠŠÄŌ×ÓÉĻµÄ¹Āµē×Ó¶Ō£»
£Ø2£©·Ē½šŹōŠŌŌ½Ē棬×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦µÄĖ®»ÆĪļµÄĖįŠŌŌ½Ē棻
£Ø3£©øł¾Ż¾§ĢåµÄ¹¹³ÉĪ¢Į£Č·¶Ø¾§ĢåĄąŠĶ£»ĄūÓĆ¾łĢƷؼĘĖć³öĀČ»ÆÄĘ¾§°ūÖŠŗ¬ÓŠÄĘĄė×ÓŗĶĀČĄė×ÓøöŹż£¬ŌŁøł¾ŻĆÜ¶Č¹«Ź½¼ĘĖć£»
£Ø4£©YµÄµēøŗŠŌĪŖ2.0£¬XµÄµēøŗŠŌĪŖ2.1£¬ĒāµÄ·Ē½šŹōŠŌĒæÓŚÅš£¬B2H6ĘųĢåĶØČĖH20ÖŠ·“Ӧɜ³ÉŅ»ÖÖĖįĪŖÅšĖįŗĶŅ»ÖÖµ„ÖŹĪŖĒāĘų£¬¾Ż“ĖŹéŠ“·½³ĢŹ½£®
½ā“š ½ā£ŗ£Ø1£©ZÓėTĶ¬Ö÷×åĒŅŌ×ÓŠņŹżTŹĒZµÄĮ½±¶£¬ZĪŖŃõŌŖĖŲ£¬TĪŖĮņŌŖĖŲ£¬ŃõŌŖĖŲŌ×ÓŗĖĶāÓŠ8øöµē×Ó£¬ĖłŅŌŗĖĶāµē×ÓÅŲ¼Ź½ĪŖ£ŗ1s22s22p4»ņ[He]2s22p4£¬SŌ×ÓŠĪ³É3øö¦Ņ¼ü£¬¹Ā¶Ōµē×ÓŹż=$\frac{6+2-3”Į2}{2}$=1£¬ĪŖsp3Ōӻƣ¬Į¢Ģå¹¹ŠĶĪŖČż½Ē׶ŠĶ£¬
¹Ź“š°øĪŖ£ŗ1s22s22p4»ņ[He]2s22p4£»Čż½Ē׶ŠĪ£»
£Ø2£©TĪŖĮņŌŖĖŲ£¬ŌņUĪŖĀČŌŖĖŲ£¬Ķ¬Ņ»ÖÜĘŚ£¬“Ó×óĻņÓŅ£¬·Ē½šŹōŠŌŌöĒ棬·Ē½šŹōŠŌ£ŗCl£¾S£¬·Ē½šŹōŠŌŌ½Ē棬×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦µÄĖ®»ÆĪļµÄĖįŠŌŌ½Ē棬¹ŹĖįŠŌ£ŗHClO4£¾H2SO4£¬
¹Ź“š°øĪŖ£ŗHClO4£¾H2SO4£»
£Ø3£©RŌŖĖŲµÄŌ×Ó°ė¾¶ŌŚ¶ĢÖÜĘŚÖ÷×åŌŖĖŲÖŠ×ī“ó£¬ĪŖÄĘŌŖĖŲ£¬TĪŖĮņŌŖĖŲ£¬ŌņUĪŖĀČŌŖĖŲ£¬»ÆŗĻĪļRUĪŖĀČ»ÆÄĘ£¬ĪŖ½šŹō”¢·Ē½šŹōŌŖĖŲ×é³ÉµÄ»ÆŗĻĪļ£¬ĪŖĄė×Ó»ÆŗĻĪļ£¬
ĀČ»ÆÄĘ¾§°ūÖŠÄĘĄė×ÓøöŹż=1+12”Į$\frac{1}{4}$=4£¬ĀČĄė×ÓøöŹż=8”Į$\frac{1}{8}$£¬ĖłŅŌĀČ»ÆÄʵÄĆܶȦŃ=$\frac{4M}{6.02”Į1{0}^{23}”ĮV}$£¬
¹Ź“š°øĪŖ£ŗĄė×Ó¾§Ģ壻$\frac{4M}{6.02”Į1{0}^{23}”ĮV}$g/cm3£»
£Ø4£©YµÄµēøŗŠŌĪŖ2.0£¬XµÄµēøŗŠŌĪŖ2.1£¬ĒāµÄ·Ē½šŹōŠŌĒæÓŚÅš£¬B2H6ÖŠHĪŖ-1¼Ū£¬B2H6ĘųĢåĶØČĖH20ÖŠ·“Ӧɜ³ÉÅšĖįŗĶĒāĘų£¬·“Ó¦·½³ĢŹ½ĪŖ£ŗB2H6+6H2OØT2H3BO3”ż+6H2”ü£¬
¹Ź“š°øĪŖ£ŗB2H6+6H2OØT2H3BO3”ż+6H2”ü£®
µćĘĄ ±¾Ģāæ¼²éŌ×Ó½į¹¹ÓėŌŖĖŲµÄŠŌÖŹ£¬ĪŖøßĘµæ¼µć£¬²ąÖŲӌѧɜµÄ·ÖĪöÄÜĮ¦µÄ漲飬ŌŖĖŲµÄĶʶĻŹĒ½ā“šµÄ¹Ų¼ü£¬×¢Ņā°ŃĪÕŌŖĖŲµÄŠŌÖŹ¼°µ„ÖŹ”¢»ÆŗĻĪļµÄŠŌÖŹ£¬Ķ»ĘĘæŚĪŖYµÄ»łĢ¬Ō×ÓŗĖĶāµē×ÓÓŠ5ÖÖ²»Ķ¬µÄŌĖ¶ÆדĢ¬£¬YĪŖB£¬ĢāÄæÄѶČÖŠµČ£¬ÄѵćŹĒ¾§°ū¼ĘĖćÖŠĀČ»ÆÄĘĆÜ¶ČµÄ¼ĘĖć£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | Mg”¢Al | B£® | Mg”¢Fe | C£® | Zn”¢Fe | D£® | Al”¢Zn |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā

| µĪ¶Ø“ĪŹż | 1 | 2 | 3 | 4 |
| KMnO4ČÜŅŗĢå»ż/mL | 20.60 | 20.02 | 20.00 | 19.98 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| ±ąŗÅ | ĪļÖŹ | ŹŌ¼Į»ņ²Ł×÷Ćū³Ę |
| ¢Ł | ³żŌÓÖŹ£ŗNaHCO3ČÜŅŗ£ØNa2CO3£© | |
| ¢Ś | ³żŌÓÖŹ£ŗMgO£ØAl2O3£© | |
| ¢Ū | ³żŌÓÖŹ£ŗFeCl2ČÜŅŗ£ØFeCl3£© | |
| ¢Ü | ¼ų±š£ŗNaCl”¢KCl | |
| ¢Ż | ¼ų±š£ŗAlCl3”¢Al2£ØSO4£©3ČÜŅŗ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
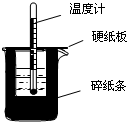 50mL0.50mol/LŃĪĖįÓė50mL0.55mol/LNaOHČÜŅŗŌŚČēĶ¼ĖłŹ¾µÄ×°ÖĆÖŠ½ųŠŠÖŠŗĶ·“Ó¦£®Ķعż²ā¶Ø·“Ó¦¹ż³ĢÖŠĖł·Å³öµÄČČĮææɼĘĖćÖŠŗĶČČ£®»Ų“šĻĀĮŠĪŹĢā£ŗ
50mL0.50mol/LŃĪĖįÓė50mL0.55mol/LNaOHČÜŅŗŌŚČēĶ¼ĖłŹ¾µÄ×°ÖĆÖŠ½ųŠŠÖŠŗĶ·“Ó¦£®Ķعż²ā¶Ø·“Ó¦¹ż³ĢÖŠĖł·Å³öµÄČČĮææɼĘĖćÖŠŗĶČČ£®»Ų“šĻĀĮŠĪŹĢā£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ·²ŹĒÖŠŠÄŌ×Ó²ÉČ”sp3ŌӻƵķÖ×Ó£¬ĘäĮ¢Ģå¹¹ŠĶ¶¼ŹĒÕżĖÄĆęĢåŠĶ | |
| B£® | ŌŚSCl2ÖŠ£¬ÖŠŠÄŌ×ÓS²ÉČ”spŌӻƹģµĄ³É¼ü | |
| C£® | ŌӻƹģµĄÖ»ÓĆÓŚŠĪ³É¦Ņ¼ü»ņÓĆÓŚČŻÄÉĪ“²ĪÓė³É¼üµÄ¹Āµē×Ó¶Ō | |
| D£® | ·²AB3ŠĶµÄ¹²¼Ū»ÆŗĻĪļ£¬ĘäÖŠŠÄŌ×ÓA¾ł²ÉÓĆsp3ŌӻƹģµĄ³É¼ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | 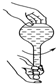 ¼ģ²éČŻĮæĘæŹĒ·ńĀ©Ė® | B£® |  øųČÜŅŗ¼ÓČČ | ||
| C£® |  µĪ¼ÓŅŗĢå | D£® | 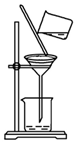 ¹żĀĖ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com