
| A. | Ba2+、K+、OH-、NO3- | B. | NH4+、Mg2+、SO42-、Cl- | ||
| C. | Al3+、Cu2+、SO42-、Cl- | D. | Na+、Ca2+、Cl-、CO32- |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
 ,则该分子中含有碳碳三键的数目为( )
,则该分子中含有碳碳三键的数目为( )| A. | 3 | B. | 2 | C. | 4 | D. | 1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 混合气体的颜色不再变化 | B. | 混合气体的压强不再变化 | ||
| C. | 反应速率v(H2)=$\frac{1}{2}$v(HI) | D. | c(H2):c(I2):c(HI)=1:1:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化钠与水反应:Na2O+H2O═Na++OH- | |
| B. | 氯化铝溶液与足量氨水反应:Al3++4OH-═AlO2-+2H2O | |
| C. | 氯化铝溶液与足量NaOH溶液反应:Al3++3OH-═Al(OH)3↓ | |
| D. | 氧化铝和适量的烧碱溶液反应:Al2O3+2OH-═2AlO2-+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 明矾在水中形成的AI(OH)3胶体能吸收水中悬浮物,可用于水的净化 | |
| B. | Sio2是良好的半导体材料,常用于制造计算机的芯片 | |
| C. | Fe2O3俗称铁红,常用作红色的油漆和涂料 | |
| D. | 浓硫酸在常温下可用铁制容器保存 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 盐酸 | 50mL | 50mL | 50mL |
| m(混合物) | 9.2g | 14.2g | 27.6g |
| V(CO2)(标准状况) | 2.2L | 3.36L | 3.36L |
| A. | 混合物中NaHCO3、KHCO的物质的量之比为1:2 | |
| B. | 当混合物质量为14.2g时,50mL盐酸恰好完全反应 | |
| C. | 盐酸的物质的量浓度为3.0mol/L | |
| D. | 9.2g混合物加热,固体质量减少2.2g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向某溶液中加入先加氯水,再加KSCN溶液后显红色,该溶液中一定含Fe2+ | |
| B. | 向某溶液中加入硝酸酸化的硝酸银溶液,出现白色沉淀,该溶液中一定含Cl- | |
| C. | 向某溶液中加入盐酸酸化的氯化钡溶液,出现白色沉淀,该溶液中一定含SO42- | |
| D. | 向某溶液中加入稀盐酸,产生的气体能使澄清石灰水变浑浊,该溶液中一定含CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
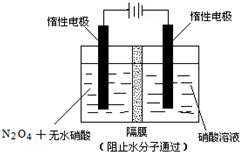 N2O5是一种新型硝化剂,其性质和制备受到人们的关注.
N2O5是一种新型硝化剂,其性质和制备受到人们的关注. .
.| t/s | 0 | 500 | 1000 |
| c(N2O5)/mol•L-1 | 5.00 | 3.52 | 2.48 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com