
分析 (1)将3.2molA和1molB两种气体混合于固定容积为2L的密闭容器中,c(A)=1.6mol/L,c(B)=0.6mol/L,则
3A(g)+B(g)?x C(g)+2D(s)
起始:3 mol 1 mol 0 0
转化:1.2 mol 0.4mol 0.4xmol 0.8 mol
平衡:1.8mol 0.6mol 0.4xmol 0.8 mol
根据平衡时C的浓度计算出x的值及结合平衡常数的定义和反应原理,写出此反应的平衡常数表达式;
(2)要提高A的转化率主要是通过外界因素的影响促进平衡正向移动,常见影响平衡的因素有温度、浓度及压强,由此分析判断;
(3)根据(1)中分析可直接计算出3min末B的反应速率;
(4)可逆反应达到平衡状态时,正逆反应速率相等(同种物质)或正逆反应速率之比等于系数之比(不同物质),平衡时各种物质的物质的量、浓度等不再发生变化,由此衍生的一些物理量不变,以此分析;
(5)反应2A(g)+B(g)?2C(g)中,气体的体积前后不相同,在一定温度下,在恒容密闭容器中得到平衡状态,只要满足物质全部转化为A、B,且满足n(A)=2mol,n(B)=1mol,即可得到完全相同平衡状态,此时平衡状态中B的体积分数仍为a%,若要平衡后B的体积分数大于a%,说明重新平衡B的物质的量要增大,如根据等效平衡,在完全等效的基础上再增加生成物或减小A的量,都可以使平衡在等效的基础上,再逆向进行,据此进行判断即可.
解答 解:(1)将3molA和1molB两种气体混合于固定容积为2L的密闭容器中,c(A)=1.6mol/L,c(B)=0.6mol/L,则
3A(g)+B(g)?x C(g)+2D(s)
起始:3 mol 1 mol 0 0
转化:1.2 mol 0.4mol 0.4xmol 0.8 mol
平衡:1.8mol 0.6mol 0.4xmol 0.8 mol
2min末该反应达到平衡,测得C的浓度为0.2mol•L-1=$\frac{0.4xmol}{2L}$,解得:x=1;
D为固体,此反应的化学平衡常数表达式K=$\frac{c(C)}{{c}^{3}(A)•c(B)}$;
故答案为:1;$\frac{c(C)}{{c}^{3}(A)•c(B)}$;
(2)反应 3A(g)+B(g)?x C(g)+2D(s)平衡后,可以通过改变温度、增大压强、减小C的量或增大B的量促进平衡正向移动,提高A的转化率,故答案为:改变温度、增大压强、减小C的量、增大B的量;
(3)3min 末B的转化率为$\frac{1.2mol}{3mol}×100%$=40%,故答案为:40%;
(4)A.反应混合物中D为固体,其余都为气体,混合气体的总质量不确定,体积为定值,密度不变,能说明到达平衡状态,故A正确;
B.反应为反应前后气体体积减小的反应,固定容积的密闭容器,容器中的压强不再变化,说明气体的总物质的量不再发生变化,说明到达平衡状态,故B正确;
C.生成C的反应速率表示正反应速率,生成B的反应速率表示逆反应速率,正逆反应速率之比等于系数之比(不同物质),说明达到平衡状态,故C正确;
D.单位时间内生成3molA说明是逆反应速率,同时生成1molC说明是正反应速率,正逆反应速率之比等于系数之比(不同物质),说明达到平衡状态,故D正确;
E.混合气体的颜色不再改变,说明C的浓度一定,能说明达到平衡状态,故E正确;
故答案为:ABCDE;
(5)A.若将2 mol C全部转化为A、B,分别得到2 mol A和1 mol B,与原平衡状态相同,平衡后B的体积分数仍为a%,故A错误;
B.2molA、1molB和1molHe(不参加反应),可以看成在原等效平衡的基础上增加1mol不参加反应的He,恒温恒容条件下,平衡不移动,B的物质的量不变,但平衡后B的体积分数小于a%,故B错误;
C.2molA和2molB,可看成在2molA和1molB的基础上增加1molB,瞬间B的体积分数增大,平衡正向移动,根据勒夏特列原理,平衡后B的体积分数大于a%,故C正确;
D.2molA、1molB和2molC,相当于4molA和2molB,在恒温恒容条件下,平衡状态应正向进行,B的转化率增大,则平衡后B的体积分数小于a%,故D错误;
故答案为:C.
点评 本题考查化学反应速率的计算、平衡常数及转化率的计算、判断可逆反应达到了化学平衡状态和等效平衡的应用等,题目难度中等,其中(5)注意与原配比数相比较,结合浓度对平衡移动的影响进行判断.


科目:高中化学 来源: 题型:选择题
| A. | 它的质量是32 g | B. | 约含有6.02×1023个O2分子 | ||
| C. | 含有2 mol O | D. | 红热的铁丝可在其中剧烈燃烧 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
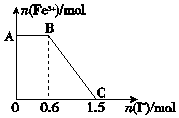 已知酸性K2Cr2O7溶液可与FeSO4反应生成Fe3+和Cr3+.现将硫酸酸化的K2Cr2O7溶液与FeSO4溶液混合,充分反应后再向所得溶液中加入KI溶液,混合溶液中Fe3+的物质的量随加入的KI的物质的量的变化关系如图所示,下列说法中不正确的是( )
已知酸性K2Cr2O7溶液可与FeSO4反应生成Fe3+和Cr3+.现将硫酸酸化的K2Cr2O7溶液与FeSO4溶液混合,充分反应后再向所得溶液中加入KI溶液,混合溶液中Fe3+的物质的量随加入的KI的物质的量的变化关系如图所示,下列说法中不正确的是( )| A. | 图中AB段的氧化剂为K2Cr2O7 | |
| B. | 图中BC段发生的反应为2Fe3++2I-=2Fe2++I2 | |
| C. | 开始加入的K2Cr2O7为0.15 mol | |
| D. | K2Cr2O7与FeSO4反应的物质的量之比为1:6 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯水宜保存在低温、避光条件下 | |
| B. | H2、I2、HI混合气体加压后颜色变深 | |
| C. | SO2催化氧化成SO3的反应,往往加入过量的空气 | |
| D. | 打开汽水瓶,看到有大量的气泡逸出 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 利用如图所示装置,当X、Y选用不同材料时,可将电解原理广泛应用于工业生产.下列说法中正确的是( )
利用如图所示装置,当X、Y选用不同材料时,可将电解原理广泛应用于工业生产.下列说法中正确的是( )| A. | 若Z是KCl溶液,则电解时溶液中Cl-向Y极移动 | |
| B. | 铜的精炼中,X是纯铜,Y是粗铜,Z是CuSO4 | |
| C. | 外加电流的阴极保护法中,Y是待保护金属 | |
| D. | 电解硫酸溶液一段时间后,加适量水可使溶液恢复到原溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
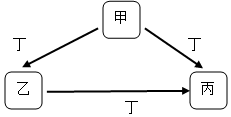 甲、乙、丙、丁均为中学化学常见物质,一定条件下它们有如下转化关系(其它产物已略去).
甲、乙、丙、丁均为中学化学常见物质,一定条件下它们有如下转化关系(其它产物已略去).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作和现象 | 结论 |
| A | 测定等物质的量浓度的Na2CO3和Na2SO3溶液的pH,前者的pH比后者的大 | 元素非金属性:S>C |
| B | 向盛有Fe(NO3)2溶液的试管中加入0.1mol•L-1 H2SO4溶液,试管口出现红棕色气体 | 溶液中NO被Fe2+还原为NO2 |
| C | 向FeBr2溶液中加入少量氯水,再加CCl4萃取,CCl4层无色 | Fe2+的还原性强于Br- |
| D | 向溶液中滴加盐酸酸化的BaCl2溶液,产生白色沉淀 | 溶液中一定含有SO42- |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com