
根据下列化学反应和事实,说明反应利用了硫酸的什么性质,将表示性质的选项的字母填在各小题的横线上。
A.不挥发性 B.酸性
C.吸水性 D.脱水性
E.强氧化性 F.强酸性
(1)浓硫酸可作气体干燥剂________;
(2)蔗糖中加浓H2SO4产生“黑面包”现象________;
(3)2NaCl+H2SO4(浓)Na2SO4+2HCl↑________;
(4)Zn+H2SO4(稀)===ZnSO4+H2↑________;
(5)Na2SO3+H2SO4(稀)===Na2SO4+SO2↑+H2O________;
(6)Cu+2H2SO4(浓)CuSO4+SO2↑+2H2O________;
(7)C+2H2SO4(浓)2SO2↑+2H2O+CO2↑________。
科目:高中化学 来源: 题型:
20世纪60年代初,英国年轻的化学家巴特列特用PtF6(六氟化铂)与等物质的量的氧气在室温下制得了一种深红色的固体,经实验确认,该化合物的化学式为O2PtF6,这是人类第一次制得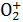 的盐。巴特列特头脑机敏,善于联想、类比和推理,考虑到稀有气体Xe(氙)和O2失去第一个电子的能量(称为第一电离能)几乎相等,他断定XePtF6也应存在。巴特列特立即动手实验,结果在室温下轻而易举制得了XePtF6黄色固体。根据以上叙述判断下列说法中不正确的是 ( )
的盐。巴特列特头脑机敏,善于联想、类比和推理,考虑到稀有气体Xe(氙)和O2失去第一个电子的能量(称为第一电离能)几乎相等,他断定XePtF6也应存在。巴特列特立即动手实验,结果在室温下轻而易举制得了XePtF6黄色固体。根据以上叙述判断下列说法中不正确的是 ( )
A.O2PtF6可能是离子化合物
B.XePtF6可能存在离子键
C.PtF6具有强氧化性
D.Xe的化合价一定为零
查看答案和解析>>
科目:高中化学 来源: 题型:
下列对于硝酸的认识,不正确的是( )
A.浓硝酸和稀硝酸都具有氧化性
B.铜与硝酸的反应属于置换反应
C.硝酸可氧化Fe2+
D.常温下可用铁或铝制品盛装浓硝酸
查看答案和解析>>
科目:高中化学 来源: 题型:
已知CO2过量时,CO2与NaOH反应生成NaHCO3(CO2+NaOH=NaHCO3)。参照物质的溶解度,用NaOH(固)、CaCO3(固)、水、盐酸为原料制取33 g纯NaHCO3。
| 25℃ | NaHCO3 | Na2CO3 | NaOH |
| 溶解度/g | 9 | 33 | 110 |
(1)若用100 g水,则制取时需用NaOH g。
(2)若用17.86 g NaOH(固),则需用水 g。
查看答案和解析>>
科目:高中化学 来源: 题型:
SO2溶于水后所得的溶液具有的性质是( )
A.有氧化性、无还原性、无酸性 B.有氧化性、有还原性、有酸性
C.有还原性、无氧化性、无酸性 D.有还原性、无氧化性、有酸性
查看答案和解析>>
科目:高中化学 来源: 题型:
有关亚硫酸的下列叙述中不正确的是( )
A.亚硫酸是SO2的水溶液,显酸性
B.SO3溶于水,剧烈反应生成亚硫酸
C.亚硫酸具有漂白性,能够使品红溶液褪色
D.亚硫酸不稳定,易分解为水和SO2
查看答案和解析>>
科目:高中化学 来源: 题型:
中学化学中很多“规律”都有适用范围,下列根据有关“规律”推出的结论正
确的是
| 选项 | 规律 | 结论 |
| A | 较强酸可以制取较弱酸 | 次氯酸溶液无法制取盐酸 |
| B | 反应物浓度越大,反应速率越快 | 常温下,相同的铝片中分别加入足量的浓、稀硝酸,浓硝酸中铝片先溶解完 |
| C | 结构和组成相似的物质,沸点随相对分子质量增大而升高 | NH3沸点低于PH3 |
| D | 溶解度小的沉淀易向溶解度更小的沉淀转化 | ZnS |
查看答案和解析>>
科目:高中化学 来源: 题型:
盛有12 mL NO2和O2的混合气体的量筒倒立于水槽中,充分反应后, 还剩余2 mL无色气体,则原混合气体中O2的体积是 ( )
还剩余2 mL无色气体,则原混合气体中O2的体积是 ( )
A.1.2 mL  B.2.4 mL
B.2.4 mL
C.3.6 mL D.4.8 mL
查看答案和解析>>
科目:高中化学 来源: 题型:
把一定质量的铁完全溶解于某浓度的硝酸中收集到0.3 mol NO2和0.2 mol NO。向反应后的溶液中加入足量NaOH溶液充分反应,经过滤、洗涤后,把所得沉淀加热至质量不再减少为止。得到固体质量不可能为
A.18 g  B.24 g C.30 g D.36 g
B.24 g C.30 g D.36 g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com