
| A. | CH3OH | B. | 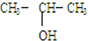 | ||
| C. | 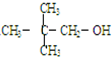 | D. | CH3-CH2-CH2-CH2OH |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
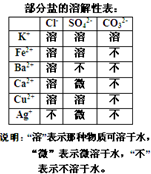 某混合物澄清透明的水溶液中,可能含有以下离子中若干种:K+、Ca2+、Fe2+、Cu2+、Cl-、CO32-、SO42-,现每次取该溶液100.00mL溶液进行以下实验:
某混合物澄清透明的水溶液中,可能含有以下离子中若干种:K+、Ca2+、Fe2+、Cu2+、Cl-、CO32-、SO42-,现每次取该溶液100.00mL溶液进行以下实验:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 可以根据PbI2和AgCl的Ksp的大小比较两者的溶解能力 | |
| B. | 常温下,同浓度的Na2S与NaHS溶液相比,NaHS溶液的pH大 | |
| C. | 能使碘化钾淀粉试纸变蓝的溶液中,Na+、S2-、Br-、NH4+等离子可以大量共存 | |
| D. | 等物质的量浓度的NH4Cl溶液和NH4HSO4溶液,后者的c(NH4+)大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K+、Na+、Cl-、SO42- | B. | NH4+、Na+、Cl-、CO32- | ||
| C. | K+、Na+、HCO3-、SO42- | D. | K+、Cu2+、H+、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2NO2(g)?N2O4 (g) | |
| B. | 2NO2(g)?2NO (g)+O2(g) | |
| C. | 2HI(g)?H2 (g)+I2(g) | |
| D. | FeCl3(aq)+3KSCN(aq)?Fe(SCN)3(aq)+3KCl(aq) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 5.6 g铁粉在0.1mol氯气中充分燃烧,转移电子数为0.3NA | |
| B. | 12.5mL 16mol•L-1浓硫酸与足量铜反应,转移电子数为0.2NA | |
| C. | 7.8g Na2S和Na2O2的混合物中含有的阴离子数等于0.1NA | |
| D. | 100mL0.1mol•L-1醋酸溶液含有的分子总数一定小于0.01NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.01mol/L | B. | 0.017mol/L | C. | 0.05mol/L | D. | 0.50mol/L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com