
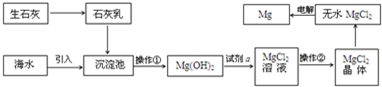
分析 海水提镁的主要流程分析可知,生石灰和水反应生成石灰乳,海水引入沉淀池加入石灰乳,利用氢氧化钙沉淀镁离子生成氢氧化镁沉淀,过滤得到氢氧化镁沉淀,加入盐酸溶液溶解得到氯化镁溶液,通过蒸发浓缩冷却结晶得到氯化镁晶体,在氯化氢气流中加热失水得到固体氯化镁,通电电解氯化镁得到镁合氯气,
(1)操作①是分离氢氧化镁沉淀,操作②加热浓缩、冷却结晶、过滤洗涤;
(2)试剂a是盐酸,用来溶解氢氧化镁得到氯化镁溶液;
(3)根据镁离子能与氢氧根离子反应生成沉淀来确定氢氧化钙的作用;
(4)根据海洋产品中与石灰石相同的物质进行解答;
(5)无水MgCl2在熔融状态下,通电后阳极氯离子失去电子生成氯气,阴极镁离子得到电子生成镁单质,发生氧化还原反应;
(6)氧化镁熔点为2852℃,无水MgCl2的熔点为714℃,MgO熔点很高,熔融时耗费大量的能量而增加生产成本.
解答 解:海水提镁的主要流程分析可知,生石灰和水反应生成石灰乳,海水引入沉淀池加入石灰乳,利用氢氧化钙沉淀镁离子生成氢氧化镁沉淀,过滤得到氢氧化镁沉淀,加入盐酸溶液溶解得到氯化镁溶液,通过蒸发浓缩冷却结晶得到氯化镁晶体,在氯化氢气流中加热失水得到固体氯化镁,通电电解氯化镁得到镁合氯气,
(1)分析可知操作①是分离氢氧化镁沉淀用过滤方法分离,操作②是溶液中得到溶质固体,需要加热浓缩、冷却结晶、过滤洗涤,得到氯化镁晶体在氯化氢气流中加热失水得到固体氯化镁,
故答案为:过滤;加热浓缩、冷却结晶、过滤洗涤,在氯化氢气流中加热失水;
(2)从氢氧化镁到氯化镁,氢氧化镁和盐酸反应得到氯化镁和水,反应的化学方程式为:Mg(OH)2+2HCl=MgCl2+2H2O,加入的足量试剂a是HCl,所以试剂a是盐酸,用来溶解氢氧化镁得到氯化镁溶液,
故答案为:盐酸;
(3)镁离子能与氢氧根离子反应生成氢氧化镁沉淀:Mg2++Ca(OH)2═Mg(OH)2+Ca2+,写离子方程式时氢氧化镁沉淀写化学式,
故答案为:Mg2++Ca(OH)2═Mg(OH)2+Ca2+;
(4)贝壳或牡蛎壳的主要成分为碳酸钙,故答案为:贝壳(或牡蛎壳等);
(5)无水MgCl2在熔融状态下,通电后阳极氯离子失去电子生成氯气,阴极镁离子得到电子生成镁单质,所以氯化镁电解会产生Mg和Cl2,
故答案为:MgCl2(熔融) $\frac{\underline{\;通电\;}}{\;}$Mg+Cl2↑;是;
(6)氧化镁熔点为2852℃,无水MgCl2的熔点为714℃,MgO熔点很高,熔融时耗费大量的能量而增加生产成本,
故答案为:MgO熔点很高,熔融时耗费大量的能量而增加生产成本.
点评 本题考查了从海水中提取镁的反应原理,利用所学知识结合流程图信息是解答本题的关键,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 水煤气,电能是一级能源 | |
| B. | 天然气,水力是二级能源 | |
| C. | 核能,煤,石油符合未来新能源标准 | |
| D. | 太阳能,生物质能,风能,氢能符合未来新能源标准 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属钠着火时,可用水或泡沫灭火器灭火 | |
| B. | 碱金属单质都可保存在煤油中 | |
| C. | 钠离子半径比钠原子半径小 | |
| D. | 碱金属中密度最小,熔、沸点最高的是铯 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向饱和的硫酸铵溶液中滴加蛋清溶液 | |
| B. | 日本核电站工作人员给核电机组注水降温 | |
| C. | 炼油厂蒸馏原油获得汽油、煤油等产品 | |
| D. | 露置于空气中的镁带表面逐渐变黑 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com